Clear Sky Science · pt
Dinâmica dependente da sequência e da escala de comprimento em biocondensados de proteínas desordenadas altamente carregadas
Por que gotículas minúsculas de proteína importam
Dentro de nossas células, muitas reações vitais ocorrem em estruturas macias e semelhantes a gotículas que não têm membrana ao redor. Esses “condensados biomoleculares” se comportam como pequenos compartimentos líquidos e geralmente são formados por proteínas flexíveis e altamente carregadas. Experimentos mostraram que moléculas dentro de algumas dessas gotículas podem se mover surpreendentemente rápido, mesmo quando as gotículas como um todo parecem bastante espessas e pegajosas. Este artigo faz uma pergunta simples, porém importante: como a ordem exata de cargas positivas e negativas ao longo dessas proteínas controla a rapidez com que as coisas se movem dentro dessas gotículas?
Construindo gotículas a partir de cadeias flexíveis e carregadas
Os autores concentram-se em proteínas intrinsecamente desordenadas — cadeias longas e flexíveis que não se dobram em formas rígidas. Muitas dessas cadeias carregam tanto cargas positivas quanto negativas, arranjadas em diferentes padrões ao longo de seu comprimento. Usando simulações computacionais em grande escala, a equipe criou gotículas modelo formadas por muitas cópias dessas proteínas, junto com água e pequenos íons, para imitar o interior congestionado de condensados reais. Eles variaram sistematicamente o quão “blocky” era o padrão de cargas, desde sequências em que cargas positivas e negativas se alternam até sequências em que todas as cargas positivas estão agrupadas e todas as negativas formam um bloco separado.
Conteúdo de água e fluxo hidráulico moldam o movimento
As simulações revelaram que essas gotículas ainda podem se comportar como líquidos verdadeiros com um teor muito alto de água — entre cerca de 55% e 84%, dependendo do padrão de cargas. Essa quantidade de água significa que o fluxo do fluido, ou hidrodinâmica, não fica completamente suprimido como muitas teorias para soluções poliméricas densas sugeririam. Ao rastrear como os segmentos das proteínas vagam ao longo do tempo, os autores encontraram padrões de movimento característicos de cadeias cuja mobilidade é auxiliada pelo fluido circundante, em vez de ser apenas retardada pelo atrito. Essa influência hidrodinâmica persiste até e mesmo além do tamanho de uma cadeia proteica inteira, especialmente em gotículas formadas por sequências com cargas mais misturadas e, portanto, mais água.
Padrões locais de carga controlam a flexibilidade em microescala
Olhando mais de perto, os autores examinaram como trechos curtos de cada cadeia relaxam e se reorganizam dentro da gotícula. Porções diferentes da mesma proteína, contendo o mesmo número de blocos construtores, podiam se mover em velocidades muito distintas dependendo de sua mistura local de cargas positivas e negativas. Trechos com carga mais equilibrada relaxavam mais rapidamente, enquanto segmentos dominados por um tipo de carga moviam-se de forma mais lenta. Surpreendentemente, essas diferenças permaneceram fortes mesmo que argumentos simples de blindagem previssem que efeitos eletrostáticos seriam de curto alcance em condições tão salgadas e congestionadas. O trabalho mostra que o fato de as cargas estarem ligadas ao longo de uma cadeia preserva correlações elétricas de longo alcance que afetam fortemente o movimento local.
A viscosidade depende do tamanho da escala que você sondar
A equipe então investigou quão “espessas” essas gotículas parecem a diferentes escalas de comprimento. Usando um método que relaciona pequenas ondulações no momento do fluido à sua resistência ao escoamento, eles calcularam uma viscosidade que depende da escala de sondagem. Para todas as sequências, o fluido parece mais fino quando sondado em escalas muito pequenas e mais espesso quando sondado em toda a gotícula. Essa dependência de escala é especialmente dramática para as sequências com cargas agrupadas: para o padrão mais segregado, a viscosidade a granel é mais de vinte vezes maior que a viscosidade local, ao nível de um monômero. Em contraste, gotículas de sequências bem misturadas mostram uma diferença muito menor. No geral, a viscosidade a granel cresce acentuadamente com a concentração de proteína, em acordo com o comportamento de soluções de polímeros neutros densos, mesmo que as próprias proteínas sejam altamente carregadas.
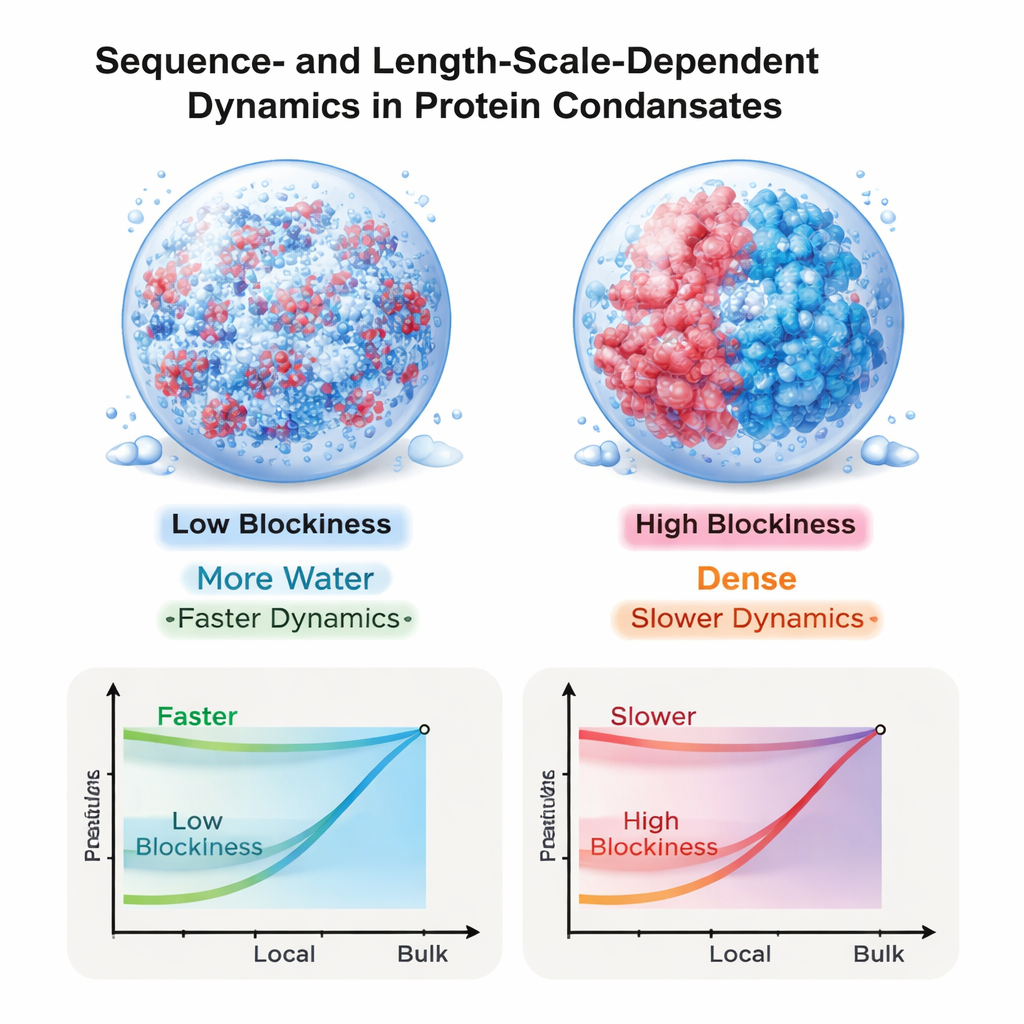
Conectando simulações a experimentos intrigantes
Esses resultados ajudam a resolver um paradoxo aparente de experimentos recentes: como pequenas moléculas e trechos de proteína podem difundir tão rapidamente dentro de condensados que, medidos como um todo, parecem extremamente viscosos? A resposta que emerge deste trabalho é que tanto o fluxo de água quanto interações elétricas de longo alcance continuam importantes nessas gotículas, e seu impacto é rigidamente controlado por como as cargas são ordenadas ao longo de cada cadeia. Sequências com padrões de carga em blocos produzem gotículas densas e altamente viscosas que, ainda assim, permanecem relativamente fluidas em escalas microscópicas, enquanto sequências mais misturadas geram ambientes uniformemente mais móveis. Ao demonstrar que a sequência de cargas pode ajustar o movimento de maneira diferente em distintas escalas de comprimento, o estudo oferece um princípio de projeto para engenheirar materiais sintéticos à base de proteína e lança luz sobre como as células podem programar o comportamento de condensados por meio da sequência detalhada de suas proteínas desordenadas.
Citação: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Palavras-chave: condensados biomoleculares, proteínas intrinsecamente desordenadas, padrões de carga, dinâmica de proteínas, viscosidade