Clear Sky Science · pt
Um fluxo de trabalho integrado para a elucidação da estrutura de pós nanocristalinos
Por que cristais minúsculos importam
Muitos medicamentos modernos e materiais avançados são produzidos como pós finos, não como belos cristais brilhantes. Isso é um problema para os cientistas, porque nossa melhor ferramenta para ver como os átomos se organizam em um sólido — a cristalografia de raios X — precisa de cristais grandes e perfeitos. Este artigo apresenta uma nova estratégia passo a passo para determinar a estrutura atômica completa de pós teimosos em escala nanométrica, do tipo frequentemente gerado por métodos de manufatura mais verdes que economizam solvente. Entender essas estruturas pode ajudar a melhorar como os fármacos se dissolvem, sua estabilidade e a confiabilidade de sua ação no organismo.
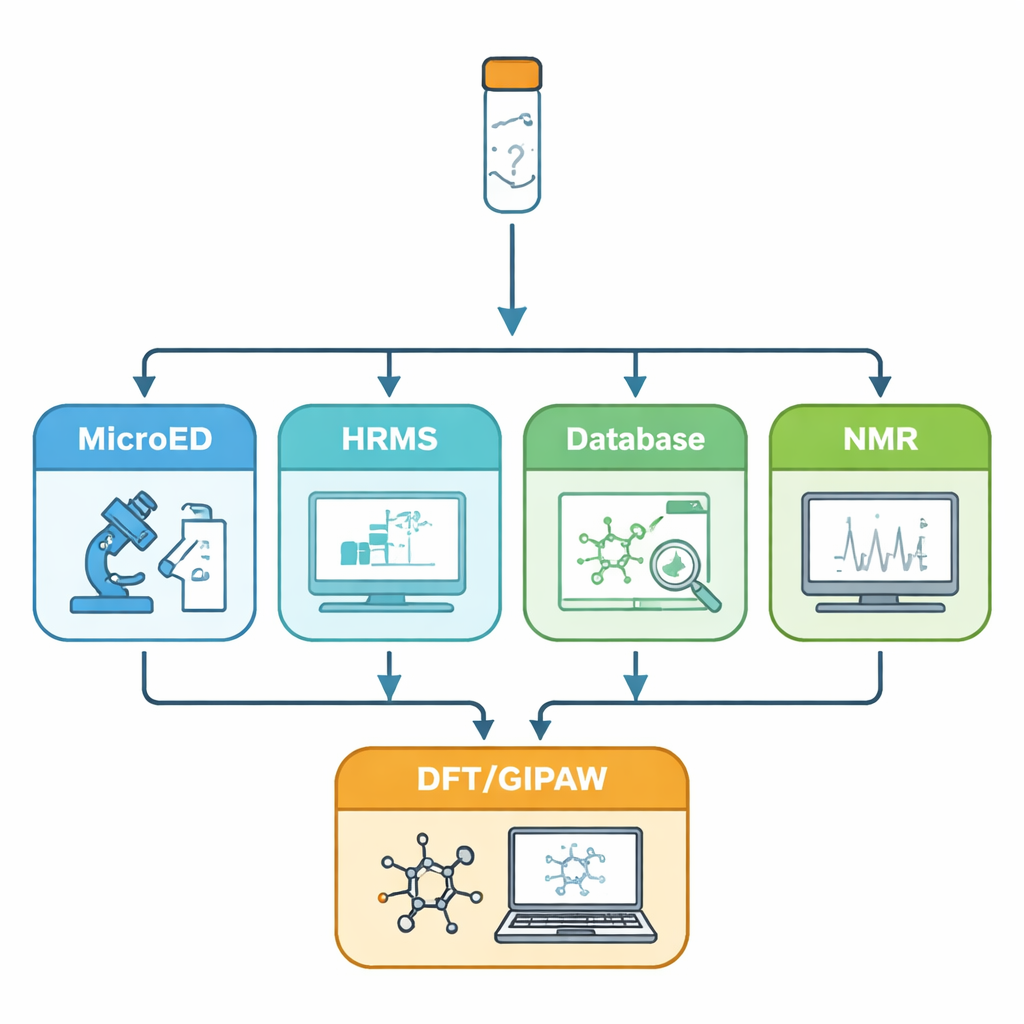
O desafio dos átomos invisíveis
Métodos mecanocatalíticos, como triturar reagentes em um moinho em vez de dissolvê‑los em grandes volumes de solvente, têm ganhado popularidade em linha com os princípios da química verde. Eles podem gerar novas formas sólidas de fármacos — como sais e corcristais — que ajustam propriedades como solubilidade e vida de prateleira. Mas os mesmos processos que tornam esses métodos atraentes também complicam a vida dos cristalógrafos: normalmente produzem apenas cristais na escala nano ou micro, por vezes misturados com material amorfo. A difração de raios X em único cristal tradicional não lida com grãos tão pequenos, enquanto a difração de raios X em pó frequentemente encontra dificuldades diante da complexidade dos sólidos farmacêuticos modernos.
Um conjunto de ferramentas para ver o invisível
Nos últimos anos, a difração eletrônica de microcristais (MicroED) emergiu como uma maneira poderosa de obter informação ao nível atômico a partir de cristais com apenas algumas centenas de nanômetros. Elétrons interagem com a matéria mais fortemente que raios X, portanto mesmo esses cristais minúsculos podem gerar padrões de difração nítidos. O MicroED pode revelar a disposição básica — ou “esqueleto” — das moléculas no sólido. No entanto, possui duas lacunas importantes: átomos de hidrogênio são muito difíceis de visualizar, e átomos como carbono, nitrogênio e oxigênio podem ser complicados de distinguir entre si. Os autores enfrentam essas limitações combinando MicroED com uma série de ferramentas complementares: espectrometria de massa de alta resolução para determinar a fórmula molecular exata, buscas em bancos de dados para sugerir identidades moleculares plausíveis, espectroscopia de RMN em solução e no estado sólido para confirmar quais moléculas estão presentes e como interagem, e cálculos quântico‑mecânicos para refinar e validar a estrutura final.
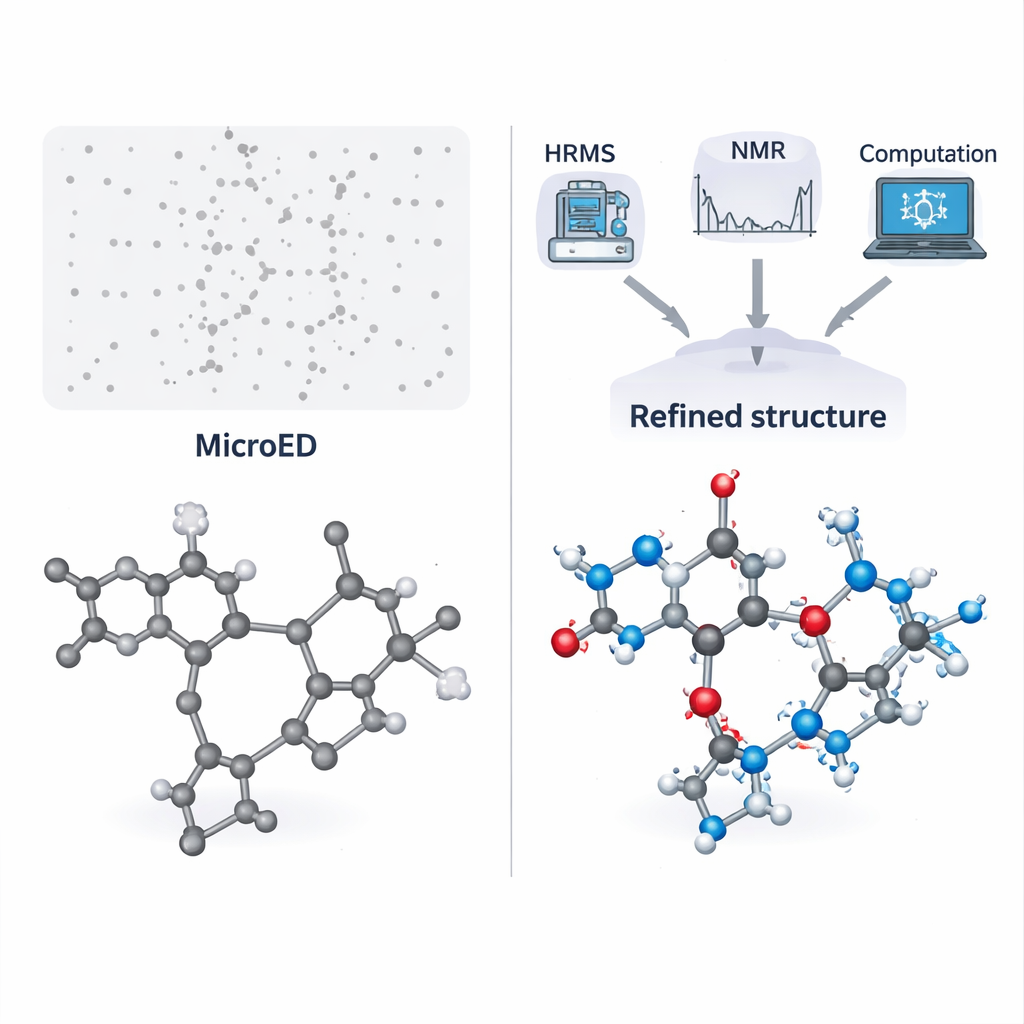
Resolvendo dois quebra‑cabeças do mundo real
A equipe aplica primeiro esse fluxo de trabalho a um sal desafiador formado por piridoxina (uma forma de vitamina B6) e o antioxidante N‑acetil‑L‑cisteína. Esse material só pode ser obtido por moagem a seco, e tentativas repetidas de cultivar cristais únicos adequados falharam porque o produto é pegajoso. O MicroED mostrou que o pó continha dois componentes moleculares diferentes e até sugeriu a presença de um átomo de enxofre, mas não conseguiu atribuir com segurança todos os demais átomos nem os hidrogênios. A espectrometria de massa de alta resolução revelou dois pesos moleculares precisos, que foram então usados para buscar em bancos de dados estruturas correspondentes. Comparando esses candidatos com o esqueleto obtido por MicroED e verificando características chave com RMN em solução, os autores reduziram as possibilidades e identificaram com confiança os dois parceiros como piridoxina e N‑acetil‑L‑cisteína.
Do esboço bruto à imagem final
Uma vez conhecidas as identidades moleculares, cálculos quântico‑químicos assistidos por computador foram usados para relaxar suavemente a estrutura derivada de MicroED e prever os deslocamentos químicos de RMN. Esses sinais de RMN calculados foram então comparados com dados de RMN no estado sólido do pó real. A excelente concordância confirmou que as posições atômicas, incluindo a maioria dos hidrogênios, estavam corretas. Experimentos adicionais de RMN concentraram‑se em um hidrogênio crucial compartilhado entre as duas moléculas, permitindo à equipe medir sua distância até um átomo de nitrogênio com grande precisão. Isso mostrou que o par forma um sal verdadeiro, e não um corcristal neutro — uma distinção importante para o comportamento do fármaco e para sua classificação regulatória. O mesmo fluxo de trabalho foi testado em um segundo composto, bastante diferente: um pequeno tripeptídeo chamado fMLF, amplamente usado como sistema modelo em estudos de RMN, mas cuja estrutura no estado sólido nunca havia sido relatada. Novamente, a abordagem integrada entregou com sucesso uma estrutura totalmente validada e até esclareceu movimentos rápidos do anel aromático.
Como isso ajuda a ciência e a medicina
Ao tratar cada pó desconhecido como um “teste cego”, os autores mostram que seu fluxo de trabalho modular pode partir de informações muito limitadas e ainda assim chegar a uma estrutura atômica completa e confiável. O MicroED fornece um primeiro esboço, a espectrometria de massa e os bancos de dados identificam moléculas candidatas, a RMN esclarece quantos componentes estão presentes e onde se localizam os hidrogênios, e os cálculos quânticos unem tudo. Para químicos e cientistas farmacêuticos, isso significa que pós complexos nanocristalinos produzidos por rotas de fabricação verdes não precisam permanecer mistérios estruturais. O método abre a porta para caracterizações rotineiras e detalhadas de pós — de pigmentos a formulações farmacêuticas — mesmo quando o crescimento tradicional de cristais falha, ajudando a projetar materiais mais seguros e eficazes desde o início.
Citação: Sabena, C., Bravetti, F., Miyauchi, N. et al. An integrated workflow for the structure elucidation of nanocrystalline powders. Commun Chem 9, 97 (2026). https://doi.org/10.1038/s42004-026-01902-1
Palavras-chave: MicroED, RMN no estado sólido, pós nanocristalinos, síntese mecanocatalítica, sais farmacêuticos