Clear Sky Science · pt
Dinâmica da fotooxidação de CO para CO2 sobre rutila (110)
Por que observar moléculas em um trilionésimo de segundo importa
A vida moderna depende de reações químicas que limpam nosso ar e água e convertem a luz solar em energia utilizável. Muitas dessas reações ocorrem nas superfícies de materiais sólidos chamados fotocatalisadores, que são acionados pela luz. Este estudo investiga uma dessas reações — como o venenoso monóxido de carbono (CO) é transformado em dióxido de carbono (CO2) sobre uma superfície de dióxido de titânio — em escalas de tempo de meros quadrilionésimos de segundo. Entender esses passos ultrarrápidos pode ajudar cientistas a projetar materiais mais inteligentes para controle de poluição, superfícies autolimpantes e tecnologias de energia solar.
Uma equipe de limpeza acionada pela luz
O dióxido de titânio é um material versátil encontrado em vidros autolimpantes, revestimentos purificadores de ar e dispositivos experimentais de combustíveis solares. É barato, estável e pode usar a luz para desencadear reações de limpeza poderosas em sua superfície. Mas nem todas as formas de dióxido de titânio se comportam da mesma maneira. Duas formas comuns, chamadas anatase e rutila, diferem em quão eficientemente promovem reações como a transformação de CO em CO2. Embora a anatase seja geralmente mais ativa no conjunto, o tempo detalhado dos passos individuais da reação — especialmente como o oxigênio do ar é ativado — permaneceu pouco claro. Este estudo foca na forma rutila com uma orientação de superfície específica, conhecida como (110), para ver exatamente quão rápido o CO é oxidado após a incidência da luz.
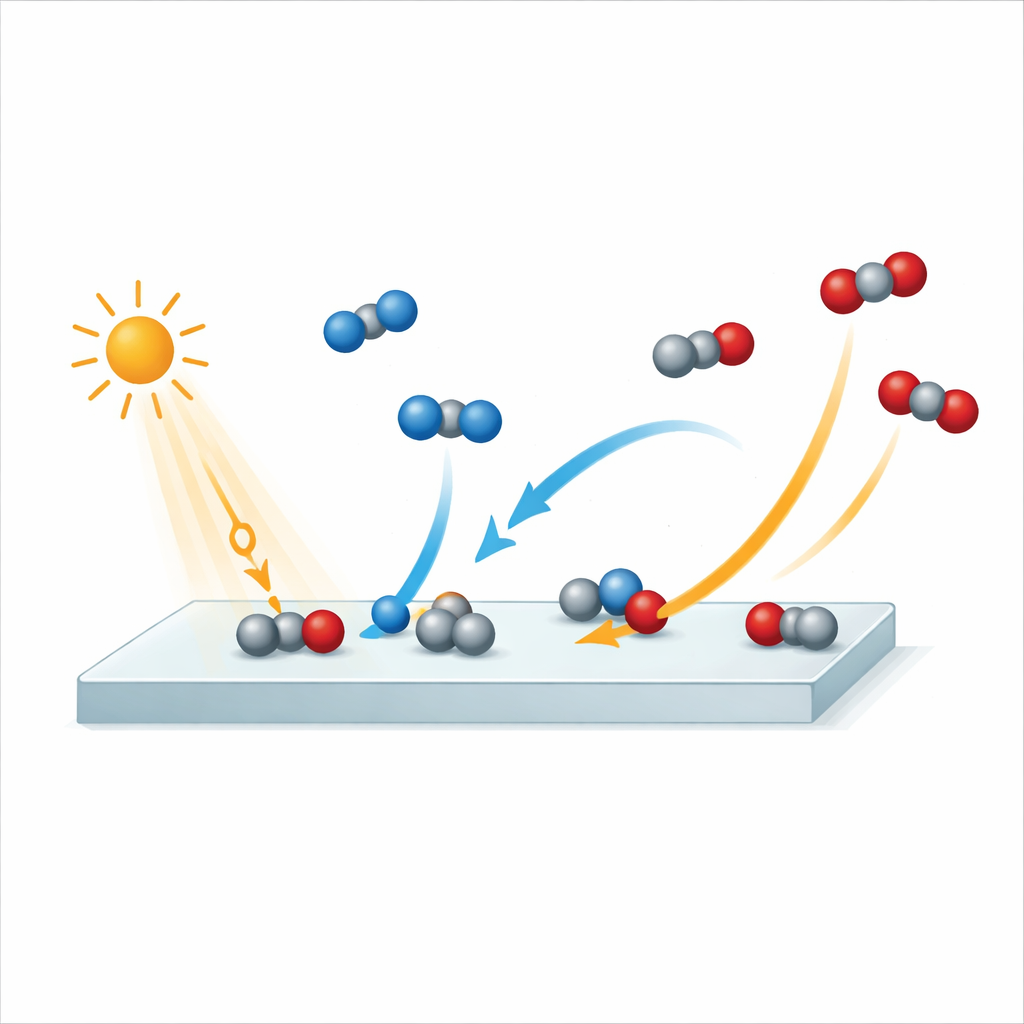
Filmando uma reação em velocidade extrema
Para capturar esse processo, os pesquisadores utilizaram uma instalação de laser de elétrons livres em Hamburgo que produz flashes extremamente curtos de raios X. Primeiro eles atingiram a superfície de rutila com um pulso de luz infravermelha, atuando como um minúsculo flash que inicia a reação. Um pulso de raios X, cuidadosamente cronometrado, então sondou como os átomos e elétrons na superfície mudaram. Repetindo essa sequência com diferentes atrasos entre os pulsos de luz e raios X, construíram uma espécie de “filme molecular” da reação com resolução temporal de cerca de 250 femtossegundos — um femtossegundo é um milionésimo de bilionésimo de segundo. A equipe monitorou sinais de átomos de oxigênio na superfície e nas moléculas gasosas, permitindo distinguir entre CO, CO2, água e o óxido em si conforme a reação se desenrolava.
Detectando CO2 em menos de um trilionésimo de segundo
A observação chave é que novo CO2 aparece na superfície de rutila em tão pouco quanto 200 a 800 femtossegundos após o pulso de luz. Isso significa que o oxigênio de moléculas O2 próximas é ativado, ligações são quebradas e o CO é convertido em CO2 em menos de um trilionésimo de segundo. Após cerca de 0,8 picosegundos, o sinal do CO2 recém-formado diminui à medida que o produto dessorve da superfície. Curiosamente, toda essa sequência ocorre mais rapidamente na rutila do que na anatase, onde trabalhos anteriores encontraram o primeiro CO2 surgindo apenas após cerca de 1,2 a 2,8 picosegundos em condições semelhantes. Mesmo que a anatase produza mais CO2 no total e seja considerada o fotocatalisador mais potente, a rutila realiza o passo crucial de oxidação mais rapidamente.
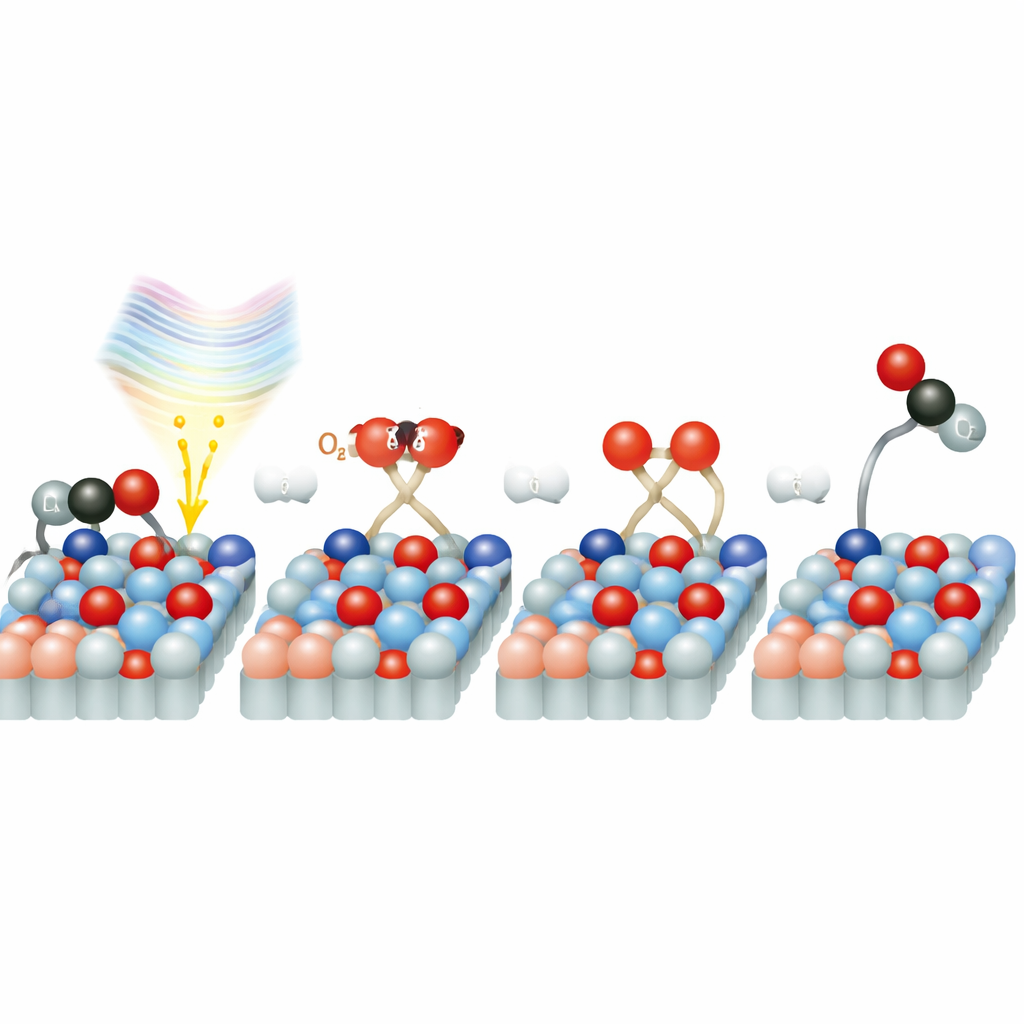
Um caminho alternativo para o oxigênio
Por que a reação é tão rápida na rutila? Simulações computacionais detalhadas sugerem que moléculas de oxigênio adsorvidas na superfície criam estados eletrônicos especiais que funcionam como uma ponte entre o sólido e o O2. Quando a luz do laser de 770 nanômetros é absorvida, ela pode mover diretamente um elétron do dióxido de titânio para a molécula de oxigênio, formando uma espécie de oxigênio carregada e ativada. Esse “atalho” evita a rota mais lenta em que os elétrons primeiro viajam pelo volume do sólido e depois migram até a superfície. Uma vez ativado, o oxigênio se divide rapidamente e um átomo de oxigênio se combina com o CO para formar CO2. O estudo também encontra que traços de água na superfície podem tanto bloquear sítios reativos quanto, em baixos níveis, potencialmente ajudar nessa transferência de carga e ativação do oxigênio, adicionando outra camada de complexidade.
Conectando estrutura eletrônica ao desempenho no mundo real
No conjunto, o trabalho mostra que detalhes minúsculos em como elétrons se movem entre uma superfície e moléculas próximas podem alterar dramaticamente as velocidades das reações, mesmo entre dois materiais intimamente relacionados. Enquanto a anatase ainda leva vantagem em termos de produção fotocatalítica total, a rutila mostra um passo de ativação do oxigênio mais rápido ligado a essa rota especial de transferência de carga. Ao unir medições ultrarrápidas e simulações avançadas, o estudo fornece um roteiro para ajustar superfícies de modo que reações acionadas pela luz aconteçam com maior eficiência. A longo prazo, tais insights podem ajudar engenheiros a projetar melhores revestimentos para purificação do ar, superfícies antibacterianas mais eficazes e materiais aprimorados para produção de combustíveis movidos a energia solar e para a divisão da água.
Citação: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Palavras-chave: fotocatálise, dióxido de titânio, espectroscopia ultrarrápida, química de superfícies, oxidação de monóxido de carbono