Clear Sky Science · pt
Desenvolvimento de um nanomodelo de pontos de carbono quadruplamente conjugados para terapia direcionada do glioma
Nova esperança para tumores cerebrais persistentes
Tumores cerebrais de alto grau, como o glioblastoma, estão entre os cânceres mais difíceis de tratar. Muitos medicamentos que funcionam em outras partes do corpo não conseguem atravessar a barreira hematoencefálica protetora do cérebro ou acabam danificando tecido saudável no trajeto. Este estudo descreve uma nanopartícula “inteligente” construída em laboratório que pretende infiltrar-se com mais precisão em tumores cerebrais, transportar um coquetel potente de drogas e liberá-lo diretamente no núcleo das células tumorais, onde pode causar o maior dano ao câncer poupando células normais.
Um minúsculo caminhão de entrega feito de carbono
No centro da nova abordagem estão os pontos de carbono — partículas na escala nanométrica feitas de carbono, baratas de produzir, compatíveis com água e que brilham sob certos tipos de luz. Como suas superfícies são ricas em ganchos químicos, podem ser decoradas com múltiplos componentes biológicos ao mesmo tempo. Neste trabalho, os pesquisadores criaram um nanomodelo “quadruplamente conjugado”: cada ponto de carbono foi ligado quimicamente, em uma única reação de um passo, a dois peptídeos de direcionamento diferentes e a dois princípios ativos anticâncer. Esse desenho modular transforma cada ponto em um pequeno caminhão de entrega capaz de reconhecer células tumorais, atravessar barreiras celulares e levar medicamentos ao endereço intracelular correto.
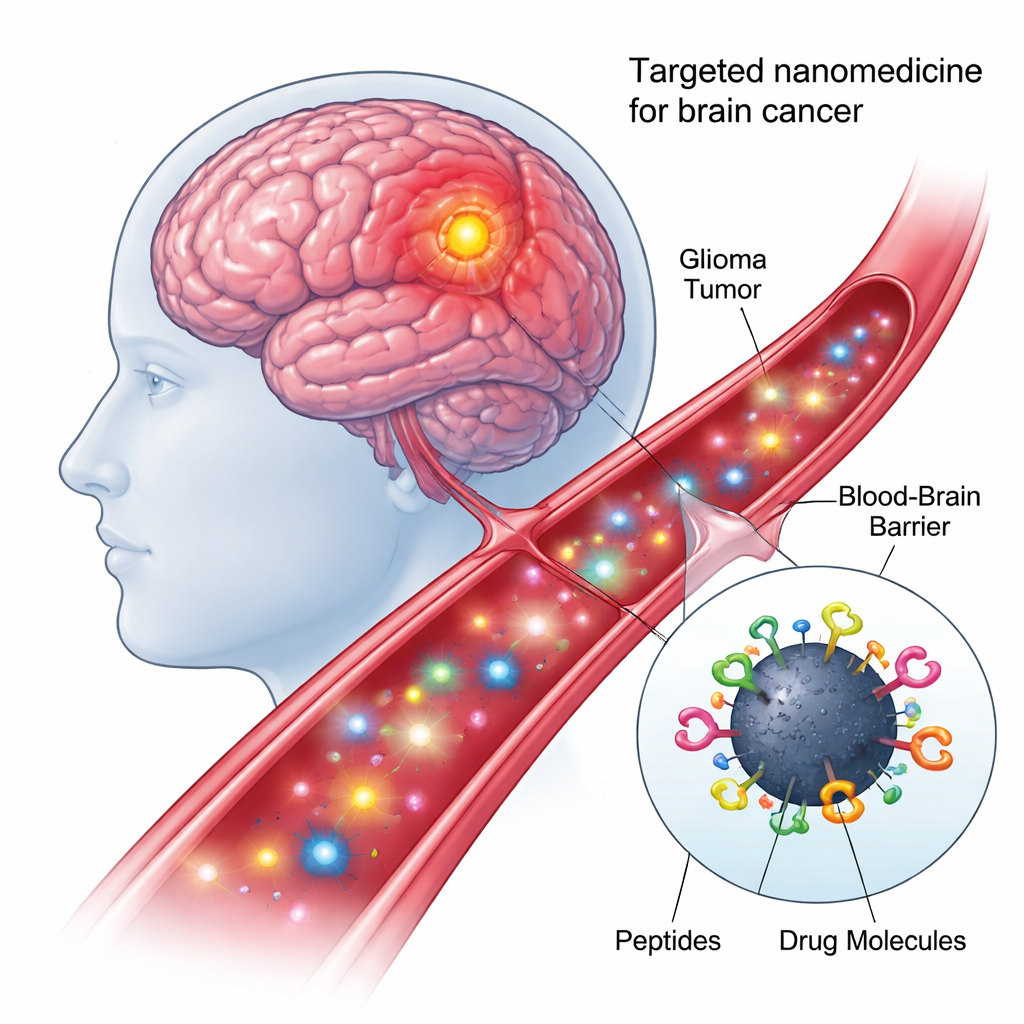
Encontrando e entrando nas células cerebrais certas
O primeiro peptídeo na nanopartícula, chamado shPep-1, foi projetado para reconhecer um receptor denominado IL13Rα2. Esse receptor é encontrado em níveis elevados em muitos tumores cerebrais agressivos — incluindo glioblastoma adulto e pediátrico e glioma pontino intrínseco difuso — mas aparece fracamente nas células cerebrais normais. Ao se ligar ao IL13Rα2, o shPep-1 ajuda os pontos de carbono a se direcionarem às células tumorais e a entrarem nelas por captação mediada por receptor. O segundo peptídeo, mais longo, lnPep-1, contém um sinal de localização nuclear: uma sequência curta que auxilia a carga a atravessar a membrana nuclear e alcançar o centro de comando da célula, onde o DNA é armazenado. Juntos, esses dois peptídeos conferem à nanopartícula tanto preferência tumoral quanto a capacidade de alcançar o núcleo uma vez no interior.
Desencadeando um ataque coordenado de drogas
A carga terapêutica consiste em duas pequenas moléculas. A primeira é a epirrubicina, um quimioterápico conhecido que mata células cancerosas ao inserir-se no DNA e bloquear enzimas necessárias para reparar quebras de fita dupla. A segunda é um metabólito chamado 5-aminoimidazol-4-carboxamida (AIC), produzido a partir do fármaco para tumores cerebrais temozolomida em pH fisiológico. Em trabalhos anteriores, o mesmo grupo mostrou que combinar epirrubicina e AIC em um ponto de carbono aumentava a morte de células cancerosas em comparação com cada fármaco isoladamente. No novo desenho, ambos são coentregues na nanopartícula de peptídeo duplo, buscando um efeito sinérgico diretamente no núcleo da célula tumoral.
Potente em células tumorais, mais suave com células normais
Para testar a eficácia do nanomodelo, a equipe expôs várias linhagens de glioma de alto grau — glioblastoma adulto, glioblastoma pediátrico e um modelo de glioma pontino intrínseco difuso — aos pontos de carbono quadruplamente conjugados. Mesmo em concentrações muito baixas (tão pouco quanto 50 nanomolar), a viabilidade das células tumorais caiu para cerca de metade dos controles não tratados e, em doses mais altas, todos os conjugados testados mataram a maioria das células tumorais. Importante, o nanomodelo quadruplo superou versões mais simples de “peptídeo único”, mesmo tendo menos epirrubicina no total. Quando testado em células de músculo liso vascular não cancerosas, foi muito menos tóxico: essas células precisaram de aproximadamente 25–40 vezes mais nanopartícula para observar perda de viabilidade semelhante, sugerindo uma janela de segurança útil impulsionada pelo direcionamento tumoral em vez de doses em força bruta.
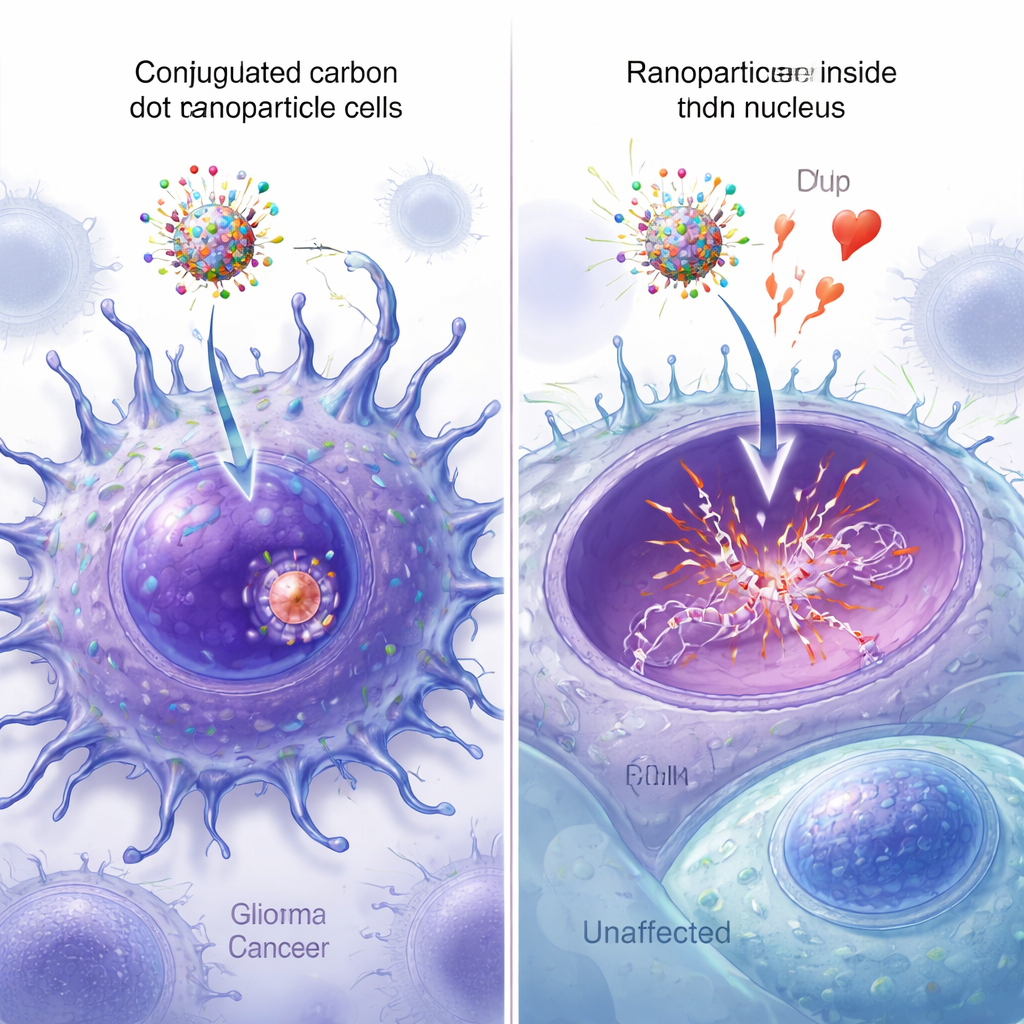
Observando as nanopartículas alcançarem o núcleo
Versões fluorescentes das nanopartículas permitiram aos pesquisadores acompanhar quão bem cada desenho entrava nas células e alcançava o núcleo. Ao microscópio, pontos de carbono equipados com ambos os peptídeos mostraram o sinal mais brilhante espalhado por toda a célula cancerosa, com forte sobreposição entre a fluorescência verde da nanopartícula e a coloração nuclear azul. A análise quantitativa de imagens confirmou que as partículas de peptídeo duplo apresentaram a maior colocalização nuclear, superando significativamente a de partículas com apenas um peptídeo ou sem peptídeo. Espectroscopia adicional, espectrometria de massa e medições por microscopia de força atômica verificaram que os quatro componentes foram efetivamente anexados aos pontos de carbono e aumentaram modestamente seu tamanho, sem prejudicar a função-chave de ligação ao DNA da epirrubicina.
O que isso pode significar para o cuidado futuro do câncer cerebral
Para os pacientes, essas descobertas ainda representam uma demonstração inicial em culturas celulares, não uma terapia pronta. Ainda assim, mostram um conceito promissor: uma nanopartícula pequena, estável e relativamente fácil de fabricar, baseada em carbono, que pode ser rapidamente customizada com peptídeos direcionadores e combinações de fármacos. Ao direcionar medicamentos especificamente a células tumorais que superexpressam IL13Rα2 e concentrá-los no núcleo, tais nanomedicamentos poderiam, um dia, permitir doses menores, menos efeitos colaterais e estratégias de tratamento mais personalizadas para tumores cerebrais altamente letais como o glioblastoma e o glioma pontino intrínseco difuso.
Citação: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Palavras-chave: glioblastoma, nanomedicina, pontos de carbono, liberação direcionada de medicamentos, tumores cerebrais