Clear Sky Science · pt
Um ensaio generalizável para acúmulo intracelular para perfilar a entrega citosólica de fármacos em células de mamíferos
Por que levar medicamentos para dentro das células importa
Muitos dos medicamentos mais promissores hoje — pequenas moléculas, curtos fragmentos de proteínas chamados peptídeos e proteínas em tamanho completo — são projetados para atuar em alvos dentro de nossas células. Mas a membrana celular é um portão de segurança rigoroso. Um fármaco pode aderir à superfície da célula ou ficar preso em sacos internos chamados endossomos e ainda assim nunca alcançar o interior aquoso, o citosol, onde muitos alvos residem. Este artigo descreve um novo teste laboratorial, chamado ensaio CHAMP, que informa aos pesquisadores não apenas se uma molécula entra na célula, mas se ela realmente chega ao citosol, onde pode exercer sua função.
Uma nova forma de rastrear a entrada de fármacos
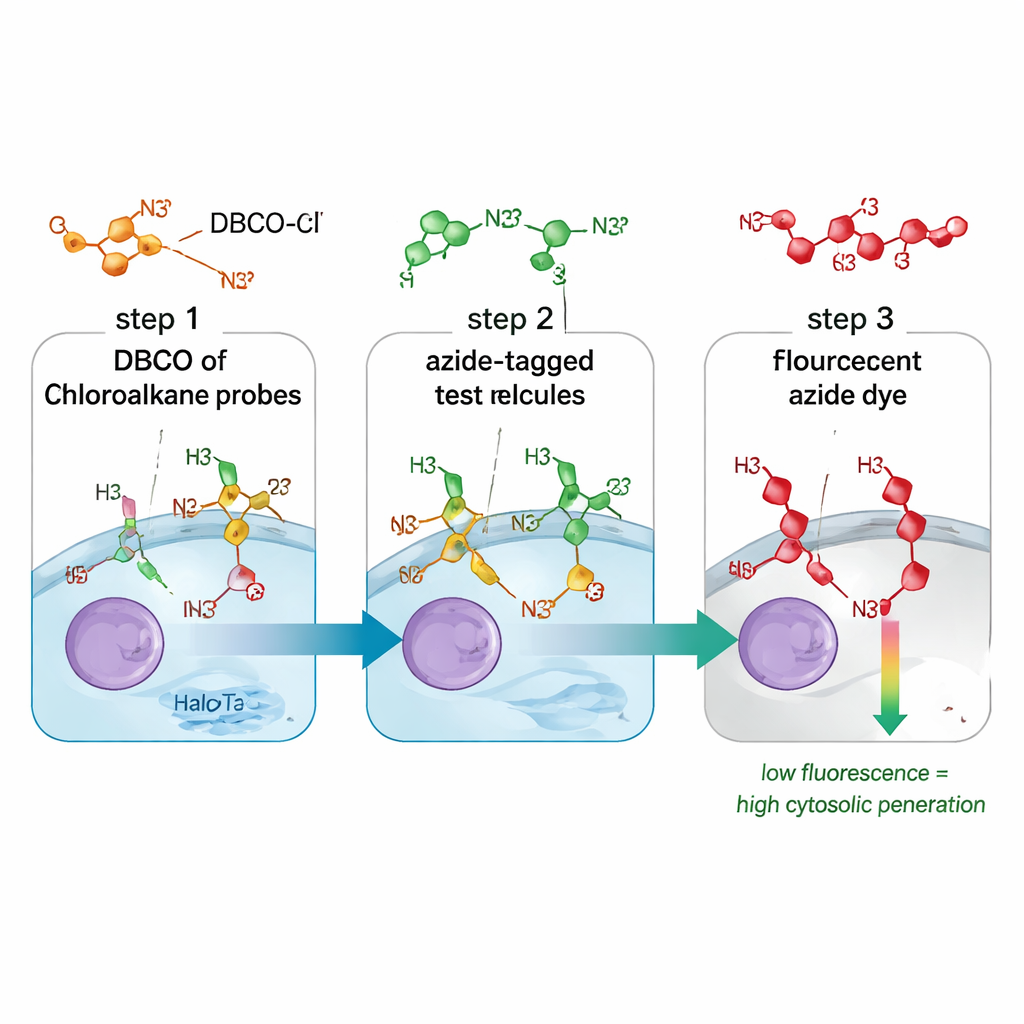
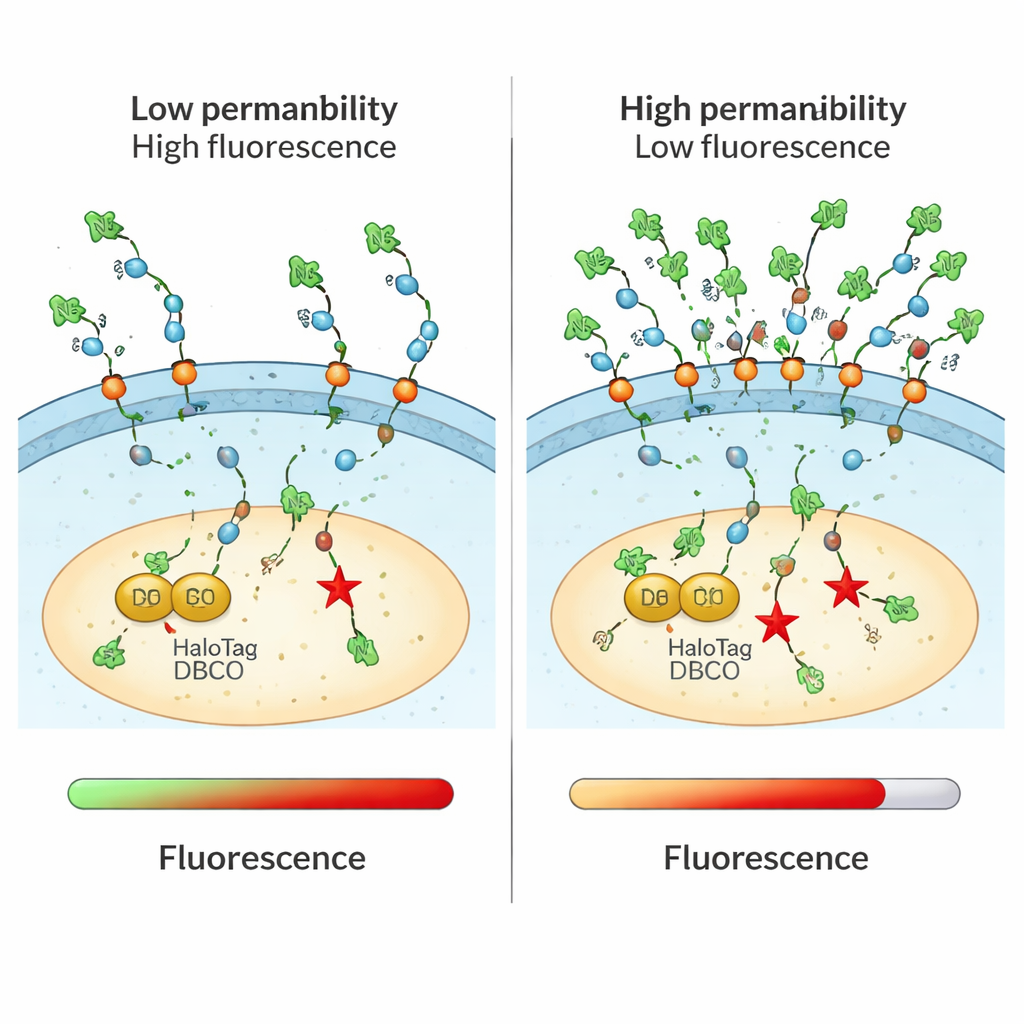
Métodos tradicionais para medir a absorção de fármacos frequentemente confundem moléculas que apenas tocam a superfície celular, ficam em endossomos ou alcançam com sucesso o citosol. Eles também podem depender de etiquetas fluorescentes volumosas que alteram o comportamento da molécula. O ensaio CHAMP resolve ambos os problemas ao combinar uma pequena “alça” química chamada azida com um marcador proteico chamado HaloTag, projetado para flutuar livremente no citosol de células humanas cultivadas. Primeiro, as células são tratadas com uma molécula ligadora que fixa DBCO, uma forma tensionada de alcino, ao HaloTag. Em seguida, os cientistas adicionam o composto em teste, que carrega a pequena etiqueta azida. Somente se esse composto atravessar a membrana celular até o citosol a azida e o DBCO podem reagir entre si em uma reação química altamente seletiva. Um corante fluorescente azida final revela quantos sítios DBCO permanecem livres: células fracas indicam que o composto de teste entrou e ocupou a maioria dos sítios; células brilhantes indicam pouco acesso citosólico.
Do conceito ao ensaio funcional
Os autores primeiro confirmaram que o HaloTag foi corretamente sintetizado e localizado no citosol de células humanas HeLa usando um corante cloroalcano padrão e imageamento. Em seguida, otimizaram cada etapa do CHAMP: quanto de ligador DBCO adicionar, por quanto tempo incubar e qual corante fluorescente azida produzia um sinal forte e específico sem prejudicar as células. Citometria de fluxo — um instrumento que mede fluorescência em milhares de células individuais — mostrou que o ensaio era rápido, robusto e ajustável. De forma crucial, a equipe demonstrou que a fluorescência realmente resultava de reações específicas nos sítios HaloTag em vez de corantes aderindo de forma inespecífica a componentes celulares, e que a pequena etiqueta azida não perturbava de forma perceptível a entrada das moléculas nas células.
O que o ensaio revela sobre pequenas drogas e peptídeos
Com o CHAMP em mãos, os pesquisadores o desafiaram com centenas de pequenas moléculas marcadas com azida e variaram sistematicamente características como carga, tamanho e flexibilidade. Observaram, por exemplo, que transformar um ácido carboxílico carregado negativamente em uma amida neutra aumentou o acúmulo citosólico, e que o grau e a posição da metilação de nitrogênio mudaram o quão bem os compostos penetravam. Ao comparar reações em Esferas livres versus células vivas, puderam separar a reatividade química intrínseca da barreira imposta pela própria membrana. A equipe também aplicou o CHAMP a um painel de antibióticos comuns, mostrando que alguns alcançavam o citosol muito melhor do que outros — informação importante ao tratar bactérias que se escondem dentro de células hospedeiras.
Peptídeos e proteínas supercarregados atravessando a barreira
O ensaio foi especialmente poderoso para estudar moléculas maiores e altamente carregadas, que são difíceis de rastrear por outros meios. Os autores examinaram peptídeos penetrantes de células formados por múltiplos resíduos de arginina e confirmaram uma tendência clara: cadeias mais longas e mais carregadas positivamente entregavam mais material no citosol, até certo ponto. Eles sondaram como reverter a quiralidade (estereoquímica) de certos aminoácidos alterava a entrada, descobrindo que versões em imagem espelho às vezes acumulavam melhor, sugerindo interações quirais sutis com a membrana. O CHAMP também mostrou que proteínas “supercarregadas” — projetadas para portar muitas cargas positivas — podiam alcançar o citosol mais efetivamente que suas contrapartes normais, sustentando seu potencial como vetores para grandes cargas terapêuticas.
Regras de projeto para futuros medicamentos intracelulares
Ao testar sistematicamente pequenas moléculas, peptídeos, peptídeos macrocíclicos e espinhas dorsais modificadas, o estudo revelou princípios gerais de projeto. Peptídeos macrocíclicos, cujas espinhas dorsais são fechadas em anéis, tendiam a atingir o citosol mais facilmente do que versões lineares flexíveis. Grupos N-metila cuidadosamente posicionados nas espinhas dorsais dos peptídeos aumentaram modestamente a entrada, mas excesso deles podia ser contraproducente. Essas relações estrutura–permeação, reveladas com um único ensaio padronizado, oferecem orientações práticas para químicos que buscam criar moléculas que não apenas se liguem aos alvos, mas que realmente cheguem até eles dentro das células.
Como isso ajuda o desenvolvimento de fármacos
Em termos simples, o ensaio CHAMP é um contador de tráfego finamente ajustado na porta e no corredor interno da célula. Ele informa aos cientistas quais fármacos experimentais realmente passam pela membrana e chegam ao citosol, sem serem enganados por moléculas presas na superfície ou em compartimentos internos. Como funciona com uma ampla variedade de formas e tamanhos moleculares e usa apenas uma pequena etiqueta azida, o CHAMP pode ser integrado a pipelines de descoberta de alto rendimento. Com o tempo, isso deve acelerar o desenho de tratamentos mais eficazes para doenças em que os alvos mais importantes estão trancados dentro de nossas células.
Citação: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Palavras-chave: entrega intracelular de fármacos, permeabilidade da membrana celular, acúmulo citosólico, peptídeos penetrantes de células, química de clique bioortogonal