Clear Sky Science · pt
Desidrocloração assistida por hidrogênio de 1,1,1,2-tetrafluoro-2-cloropropano para 2,3,3,3-tetrafluoropropeno sobre Pd-Ag/nano-MgF2 com sítios Pd isolados otimizados
Refrigerantes mais limpos para um mundo em aquecimento
Ar-condicionados e refrigeradores nos mantêm confortáveis, mas muitos dos químicos que os fazem funcionar são potentes gases de efeito estufa. Este estudo enfrenta um desafio crucial: como produzir de forma mais eficiente e com menor pegada de carbono um dos refrigerantes de próxima geração mais importantes, o HFO‑1234yf. Ao projetar um catalisador mais inteligente — essencialmente uma máquina química microscópica — os autores mostram uma maneira de fabricar esse refrigerante de baixo aquecimento a temperaturas mais baixas e com muito menos subprodutos indesejados.
Por que precisamos de uma química de refrigerantes melhor
Os hidrofluorocarbonos (HFCs) tradicionais, como o HFC‑134a usado em ar-condicionados de automóveis, aprisionam calor na atmosfera milhares de vezes mais fortemente que o dióxido de carbono. Acordos internacionais, como a Emenda de Kigali, estão reduzindo seu uso, empurrando a indústria em direção aos hidrofluoroalfenos (HFOs), que têm desempenho similar, mas potencial de aquecimento global muito menor (frequentemente abaixo de 10). O HFO‑1234yf é o principal candidato a substituto, contudo os métodos industriais atuais para sua produção dependem de etapas em alta temperatura e intensivas em energia que também encurtam a vida útil dos catalisadores e aumentam os resíduos. Uma rota mais fria e seletiva para o HFO‑1234yf poderia, portanto, reduzir tanto as emissões quanto os custos operacionais.
Uma via mais branda para uma molécula chave
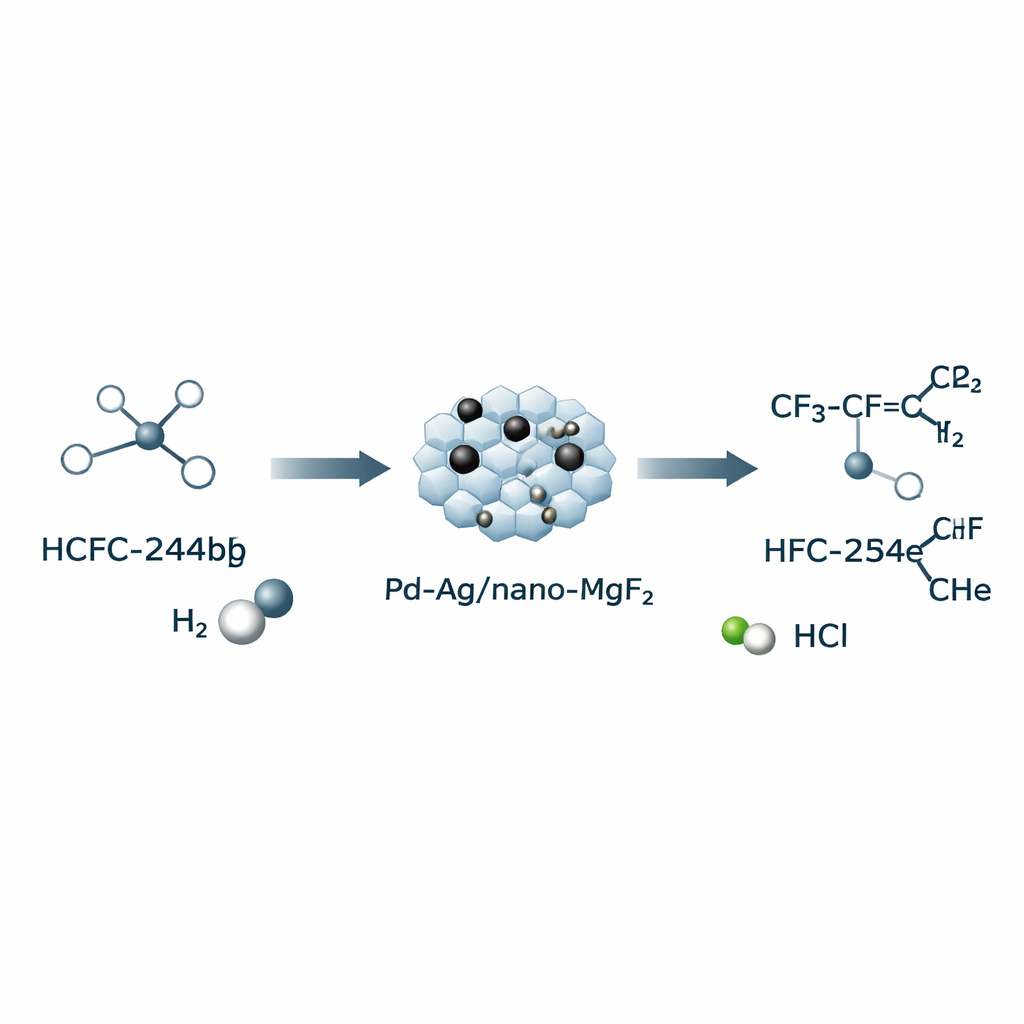
Os autores se concentram na conversão de um composto relacionado, HCFC‑244bb, em HFO‑1234yf pela remoção de cloreto de hidrogênio (HCl) com auxílio de gás hidrogênio. Essa “desidrocloração assistida por hidrogênio” permite que a reação ocorra a um 270 °C relativamente ameno — bem abaixo dos 600–800 °C frequentemente necessários em métodos puramente térmicos. O cerne do processo é um catalisador sólido feito sob medida: partículas ocas minúsculas de fluoreto de magnésio (nano‑MgF2) decoradas com paládio (Pd) e prata (Ag). Ao alterar a ordem de adição de Pd e Ag durante a preparação, a equipe consegue controlar o grau de mistura dos dois metais — formando ligas de caráter distinto — e como os sítios ativos de Pd aparecem na superfície durante a reação.
Transformando aglomerados metálicos em átomos isolados
Nas primeiras horas em operação, os catalisadores exibem um “período de indução”: a conversão de HCFC‑244bb declina lentamente, enquanto a seletividade para o desejado HFO‑1234yf aumenta de forma constante. Microscopia, espectroscopia e medidas de superfície cuidadosas revelam o porquê. À medida que a reação avança, o cloreto de hidrogênio formado in situ clora as partículas metálicas, fragmentando maiores aglomerados de Pd e remodelando-os em átomos de Pd isolados ancorados na superfície do nano‑MgF2. Catalisadores que começam com um maior grau de metalização Pd–Ag — alcançado quando Pd é adicionado primeiro e depois Ag — sofrem a reestruturação mais extensa e acabam com a maior densidade de sítios Pd de átomo único. Esse material otimizado converte cerca de 60% do HCFC‑244bb e direciona aproximadamente 82% do produto para HFO‑1234yf, enquanto suprime fortemente a hidrogenação mais profunda para um composto saturado indesejado, HFC‑254eb.
Como o comportamento do hidrogênio controla o resultado
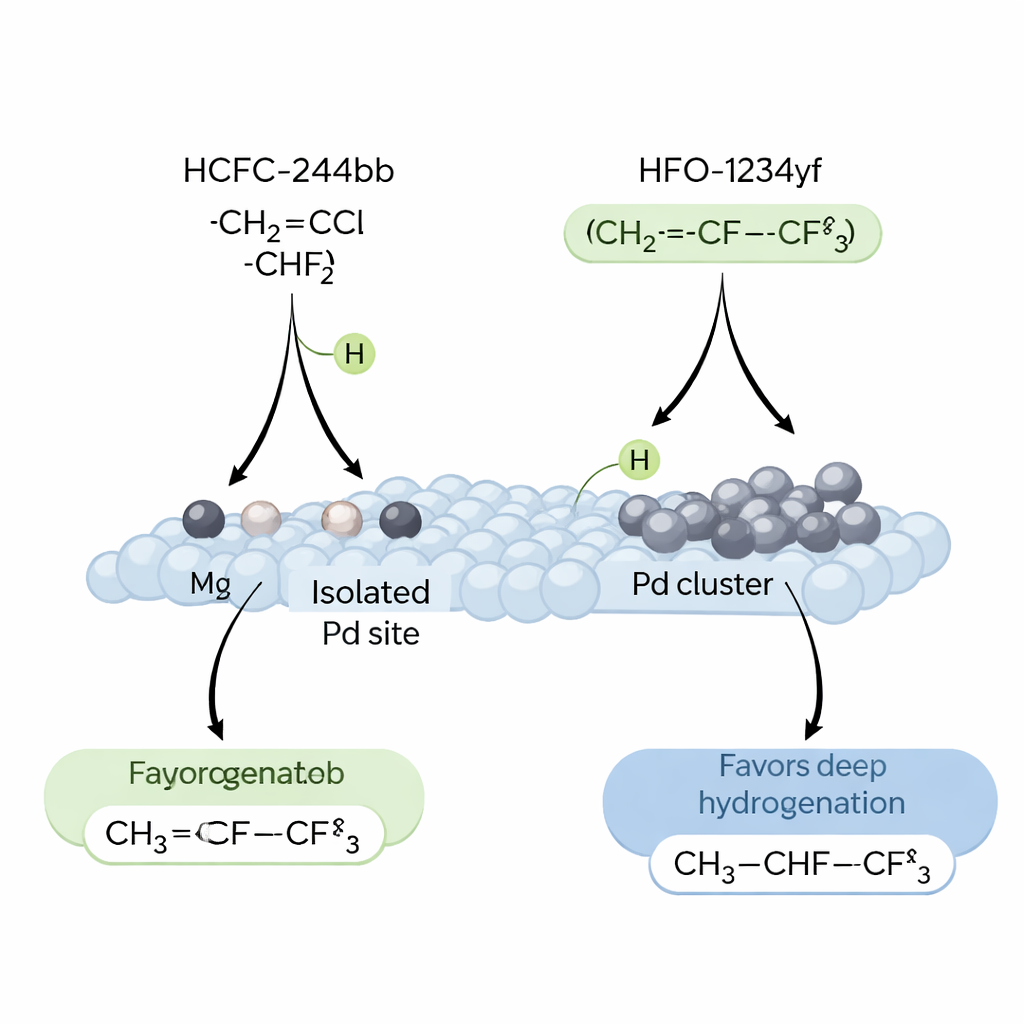
Para entender por que os átomos isolados de Pd apresentam desempenho superior, os pesquisadores investigaram como o hidrogênio, a molécula refrigerante inicial e o produto interagem com diferentes superfícies catalíticas. Eles descobriram que HCFC‑244bb e hidrogênio preferem se adsorver no Pd, não na Ag, mas que a força e a natureza da ligação do hidrogênio são cruciais. Grandes agregados de Pd tendem a criar hidrogênio de “spillover” que permanece fortemente ligado em altas temperaturas e promove a sobre‑hidrogenação, transformando o valioso HFO‑1234yf em produtos saturados menos úteis. Em contraste, sítios de Pd de átomo único retêm o hidrogênio em uma forma mais reativa, porém menos persistente — ideal para remover limpidamente o HCl e formar a dupla ligação carbono‑carbono desejada. Simulações computacionais usando teoria do funcional da densidade apoiam essa conclusão, mostrando que esses ambientes isolados Pd–fluoreto facilitam a remoção de hidrogênio de intermediários chave no caminho para o HFO‑1234yf, enquanto tornam energeticamente menos favoráveis as etapas secundárias de hidrogenação.
Do insight de laboratório ao resfriamento mais verde
Em termos práticos, o melhor catalisador Pd–Ag/nano‑MgF2 entrega taxas de formação de HFO‑1234yf dezenas de vezes maiores do que catalisadores sólidos anteriores que dependiam de desidrocloração severa em alta temperatura. O trabalho demonstra que controlar átomos metálicos um a um — não apenas como nanopartículas — pode guiar dramaticamente as vias reacionais, melhorando tanto a eficiência quanto a seletividade. Para não especialistas, a mensagem principal é que um desenho de catalisador melhor pode se traduzir diretamente em produção mais limpa de refrigerantes modernos. Isso, por sua vez, ajuda o mundo a alcançar metas climáticas ao mesmo tempo em que mantém nossos prédios, veículos e suprimentos alimentares refrigerados.
Citação: Yang, C., Mao, W., Dong, X. et al. Hydrogen-assisted dehydrochlorination of 1,1,1,2-tetrafluoro-2-chloropropane to 2,3,3,3-tetrafluoropropene over Pd-Ag/nano-MgF2 with optimized Pd isolated sites. Commun Chem 9, 93 (2026). https://doi.org/10.1038/s42004-026-01896-w
Palavras-chave: refrigerantes, catálise, paládio-prata, gases de efeito estufa, hidrofluoroalfenos