Clear Sky Science · pt
Crescimento controlado de cristais esferulíticos a partir de misturas de sal
Por que cristais de sal podem parecer flores
A maioria de nós pensa em cristais como formas nítidas e facetadas, mas na natureza eles frequentemente crescem em esferas espetaculares que lembram flores ou bolas de neve. Esses “esferulitos” aparecem em rochas vulcânicas, cálculos renais e até em algumas doenças ligadas a proteínas mal dobradas. Este artigo explora como um mineral comum, o sulfato de sódio — o mesmo sal encontrado em detergentes e alguns materiais de construção — pode ser induzido a formar cristais esféricos tão intrincados, e o que isso revela sobre como estruturas complexas se auto-organizam a partir de ingredientes simples.
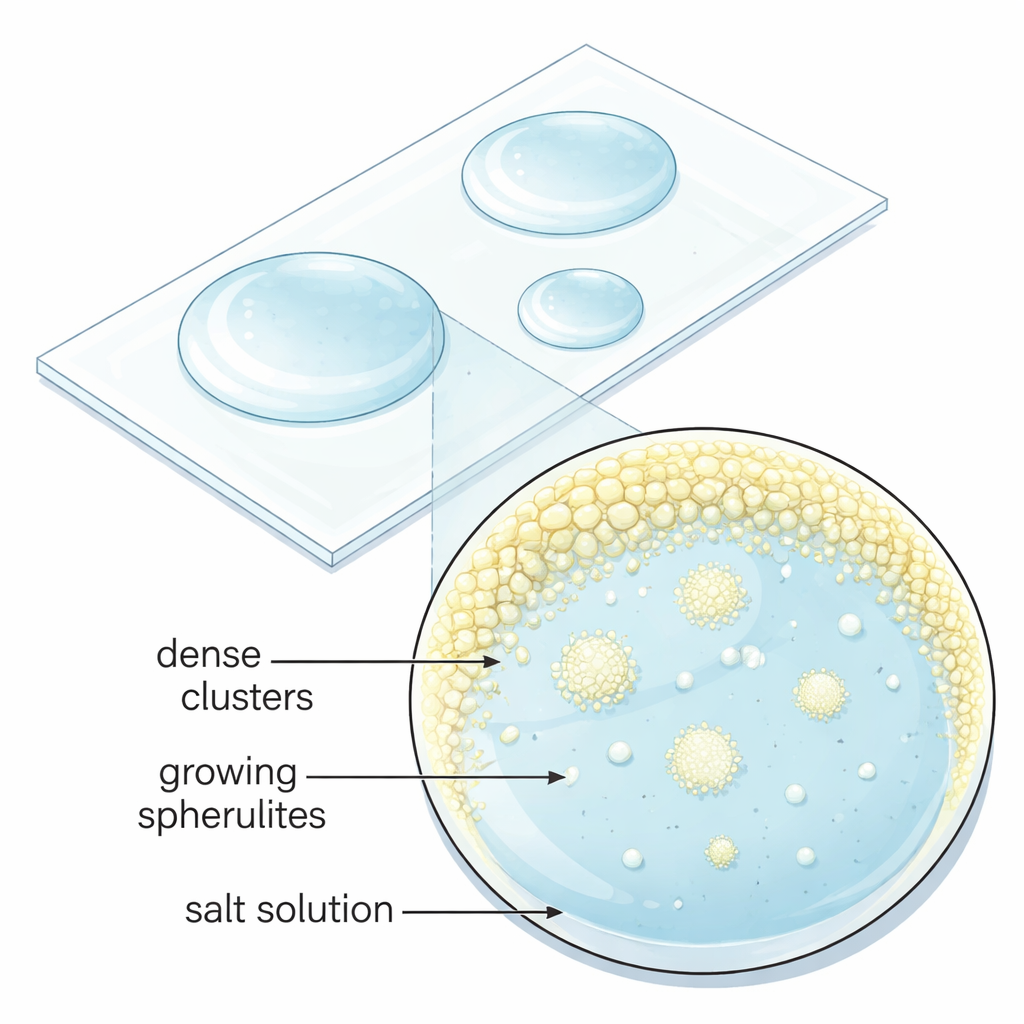
De sais simples a esferas esculpidas
Os pesquisadores buscaram entender quando e como o sulfato de sódio cresce em esferulitos em vez de cristais blocosos comuns. Prepararam gotículas minúsculas de água contendo misturas de sulfato de sódio e outros sulfatos cujos íons metálicos têm carga dupla positiva, como magnésio ou ferro. À medida que essas gotículas, de picolitro a microlitro, evaporavam lentamente sobre lâminas de vidro à temperatura ambiente, os sais dissolvidos se concentravam cada vez mais até o início da cristalização. Variando sistematicamente a proporção de mistura, encontraram “pontos ótimos” de composição onde o sulfato de sódio produzia de forma consistente cristais esféricos com textura radial. Fora dessas faixas, a mesma solução gerava grãos facetados regulares ou um sólido amorfo semelhante a gel, mostrando que as formas esféricas exigem condições cuidadosamente ajustadas.
Pequenos bolsões líquidos que semeiam as esferas cristalinas
Ao microscópio, a equipe observou que os esferulitos não surgiam diretamente de uma solução límpida. Em vez disso, a evaporação primeiro criou pequenos aglomerados líquidos densos enriquecidos em íons dissolvidos perto da borda da gota. Esses bolsões de tamanho micrométrico perduravam por minutos antes de, de repente, darem origem a muitos esferulitos de uma só vez. Imagens de alta resolução por microscopia eletrônica das estruturas secas revelaram que cada esferulito é formado por inúmeros cristais de sulfato de sódio em escala nanométrica apontando aproximadamente para fora, que depois se fundem. Esse comportamento contradiz a imagem clássica do crescimento cristalino, em que um único núcleo estável cresce de forma contínua, e aponta para uma via em vários passos — “não clássica” — na qual gotas densas e nanopartículas se montam e se reorganizam até atingir a forma sólida final.
Quando água salgada fica com consistência de manteiga de amendoim
Uma parte crucial da história é o quão espessa, ou viscosa, a solução fica à medida que a água se perde. Ao monitorar a velocidade de expansão dos esferulitos e medindo diretamente as propriedades de fluxo de soluções salinas relacionadas, os autores mostraram que soluções mistas de sódio–magnésio ou sódio–ferro se tornam extraordinariamente viscosas — até cerca de 100 vezes mais espessas que mel — justamente quando os esferulitos começam a se formar. Essa consistência quase de “manteiga de amendoim” desacelera tanto o movimento dos íons que a difusão, e não a química de superfície, limita a velocidade de crescimento cristalino. Nesse ambiente lento, inúmeros pequenos aglomerados e nanocristais se formam e têm tempo para se ligar em agregados esféricos em vez de crescerem em poucos cristais grandes e bem moldados. Os íons metálicos divalentes são decisivos: eles prendem fortemente a água e se ligam em cadeias ou redes curtas, o que tanto aumenta a viscosidade quanto ajuda a gerar um fundo amorfo, tipo gel, ao redor dos esferulitos em crescimento.
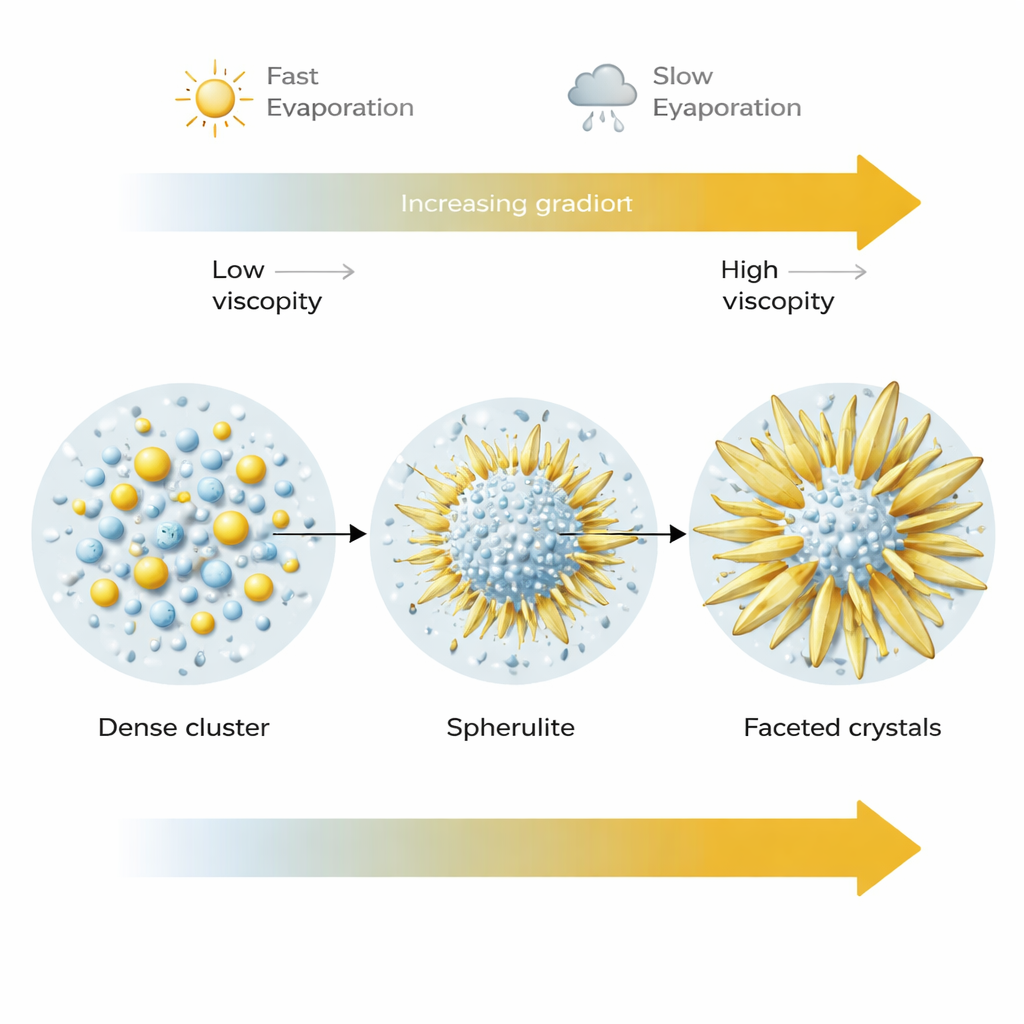
Como a velocidade de secagem remodela os cristais finais
A taxa de evaporação revelou-se outro controle poderoso. Em secagem mais rápida (umidade mais baixa), muitos esferulitos nucleavam mas permaneciam relativamente pequenos, presos em sua forma esférica metaestável à medida que o fluido circundante engrossava rapidamente. Em secagem mais lenta (umidade mais alta), as mesmas esferas iniciais tiveram mais tempo e acesso a íons dissolvidos. Seus minúsculos blocos estruturais puderam se rearranjar e fundir-se em cristais maiores, mais lisos e mais facetados, frequentemente produzindo saliências em forma de lâmina que acabavam convertendo-se na forma termodinamicamente estável do sulfato de sódio. Em outras palavras, as estruturas esféricas atuam como um estágio transitório em uma jornada de crescimento que pode terminar em formas muito diferentes, dependendo de quão rápido a solução seca e de quão facilmente o material ainda pode se mover através dela.
Por que isso importa além de cristais bonitos
Em termos simples, o estudo mostra que esferas salgadas bonitas e com aparência de flor surgem quando misturas concentradas de sais simples se tornam suficientemente espessas para desacelerar tudo, mas não tão espessas a ponto de interromper totalmente o crescimento. Nestas condições “no ponto certo”, bolsões líquidos densos e enxames de pequenos cristais se auto-organizam em agregados esféricos que podem posteriormente evoluir para grãos facetados mais estáveis. Compreender e controlar esse equilíbrio delicado entre composição, viscosidade e evaporação abre caminho para projetar texturas cristalinas sob medida para aplicações que vão desde materiais de construção mais resistentes e fármacos aprimorados até melhores modelos da formação de cristais em contextos geológicos e biológicos.
Citação: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Palavras-chave: esferulitos, sulfato de sódio, crescimento cristalino, nucleação não clássica, soluções salinas