Clear Sky Science · pt
Primeira estrutura cristalina de um aduto formado pela reação de um composto de vanádio com a transferrina sérica humana
Por que uma proteína sanguínea e um fármaco metálico importam
Muitos fármacos experimentais contêm átomos metálicos que podem ajudar a tratar doenças que vão do diabetes ao câncer. Mas, uma vez que essas medicinas à base de metal entram na corrente sanguínea, elas precisam se apoiar nas proteínas transportadoras naturais do corpo. Este estudo investiga como uma dessas proteínas, a transferrina sérica humana — o principal transportador de ferro no nosso sangue — interage com um promissor composto de vanádio, esclarecendo como fármacos metálicos são transportados pelo organismo e como eles podem ser ajustados para terapias mais seguras e eficazes.
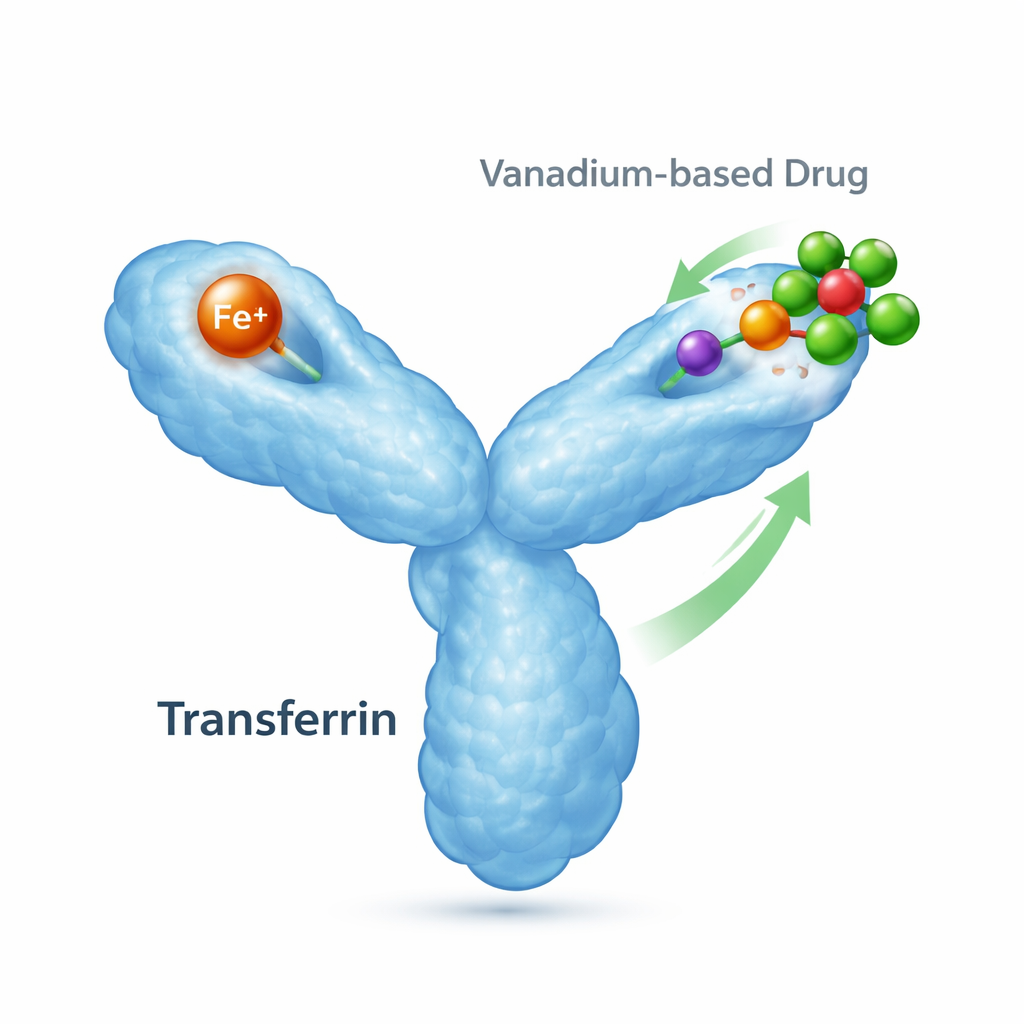
O mensageiro do ferro no corpo e suas funções secundárias
A transferrina é uma proteína de 80 quilodaltons cuja função principal é capturar ferro e entregá‑lo às células que dele necessitam. Possui dois “lóbulos”, cada um capaz de ligar um íon de ferro, e muda de conformação conforme o ferro está presente ou não. Quando o ferro se liga, o lóbulo se fecha; sem ferro, permanece aberto. Receptores especializados na superfície celular reconhecem essas formas com ferro e as internalizam, tornando a transferrina central para o equilíbrio do ferro e a saúde celular. No entanto, a transferrina também pode ligar outros metais, inclusive os usados em tratamentos médicos, o que significa que ela pode influenciar para onde fármacos metálicos viajam e como atuam.
Um retrato conformacional do vanádio na transferrina
Os pesquisadores focaram num candidato a fármaco de vanádio bem estudado chamado bis(acetilacetonato)oxovanádio(IV), frequentemente escrito como [VIVO(acac)₂]. Trabalhos anteriores mostraram que esse composto, ou espécies derivadas dele em água, pode se ligar à transferrina, mas ninguém tinha visto exatamente como. Usando cristalografia de raios X, a equipe obteve estruturas de alta resolução da transferrina que carrega ferro apenas em seu lóbulo C‑terminal (a forma “FeC”), tanto antes quanto depois da exposição ao composto de vanádio. Nos cristais tratados com vanádio, observaram não o fármaco original, mas um fragmento transformado de vanádio‑oxigênio ligado no lóbulo N desprovido de ferro. Isso forneceu a primeira imagem estrutural direta de um fragmento de vanádio ligado à transferrina humana.
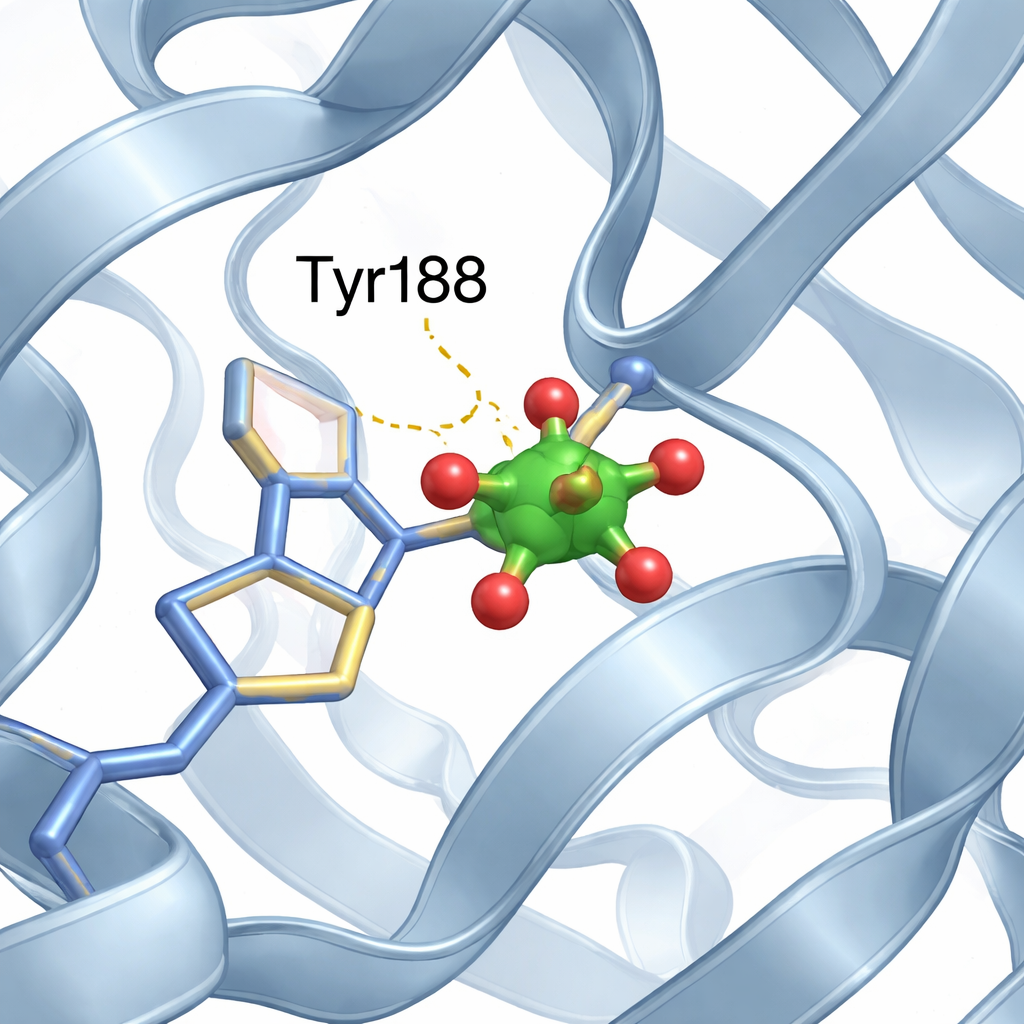
Um minúsculo aglomerado de vanádio encontra seu lugar
No sítio do ferro do lóbulo N, a equipe identificou um pequeno aglomerado composto por dois átomos de vanádio e átomos de oxigênio, melhor descrito como uma unidade modificada de “divanadato”. Uma das posições de oxigênio do aglomerado é ocupada pelo oxigênio de um aminoácido específico, a tirosina 188 (Tyr188), formando uma ligação direta entre a proteína e o aglomerado metálico. Interações adicionais mais sutis, como ligações de hidrogênio de segmentos proteicos próximos, estabilizam ainda mais o aglomerado no lugar. Importante notar que, apesar desse novo hóspede metálico ocupar um bolso de ligação ao ferro, a proteína mantém a disposição usual de lóbulo N aberto e lóbulo C fechado, quase idêntica à estrutura sem vanádio.
Como a transferrina remodela a química do vanádio
Em solução, nas condições de pH e concentração usadas para cristalização, a espécie de dois vanádios observada no cristal normalmente é apenas um componente minoritário; aglomerados maiores de vanádio‑oxigênio tendem a dominar. Medições espectroscópicas e cálculos teóricos de especiação sugerem que o fármaco original de vanádio se oxida e se degrada lentamente em água, produzindo íons vanadato simples que então se associam em vários aglomerados. A estrutura cristalina indica que a transferrina estabiliza seletivamente esse pequeno fragmento do tipo divanadato em relação aos aglomerados maiores, essencialmente “escolhendo” uma forma química de uma mistura complexa em solução ao fornecer um sítio de ligação acolhedor em Tyr188 e uma rede de ligações de hidrogênio de apoio.
Mantendo o aperto de mão com o receptor celular
Como a transferrina precisa unir‑se a um receptor na superfície celular para entregar ferro, os pesquisadores questionaram se a fixação desse aglomerado de vanádio poderia perturbar esse aperto de mão crucial. Usando eletroforese em gel não desnaturante e uma técnica sensível chamada interferometria de biocamada, mediram quão bem a transferrina tratada com vanádio ligava‑se ao receptor de transferrina em comparação com a forma não tratada, contendo apenas ferro. Ambas se comportaram quase identicamente, com ligação muito forte na faixa de nanomolar baixa. Isso confirma que o aglomerado de vanádio, embora alojado no lóbulo N, não altera significativamente a conformação da transferrina na região de interação com o receptor e, portanto, não deve impedir o reconhecimento da proteína pelas células.
O que isso significa para medicamentos à base de metais
Para leigos, a conclusão é que este estudo fornece um retrato molecular de como um derivado de fármaco de vanádio se fixa ao principal transportador de ferro do corpo sem atrapalhar sua função normal. A transferrina pode capturar um aglomerado específico e pequeno de vanádio‑oxigênio em um sítio de ferro, mas a conformação global da proteína e sua capacidade de ligar o receptor permanecem essencialmente inalteradas. Isso ajuda a explicar como fármacos de vanádio podem circular ligados à transferrina e ressalta que proteínas diferentes podem favorecer tamanhos distintos de aglomerados de vanádio. Esses insights são fundamentais para projetar terapias à base de metais mais inteligentes, cujo comportamento na corrente sanguínea — que formas adotam, para onde vão e quanto tempo duram — possa ser previsto e controlado.
Citação: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Palavras-chave: fármacos de vanádio, transferrina sérica humana, terapêuticos à base de metais, ligação proteína–metal, biologia estrutural