Clear Sky Science · pt
Lactama possibilita rearranjos remotos de boronato para ligações C═N
Um novo atalho para construir moléculas com perfil de fármaco
Químicos estão sempre em busca de formas mais rápidas e limpas de montar as moléculas complexas presentes em medicamentos e materiais avançados. Este estudo apresenta um atalho engenhoso que permite que uma estrutura comum em forma de anel, chamada lactama, oriente temporariamente uma reação e depois se retire discretamente — possibilitando transformar ingredientes simples e prontamente disponíveis em blocos de construção valiosos para a indústria farmacêutica sem recorrer a metais caros ou etapas de preparo elaboradas.
Transformando um ajudante discreto em um guia temporário
Muitos fármacos modernos e materiais funcionais dependem de reações de ácidos borônicos, uma família de compostos contendo boro valorizada por sua confiabilidade e comportamento suave. Tradicionalmente, para induzir os ácidos borônicos a formar novas ligações com ligações duplas carbono‑nitrogênio (C=N), os químicos precisam pré-instalar “grupos direcionadores” especiais nos reagentes. Esses grupos atuam como alças que guiam a reação, mas acrescentam tempo, custo e etapas — e frequentemente funcionam apenas com parceiros muito reativos. Os autores perceberam que lactamas, parentes em anel da conhecida ligação amida encontrada em proteínas, poderiam servir como guias embutidos e temporários. Ao coordenar com o átomo de boro, o oxigênio da lactama ajuda a formar um centro de boro altamente organizado e tetracoordenado que pode deslocar um fragmento ligado para uma posição distante ao longo da molécula, preparando a formação de novas ligações C–N sem qualquer grupo direcionador permanente.
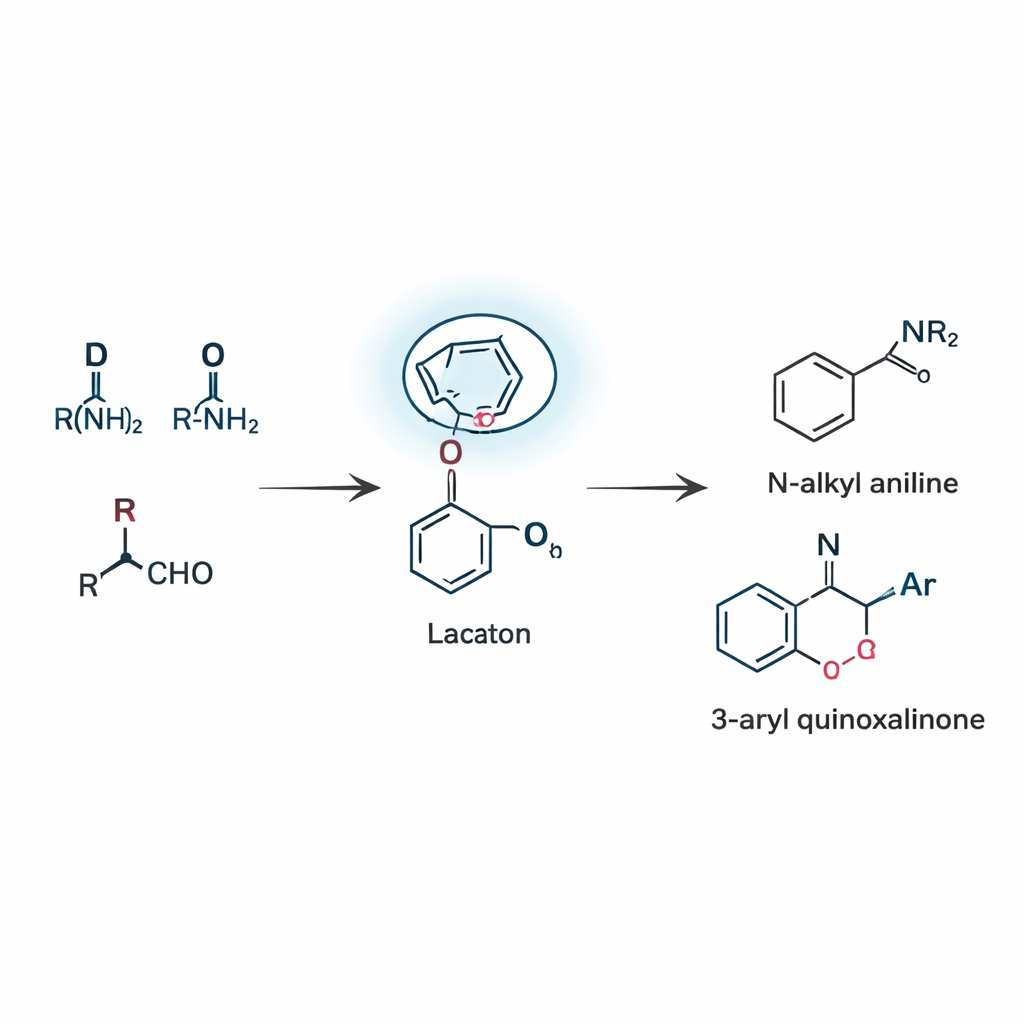
Construindo duas famílias de produtos úteis numa mesma estratégia
Com esse conceito, a equipe desenvolveu duas reações relacionadas que dependem desse rearranjo guiado pela lactama, conhecido como rearranjo remoto de boronato. Na primeira, três peças simples — um aldeído, uma amina e um ácido borônico — se juntam para formar anilinas N‑alquiladas, um motivo central presente em inúmeros candidatos a fármacos e corantes. A reação segue por um raro deslocamento 1,5, no qual um grupo arila no boro salta cinco átomos para alcançar a ligação C=N. Ao ajustar cuidadosamente o catalisador, o solvente e a temperatura, os pesquisadores obtiveram rendimentos respeitáveis e mostraram que muitos substituintes diferentes, incluindo halogênios, grupos alquila e heterociclos, são tolerados. No segundo modo reacional, a mesma ideia guia é aplicada a quinoxalinonas, uma classe de anéis ricos em nitrogênio comuns na química medicinal. Aqui, a reação não usa nenhum catalisador metálico adicionado e ainda fornece 3‑aril quinoxalinonas com eficiência, graças à capacidade da lactama de interagir com o boro e estabilizar o intermediário chave.
Condições verdes e edição em estágio tardio de fármacos
Além de demonstrar amplo escopo, os autores mostram que essa estratégia é prática para moléculas do mundo real. Como o rearranjo 1,4 nas quinoxalinonas ocorre em condições sem metal em um solvente alcoólico especializado, evita-se a necessidade de metais de transição caros ou tóxicos. A equipe aplicou o método a fragmentos complexos derivados de medicamentos comercializados, como ibuprofeno, e outros fármacos que contêm o arcabouço de quinoxalinona. Em cada caso, a reação introduziu novos grupos arila em uma posição específica sem perturbar outras funções sensíveis. Esse tipo de “funcionalização em estágio tardio” permite que químicos decorem rapidamente núcleos de fármacos existentes com novas cadeias laterais, acelerando a busca por maior potência, segurança ou propriedades físicas aprimoradas.
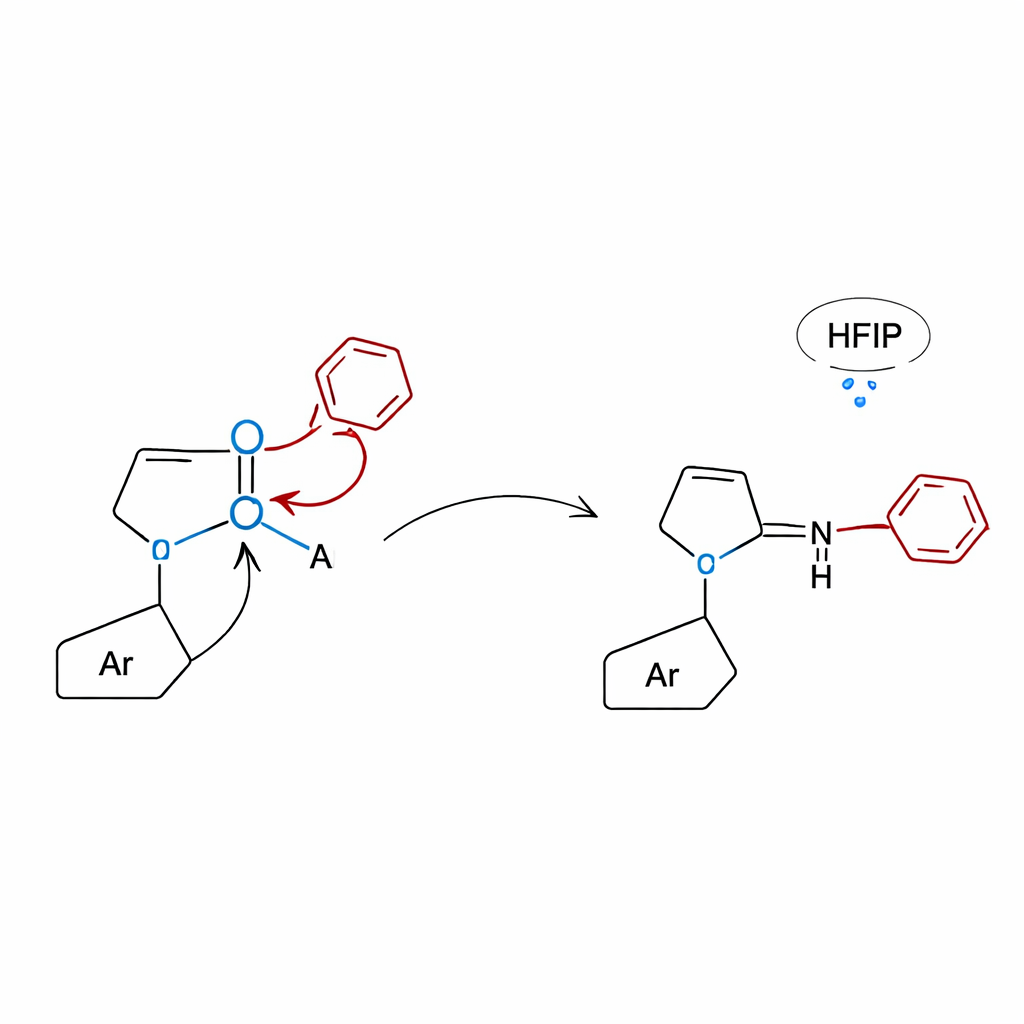
Vendo por trás das cortinas com teoria e testes de controle
Para entender por que a abordagem com lactama funciona tão bem, os pesquisadores combinaram experimentos de controle cuidadosamente projetados com simulações em computador. Quando moléculas sem a unidade de lactama foram testadas, as reações essencialmente cessaram, confirmando que o anel de lactama é essencial para ativar o ácido borônico e direcionar o rearranjo. Cálculos quântico‑químicos revelaram que o oxigênio da lactama se liga ao boro para formar uma estrutura compacta e tetracoordenada da qual o grupo arila pode migrar ou sobre cinco átomos (deslocamento 1,5) para dar anilinas N‑alquiladas, ou sobre quatro átomos (deslocamento 1,4) para dar 3‑aril quinoxalinonas. No caso das quinoxalinonas, a rede de ligações de hidrogênio fornecida pelo solvente HFIP reduz ainda mais a barreira energética, ajudando a reação a ocorrer sob condições térmicas relativamente brandas sem qualquer catalisador adicionado.
Por que isso importa para futuros medicamentos
No geral, o trabalho mostra que um anel de lactama simples pode atuar como um guia dinâmico e reciclável que desbloqueia padrões de formação de ligações anteriormente inacessíveis na química de ácidos borônicos. Para não especialistas, a mensagem principal é que os químicos agora dispõem de uma forma mais direta e eficiente de transformar blocos de construção básicos em duas classes importantes de moléculas contendo nitrogênio que sustentam muitos fármacos. Como o método evita metais preciosos, tolera uma grande variedade de grupos funcionais e funciona em estruturas avançadas com perfil de fármaco, ele está bem posicionado para ajudar a simplificar o desenho e a otimização de futuros produtos farmacêuticos e potencialmente novos agroquímicos também.
Citação: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Palavras-chave: ácidos borônicos, química de lactama, formação de ligação C–N, quinoxalinonas, química medicinal