Clear Sky Science · pt
A mutação da síndrome PACS1 interrompe o transporte de carga mediado por dineína via HDAC6 e BICD2
Por que isso importa para o desenvolvimento cerebral
A síndrome PACS1 é uma condição genética rara que causa deficiência intelectual, convulsões e feições faciais características. Famílias e clínicos conhecem os sintomas, mas até recentemente não estava claro o que realmente falhava dentro das células dos pacientes. Este estudo desvenda esse mistério, mostrando como uma alteração de uma única letra no gene PACS1 embaralha o sistema de transporte interno da célula, especialmente nos neurônios, e como isso liga a síndrome PACS1 a uma família mais ampla de doenças de “tráfego” do sistema nervoso. 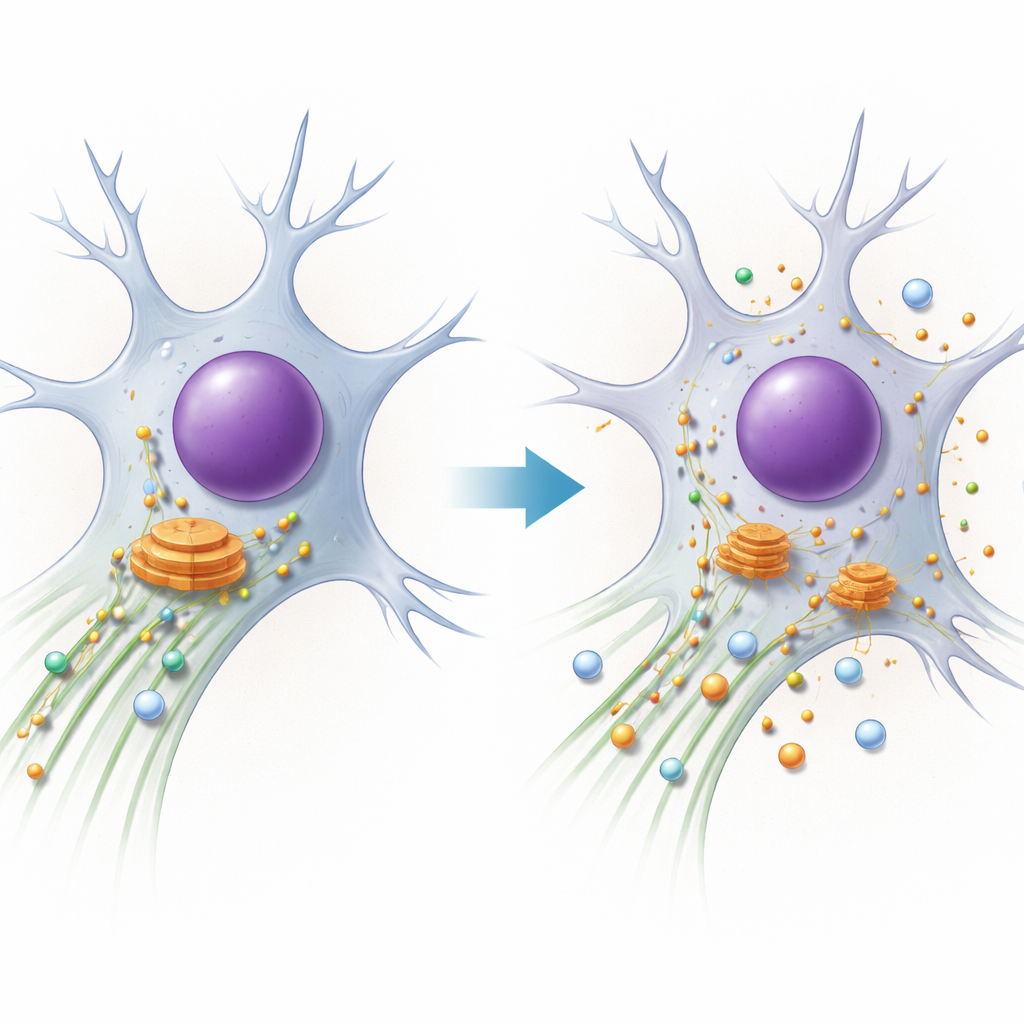
As rodovias de entrega da célula
Toda célula depende de rodovias microscópicas formadas por tubos proteicos chamados microtúbulos. Motores moleculares percorrem essas vias, puxando cargas como enzimas e compartimentos de membrana para onde são necessárias. Um desses motores, a dineína, é responsável pelas “viagens de retorno” de longa distância, puxando cargas da periferia celular de volta em direção ao centro, onde fica uma importante estação de triagem chamada aparelho de Golgi. Os autores se concentram no PACS1, uma proteína que ajuda a selecionar quais cargas utilizam a dineína e também ajusta o estado das vias por meio de outra proteína, a HDAC6, que controla uma marca química (acetilação) nos microtúbulos. Neurônios, com suas extensões muito longas, são especialmente sensíveis até a pequenos defeitos nesse sistema.
Um coordenador mutante que se agarra com força excessiva
A síndrome PACS1 é causada pela mutação recorrente R203W no PACS1. A equipe encontrou que tanto o PACS1 normal quanto o mutante se ligam fisicamente à cadeia pesada da dineína, mas a forma mutante se prende com mais força. Usando células da pele de pacientes e linhagens celulares modificadas, eles mostraram que esse envolvimento excessivo produz o mesmo desfecho que uma perda parcial da função da dineína: o Golgi se desagrega em mini‑pilhas dispersas, e uma enzima importante chamada furina, normalmente localizada no lado trans do Golgi, é mal direcionada para outros compartimentos. Ao dissecar a estrutura do PACS1, localizaram uma pequena “faixa” de beta‑foja que faz contato específico com a dineína. Quando alteraram essa faixa sem perturbar outras funções do PACS1, a furina voltou a perder seu endereço adequado, confirmando que o aperto entre dineína e PACS1 é crucial para a colocação correta das cargas. 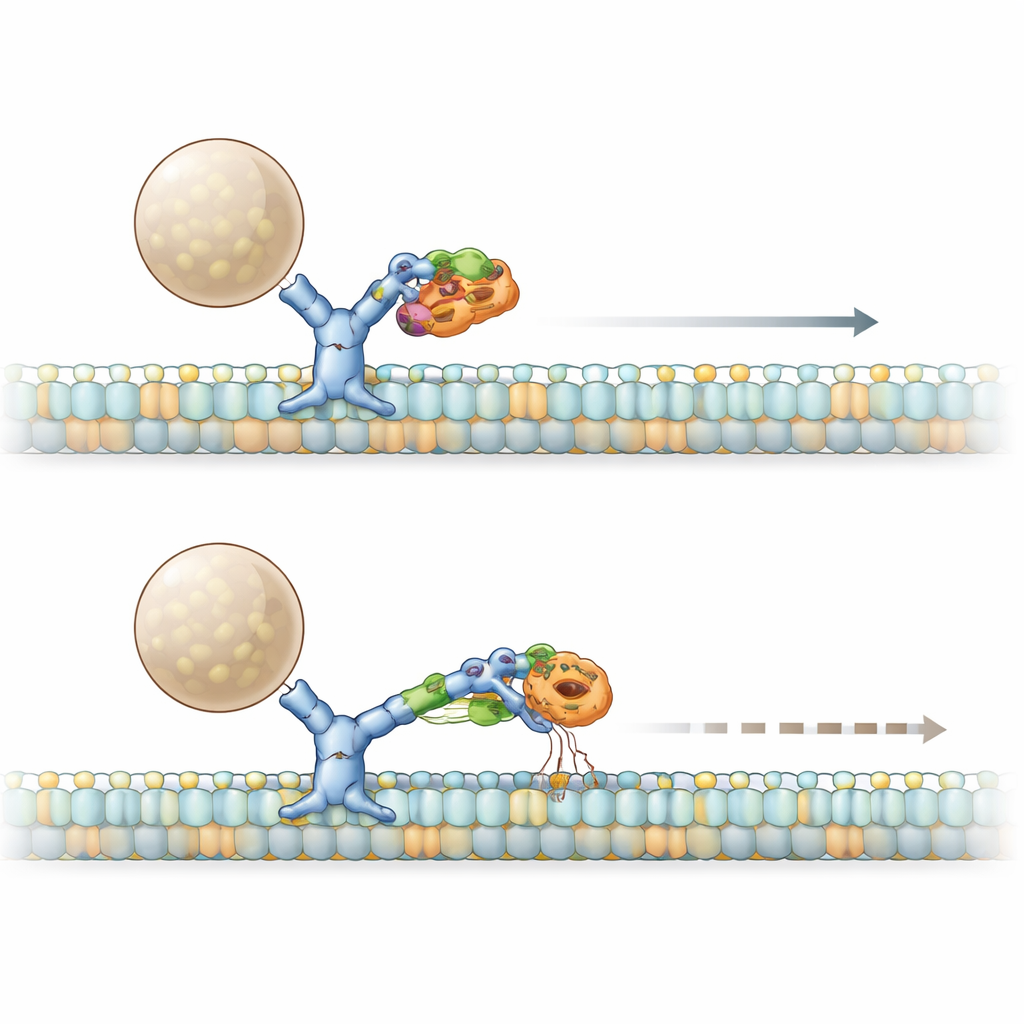
Como uma aliança de três proteínas emperra o motor
A história se aprofunda com dois protagonistas adicionais: a HDAC6 e um adaptador chamado BICD2, que ajuda a montar complexos ativos de dineína. O PACS1 mutante não apenas aumenta a atividade da HDAC6, reduzindo a acetilação dos microtúbulos, como também forma um complexo ampliado com HDAC6 e BICD2. Testes bioquímicos revelaram que, juntos, o PACS1 mutante e a HDAC6 afastam o BICD2 da dineína enquanto deixam intacta sua parceria com um motor que se dirige para a frente (cinesina). Em células vivas, uma carga artificial que normalmente percorre rapidamente via dineína desacelerou e menos cargas se moveram quando o PACS1 mutante estava presente. Bloquear a atividade da HDAC6 restaurou tanto a velocidade quanto o número de partículas em movimento, mostrando que o complexo PACS1 mutante–HDAC6–BICD2 age como um freio na capacidade da dineína de iniciar e sustentar o transporte.
Resgatando o tráfego com um ajudante natural da dineína
Os pesquisadores então testaram se a dineína poderia ser “reativada” apesar do complexo mutante. Eles recorreram à Lis1, um conhecido auxiliar da dineína que estabiliza os montagens ativas do motor. Nas células de pacientes, os níveis de Lis1 estavam um pouco reduzidos. Quando a equipe adicionou Lis1 em excesso, duas coisas melhoraram: o Golgi voltou a se reagrupar próximo ao centro celular, e os lisossomos, outra classe de organelas que haviam migrado para a periferia, retornaram ao lugar. No mesmo ensaio de motilidade, a Lis1 aumentou tanto a frequência quanto a velocidade do movimento de cargas movidas pela dineína na presença do PACS1 mutante. Esses resultados mostram que o problema não é ausência de dineína, mas sim que ela fica presa em um estado pouco ativo — um estado que pode ser parcialmente corrigido quer por reduzir a atividade da HDAC6 quer por reforçar a ativação da dineína.
Ligando uma síndrome rara a um conjunto mais amplo de distúrbios
Ao combinar análise estrutural, biologia celular e imagem em células vivas, os autores propõem um modelo claro: o PACS1 normalmente conecta cargas selecionadas à dineína e ajusta o desempenho do motor por meio da HDAC6 e da acetilação dos microtúbulos. A mutação R203W expõe a superfície de interação do PACS1, recrutando em excesso a HDAC6 e o BICD2 para um complexo que prejudica a capacidade da dineína de agarrar microtúbulos e mover‑se com eficiência. O resultado é o posicionamento incorreto generalizado do Golgi, lisossomos e outras cargas, particularmente em neurônios onde o transporte de longa distância é vital. Esse mecanismo ajuda a explicar por que a redução de PACS1 ou HDAC6 com terapias antisense corrige defeitos cerebrais em modelos de camundongo e está agora sendo explorada em pacientes. Mais amplamente, isso insere a síndrome PACS1 no espectro crescente de desordens de trafegamento por microtúbulos, ao lado de condições causadas por mutações em dineína, BICD2 e fatores de transporte relacionados.
Citação: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Palavras-chave: síndrome PACS1, transporte por dineína, trafegamento por microtúbulos, organização do Golgi, desenvolvimento neuronal