Clear Sky Science · pt
O sistema de secreção tipo VI de Acinetobacter: mecanismos, biologia e potencial terapêutico
Armas ocultas nos germes hospitalares
Muita gente sabe que alguns germes hospitalares resistem a antibióticos, mas menos pessoas percebem que esses micróbios também travam batalhas violentas entre si. Esta revisão examina uma “lança acionada por mola” microscópica dentro de Acinetobacter, um grupo de bactérias que inclui o notório patógeno hospitalar Acinetobacter baumannii. Entender como essa arma embutida funciona, quando é ativada e como ajuda as infecções a se estabelecerem pode abrir novos caminhos para diagnosticar e desarmar infecções resistentes a medicamentos e potencialmente letais.
Uma máquina de sobrevivência, não apenas um dardo venenoso
Espécies de Acinetobacter vivem no solo, na água e sobre nossa pele, mas algumas se tornaram patógenos hospitalares altamente bem‑sucedidos. Uma ferramenta-chave em seu conjunto é o sistema de secreção tipo VI, ou T6SS, uma minúscula máquina contrátil ancorada no envelope celular. Quando acionada, dispara uma ponta semelhante a uma agulha carregada com proteínas tóxicas em células vizinhas, frequentemente matando bactérias concorrentes por contato. Ao contrário de alguns outros micróbios que carregam várias versões desse sistema, Acinetobacter patogênico geralmente possui apenas um T6SS, mas reconfigurou essa plataforma única para servir a vários propósitos, desde afastar rivais até moldar infecções.
Hardware reconstruído: uma plataforma de lançamento incomum
A maioria das bactérias monta seu T6SS em torno de um conjunto padrão de peças, mas Acinetobacter remodelou várias peças-chave. Falta-lhe um âncora comum na membrana externa chamada TssJ e, em vez disso, conta com um trio de auxiliares especializados: TsmK forma uma base na membrana interna, TslA estabiliza uma longa proteína “túnel” (TssM) enquanto ela atravessa a parede celular, e TagX corta localmente a parede para abrir caminho para a arma. Além disso, uma proteína de ponta particular, VgrG1, precisa ter uma conformação quase perfeita para que o sistema dispare — mudanças de um único aminoácido podem torná‑la ineficaz. Juntas, essas adaptações mostram como a evolução pode substituir peças ausentes por novas soluções, preservando o princípio básico de disparo.
Controles inteligentes: quando o modo ataque faz sentido
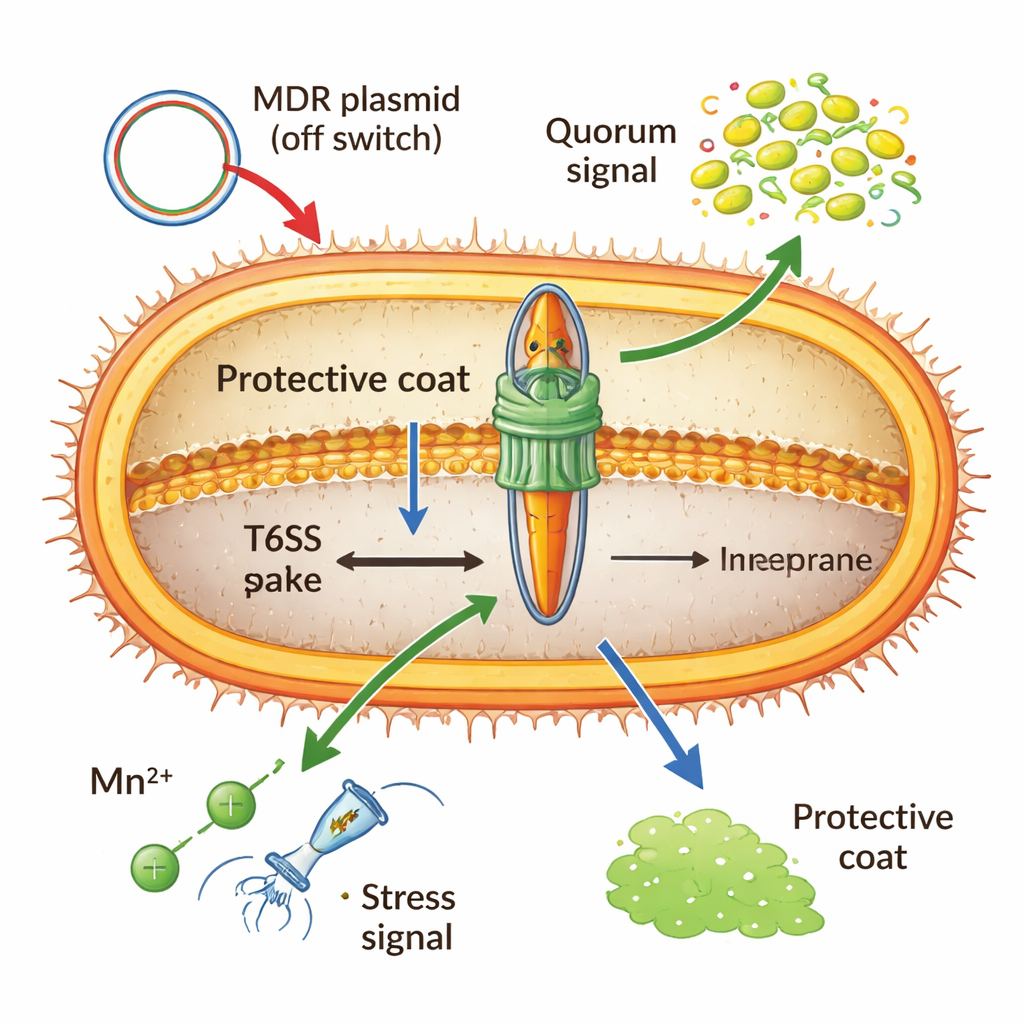
Construir e disparar essa nanomáquina é caro, então Acinetobacter a mantém sob rigoroso controle. Uma proteína global de ligação ao DNA (H‑NS) e repressores especiais carregados em plasmídeos multirresistentes podem travar o sistema na posição “desligado”, especialmente quando genes de resistência estão sendo compartilhados entre células. Em alta densidade celular, sinais químicos de “quorum” podem ligá‑lo, preparando as bactérias para competição em espaço reduzido. Íons metálicos também desempenham um papel: sob estresse oxidativo, manganês importado ativa um pequeno RNA que faz com que mensagens-chave do T6SS sejam destruídas, reduzindo a arma para favorecer a sobrevivência dentro do hospedeiro. Até a cápsula — um revestimento externo açucarado — atua tanto como escudo quanto como freio, bloqueando ataques vindos de fora, mas também amortecendo fisicamente o próprio disparo do Acinetobacter.
Um kit diversificado de golpes microscópicos
Quando Acinetobacter realmente puxa o gatilho, pode entregar uma ampla gama de toxinas. Algumas enzimas corroem a resistente parede celular dos rivais; outras degradam silenciosamente membranas celulares, e outras ainda cortam o DNA dentro das células‑alvo. Cada toxina vem associada a uma proteína “imunidade” correspondente que protege o atacante de fogo amigo. Uma toxina que corta DNA, agora chamada TafE, pode até matar fungos, sugerindo escaramuças entre reinos em locais como intestino ou pulmões. Estudos genômicos indicam que Acinetobacter codifica muitas outras toxinas ainda não caracterizadas, frequentemente agrupadas em grandes proteínas Rhs que atuam como transportadoras modulares. Em vez de depender de um único golpe, essas bactérias parecem usar ataques em camadas que danificam várias estruturas essenciais ao mesmo tempo.
Moldando infecções, genes e tratamentos futuros
Evidências de isolados de pacientes e modelos animais sugerem que um T6SS ativo frequentemente anda de mãos dadas com doença mais grave, inflamação mais intensa e maior sobrevivência das bactérias dentro dos hospedeiros. Ao matar micróbios vizinhos, o sistema também libera DNA que células de Acinetobacter naturalmente competentes podem absorver, acelerando a disseminação de características como resistência a antibióticos. Ainda assim, manter a arma constantemente ativa é oneroso, de modo que muitas cepas hospitalares bem‑sucedidas carregam plasmídeos ou mutações que a silenciam uma vez que a resistência está assegurada. Em geral, os autores defendem que esse sistema de secreção deve ser visto não como um simples fator de virulência, mas como um “módulo de aptidão” flexível que Acinetobacter ajusta para equilibrar agressão, persistência e consumo de energia. Essa nova visão aponta para aplicações práticas, desde vacinas que visem partes conservadas do T6SS até drogas que travem seletivamente o mecanismo de disparo, ajudando médicos a superar um inimigo hospitalar perigoso e adaptável.
Citação: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Palavras-chave: Acinetobacter, sistema de secreção tipo VI, resistência a antibióticos, competição bacteriana, infecções hospitalares