Clear Sky Science · pt
Glicosilação como reguladora dinâmica das vias de sinalização imune inata RLR e cGAS-STING
Como etiquetas de açúcar ajudam as células a detectar vírus
Nossas células estão constantemente em alerta contra vírus invasores, e grande parte dessa defesa depende de pequenas etiquetas de açúcar anexadas a proteínas. Esta revisão explica como essas etiquetas de açúcar, conhecidas como glicosilação, atuam mais como controles de intensidade do que como simples botões liga/desliga em vias antivirais essenciais. Entender esse ajuste fino baseado em açúcares pode abrir novas formas de potencializar vacinas, tratar infecções virais e até explorar o sistema imunológico contra o câncer.
O alarme precoce da célula
Quando vírus entram numa célula, deixam rastros característicos de RNA ou DNA. Sistemas especializados de “alarme” patrulham o interior celular em busca desses detritos genéticos. Um sistema, chamado via dos receptores do tipo RIG-I (RLR), detecta RNA viral. Outro, conhecido como via cGAS–STING, percebe DNA que aparece no lugar errado dentro da célula. Uma vez ativadas, ambas as vias disparam cascatas químicas que terminam na liberação de interferons do tipo I e moléculas inflamatórias — sinais potentes que avisam células vizinhas e mobilizam defesas imunológicas. Como uma resposta excessiva ou insuficiente pode ser perigosa, a célula precisa afinar cuidadosamente esses alarmes, e a glicosilação é uma das maneiras principais de fazê-lo. 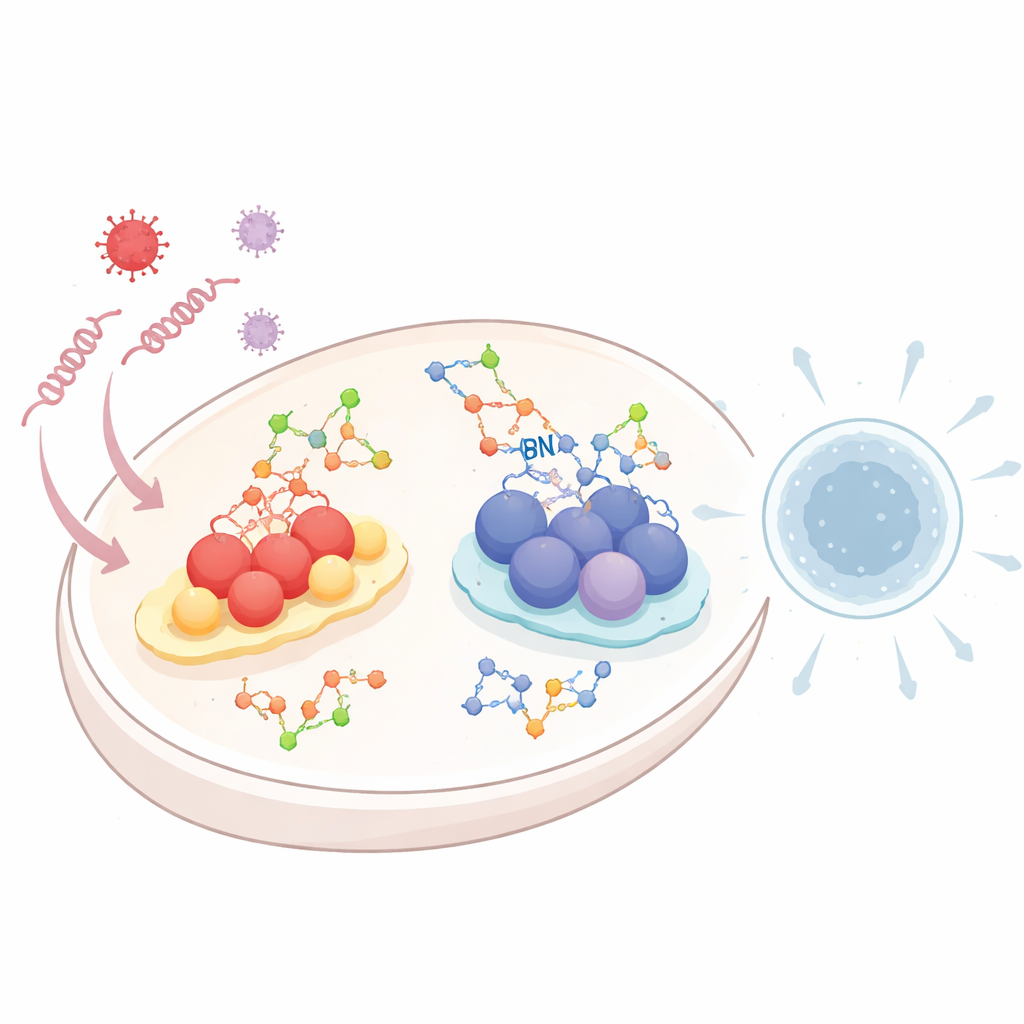
Revestimentos açucarados como controles de precisão
A glicosilação adiciona pequenas unidades de açúcar a proteínas em diferentes locais celulares. Na rede interna de transporte da célula, o retículo endoplasmático e o Golgi, cadeias N-ligadas volumosas ajudam proteínas a se dobrarem corretamente, manterem-se estáveis e irem para a membrana correta. Em contraste, uma forma mais enxuta chamada O-GlcNAcilação coloca um único açúcar em proteínas no citoplasma e no núcleo. Essa etiqueta minimalista é altamente dinâmica, renovando-se rapidamente conforme duas enzimas a adicionam ou removem em resposta a níveis de nutrientes e estresse. A revisão descreve como esses diferentes tipos de açúcar não simplesmente ligam ou desligam os sensores imunológicos; em vez disso, ajustam com que facilidade os sensores se agregam, quanto tempo persistem e quão forte sinalizam. Dessa forma, a glicosilação liga o estado metabólico da célula diretamente à sua prontidão para combater infecções.
Afinando a via sensor de RNA
No sistema RLR que detecta RNA, uma proteína de retransmissão central chamada MAVS fica nas mitocôndrias e atua como um polo chave. A revisão mostra que a O-GlcNAcilação em MAVS pode tanto acelerar quanto frear a sinalização antiviral, dependendo de onde o açúcar é anexado. Etiquetas de açúcar em certos sítios promovem decorações proteicas adicionais, como um tipo específico de cadeia de ubiquitina, que ajudam MAVS a formar grandes aglomerados de sinalização e a impulsionar forte produção de interferon contra vírus de RNA. Outros sítios açucarados mantêm MAVS disperso e inativo em condições normais, evitando inflamação desnecessária. Infecção viral e alterações na via metabólica que produz açúcares podem deslocar o equilíbrio entre essas etiquetas ativadoras e inibidoras. Modificações relacionadas em outro fator, IRF5, podem empurrar o sistema imunológico em direção a “tempestades de citocinas” prejudiciais, evidenciando que mais açúcar nem sempre é melhor. Paralelamente, vírus podem explorar açúcares N-ligados em proteínas de superfície celular como o receptor do fator de crescimento EGFR para marcar sensores a montante, como RIG-I, para degradação, enfraquecendo as defesas antivirais.
Afinando a via sensor de DNA
A via cGAS–STING que detecta DNA também é fortemente modulada pela glicosilação. STING, uma proteína de membrana no retículo endoplasmático, precisa de cadeias N-ligadas para dobrar corretamente, permanecer estável e se montar em aglomerados de sinalização uma vez ativada por mensageiros derivados de DNA. Sem esses açúcares, STING não consegue formar as estruturas de ordem superior nem trafegar pelos compartimentos celulares necessários para uma liberação robusta de interferon. Ao mesmo tempo, a O-GlcNAcilação de STING em um sítio particular aumenta um conjunto diferente de marcas químicas que promovem seu agrupamento e movimentação, ampliando sinais antivirais contra vírus de DNA. Cadeias açucaradas chamadas glicosaminoglicanos sulfatos, construídas no Golgi, auxiliam ainda mais ao ajudar STING ativado a polimerizar em estruturas longas que recrutam enzimas a jusante. Vírus contra-atacam alterando suas próprias glicoproteínas ou desencadeando vias de degradação que miram STING, muitas vezes nos mesmos espaços celulares onde essas decorações de açúcar são adicionadas ou processadas. 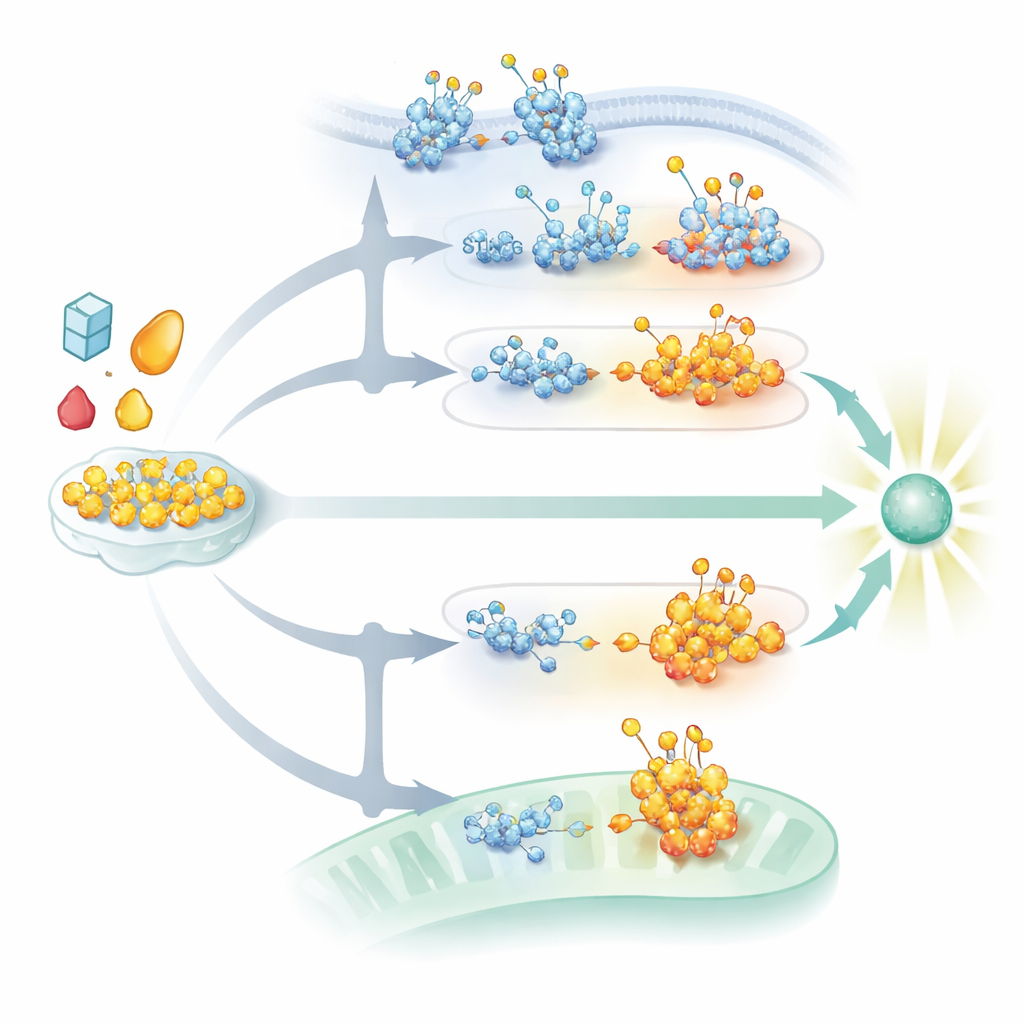
Metabolismo, doença e terapias futuras
Como o principal doador de açúcar para a O-GlcNAcilação é produzido por uma via metabólica conhecida como via biossintética das hexosaminas, mudanças no uso de nutrientes moldam diretamente a sinalização antiviral. Muitos vírus impulsionam essa via em seu favor, enquanto o aumento experimental ou bloqueio do fluxo de hexosaminas pode fortalecer ou enfraquecer respostas antivirais em modelos animais. A revisão conecta esses mecanismos a doenças humanas: tumores frequentemente redesenham a glicosilação para amortecer a sinalização de interferon e escapar do ataque imune, enquanto estresse metabólico crônico ou defeitos hereditários no processamento de glicanos podem deslocar o equilíbrio em direção a autoimunidade prejudicial. Os autores argumentam que enzimas que controlam a glicosilação — especialmente aquelas que adicionam ou removem O-GlcNAc ou constroem estruturas N-ligadas-chave — são alvos promissores, embora desafiadores, para drogas. Terapias futuras provavelmente precisarão atuar de forma específica por sítio e sensível ao contexto, ajustando o “glico-código” em direção a melhor proteção contra infecções, câncer e distúrbios inflamatórios sem desencadear novas formas de desequilíbrio imunológico.
A visão geral para a saúde do dia a dia
Em termos cotidianos, este artigo revela que os alarmes antivirais da linha de frente do corpo não operam isoladamente — eles estão conectados ao uso de energia e à química dos açúcares da célula. Pequenas etiquetas de açúcar em um punhado de proteínas críticas decidem se um genoma viral solto provoca um aviso moderado, uma defesa completa ou uma reação exagerada e perigosa. Ao decodificar e, eventualmente, aprender a ajustar esse sistema de controle baseado em açúcares, os pesquisadores esperam projetar tratamentos que tornem vacinas mais eficazes, ajudem a eliminar infecções persistentes, exponham tumores ao sistema imune e acalmem inflamação descontrolada em doenças autoimunes.
Citação: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Palavras-chave: imunidade inata, glicosilação, via RLR, cGAS-STING, O-GlcNAcilação