Clear Sky Science · pt
Percepções estruturais sobre a maquinaria do tipo IV pilus de Thermus thermophilus que monta dois pili distintos
Pelinhos bacterianos minúsculos com grandes funções
Bactérias podem ser microscópicas, mas muitas possuem notáveis “pelos” de superfície que lhes permitem mover-se, aderir a superfícies e até captar DNA livre do ambiente. Neste estudo, os pesquisadores examinam como uma bactéria termófila, Thermus thermophilus, constrói e opera uma sofisticada nanomáquina que empurra esses pelos — chamados pilos — através de seu envelope celular. Entender essa maquinaria não apenas revela como micróbios se adaptam e evoluem, mas também inspira futuras aplicações em nanotecnologia e novas formas de neutralizar bactérias nocivas.
Dois pelos diferentes vindos de uma única máquina
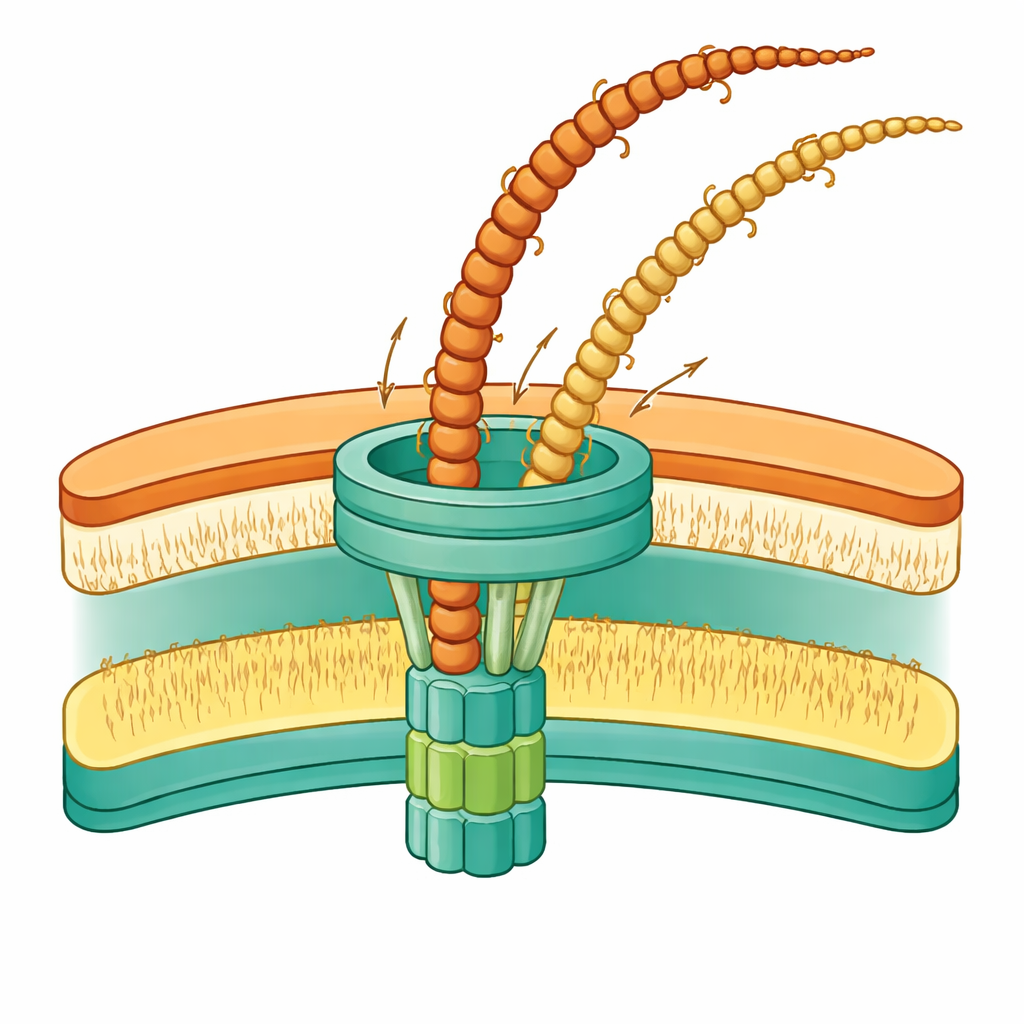
Thermus thermophilus produz dois tipos distintos de pilos: um filamento mais largo e espesso e outro mais estreito e delgado. Trabalhos anteriores mostraram que esses filamentos são feitos de blocos construtores diferentes e provavelmente cumprem funções distintas, como locomoção sobre superfícies ou captação de DNA. Ainda assim, ambos são montados pela mesma máquina multipartida que atravessa da superfície interna à externa da célula. A questão central deste estudo é como um único sistema consegue montar dois filamentos diferentes e empurrá‑los através das camadas protetoras da célula até o ambiente externo.
Mapeando o hardware oculto
Para descobrir como a máquina é montada, os pesquisadores usaram tomografia crioeletrônica, uma técnica que congela células rapidamente e as imagina em 3D a temperaturas muito baixas. Eles combinaram essas imagens com alterações genéticas direcionadas que removeram ou modificaram partes específicas da máquina. Ao comparar células normais com mutantes sem certos componentes, puderam identificar quais formas desfocadas em seus mapas 3D correspondiam a quais proteínas. Ferramentas avançadas de predição estrutural foram então usadas como plantas moleculares, ajudando a encaixar esses modelos proteicos nas densidades observadas e a montar um modelo hipotético de comprimento total da maquinaria.
Um elo flexível que mantém tudo unido
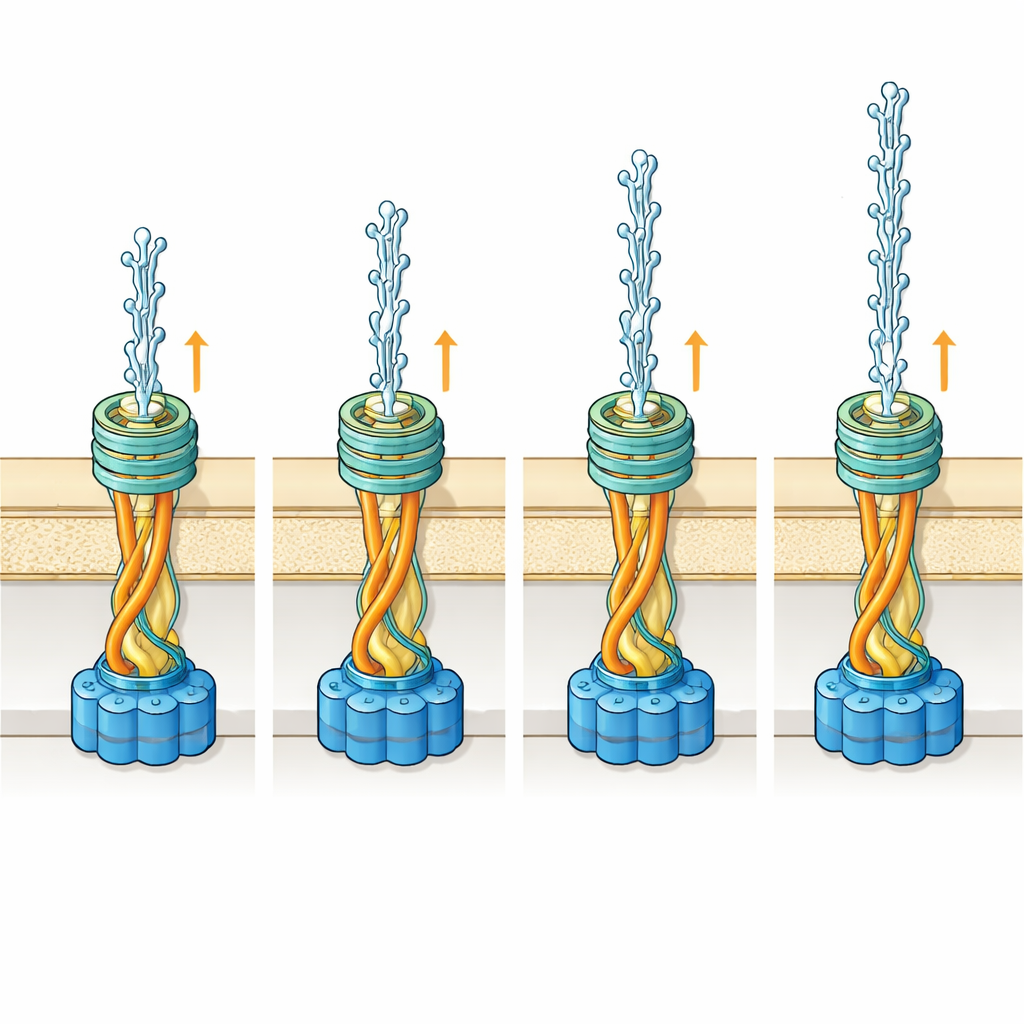
Um resultado de destaque refere‑se a uma proteína chamada PilW. Esse componente situa‑se entre uma porta na membrana externa e uma plataforma interna ancorada na membrana citoplasmática. Quando PilW está totalmente ausente, os pilos não alcançam o exterior e se acumulam no espaço entre as membranas. Quando apenas uma parte de PilW é aparada, a máquina ainda funciona, mas seus componentes internos deslocam‑se de posição e as membranas adjacentes curvam‑se para dentro. Essas observações sugerem que PilW atua como uma amarra flexível que liga a porta externa à plataforma interna, ajustando seu comprimento e forma à medida que a máquina alterna entre estados ociosos e ativos. Os modelos da equipe indicam que essa flexibilidade permite ao sistema lidar com a lacuna incomumente larga entre as duas membranas em Thermus, ao mesmo tempo em que alinha todas as partes o suficiente para montar e ejetar os pilos.
Observando os filamentos e seus revestimentos de açúcar
Paralelamente às imagens in‑cell, os pesquisadores também isolaram os dois tipos de pilos e os examinaram em maior detalhe usando crio‑microscopia eletrônica de partícula única. Essa abordagem de resolução mais alta revelou o arranjo preciso dos blocos construtores e, crucialmente, permitiu à equipe modelar as moléculas de açúcar que decoram a superfície dos filamentos. O pilus mais largo carrega três sítios de ligação de açúcar por bloco construtor, produzindo um halo denso de carboidratos. O pilus mais estreito tem apenas um desses sítios, mas sua cadeia de açúcar projeta‑se mais para fora, fazendo o filamento parecer maior do que o núcleo proteico sugeriria. Simulações computacionais então exploraram como esses açúcares se dobram e oscilam enquanto o filamento passa pela porta da membrana externa.
Uma porta compartilhada para dois cabos muito diferentes
Ao encaixar suas estruturas detalhadas dos pilos em um modelo da porta da membrana externa, chamada PilQ, a equipe descobriu que, em princípio, ambos os tipos de filamento podem deslizar pela mesma abertura. Para o filamento mais largo, seus vários açúcares têm espaço suficiente para assumir muitas conformações enquanto passam pela porta. Para o filamento mais estreito, o espaço fica apertado em um ponto do canal, de modo que algumas conformações de açúcar colidiriam com as paredes. Simulações sugerem que, nesse caso, a cadeia de açúcar provavelmente fica mais aderida ao filamento enquanto está dentro da porta e só se abre novamente fora da célula. Em vez de evoluir uma porta maior e mais custosa para acomodar confortavelmente ambos os filamentos, a bactéria parece depender da flexibilidade natural dessas cadeias de açúcar para fazer o sistema funcionar de forma eficiente.
O que isso significa para a vida microbiana
Em conjunto, o estudo desenha um quadro coerente de como uma única máquina adaptável constrói e exporta dois pilos muito diferentes em uma bactéria de fontes termais. Uma proteína ligação flexível parece manter as partes internas e externas alinhadas à medida que o motor cicla e a estrutura encurta ligeiramente durante o crescimento ativo do filamento. Ao mesmo tempo, os revestimentos de açúcar nos pilos lhes conferem proteção e alcance, mantendo‑se suficientemente flexíveis para se espremerem por um canal de saída relativamente estreito. Para não especialistas, a mensagem central é que mesmo micróbios simples dependem de conjuntos móveis altamente coordenados para sobreviver e evoluir — dispositivos moleculares cuja elegância e eficiência rivalizam, e às vezes superam, máquinas humanas na escala nanométrica.
Citação: Neuhaus, A., McLaren, M., Isupov, M.N. et al. Structural insights into the Thermus thermophilus type IV pilus machinery assembling two distinct pili. Commun Biol 9, 474 (2026). https://doi.org/10.1038/s42003-026-09762-0
Palavras-chave: pilis do tipo IV, nanomáquinas bacterianas, crio-microscopia eletrônica, glicosilação de proteínas, Thermus thermophilus