Clear Sky Science · pt
Modelagem dirigida pela taxa de crescimento sugere que a adaptação fenotípica impulsiona a resistência a fármacos em melanoma com mutação BRAFV600E
Células cancerosas que aprendem a conviver com medicamentos
Fármacos direcionados transformaram o tratamento de muitas pessoas com melanoma, um câncer de pele grave. Ainda assim, esses medicamentos quase sempre deixam de funcionar: tumores que antes encolhiam começam a crescer novamente. Este trabalho coloca uma pergunta simples, porém poderosa: em vez de depender apenas de mutações genéticas, as células de melanoma podem «aprender» a sobreviver ao tratamento mudando seu comportamento — e esse aprendizado poderia explicar por que algumas formas de administração do medicamento funcionam melhor do que outras?
De células sensíveis a sobreviventes
Os pesquisadores concentraram-se em células de melanoma que carregam uma alteração comum no gene BRAF, que as torna especialmente sensíveis a um tipo de medicamento conhecido como inibidor de BRAF. Em experimentos de laboratório de trabalhos anteriores, essas células foram expostas ao fármaco encorafenibe em doses diferentes e por durações distintas. Ao medir cuidadosamente quão rapidamente as células cresciam ou morriam em cada condição, os autores dividiram as células em duas categorias amplas: células não expostas ao medicamento (drug-naive) que nunca tinham visto o fármaco, e células adaptadas ao fármaco que viveram na presença dele por pelo menos uma semana. As células não expostas cresciam bem sem tratamento, mas eram fortemente retardadas ou mortas pelo medicamento. As células adaptadas, em contraste, cresciam melhor na presença do fármaco, mas perdiam essa vantagem quando o medicamento era removido — sugerindo que sua sobrevivência estava ligada a uma mudança de estado flexível e reversível, em vez de a uma alteração genética permanente.
Um mapa de comportamentos celulares ocultos
Para entender essas mudanças, a equipe construiu um modelo matemático em que cada célula cancerosa recebe um «estado fenotípico» — uma posição abstrata em uma escala que vai de muito sensível ao medicamento a muito resistente. Em vez de assumir apenas dois tipos de células, eles permitiram muitos estados intermediários, refletindo deslocamentos graduais no comportamento observados em marcadores biológicos de resistência. Para cada combinação de estado e dose do medicamento, estimaram uma taxa de crescimento líquida, que poderia ser positiva (mais divisões celulares do que mortes) ou negativa (mais mortes do que divisões). Todas essas taxas foram organizadas em uma grade, ou «matriz de aptidão», que funciona como uma paisagem: alguns estados em certas doses são bons lugares para as células prosperarem, outros são letais. No modelo, as células podem mover-se passo a passo por essa paisagem conforme o tratamento é ligado ou desligado.
As células derivam ou escalam em busca de vantagem?
O ponto desconhecido era como as células se movem por essa paisagem. Os autores testaram quatro estratégias possíveis. Em uma, as células nunca mudam de estado, de modo que quaisquer células resistentes devem estar presentes desde o início. Em outra, as células perambulam aleatoriamente entre estados vizinhos, como uma caminhada do bêbado, independentemente de a situação melhorar ou não. Nas duas estratégias restantes, as células tendem a mover-se em direção a estados em que sua taxa de crescimento é maior — seja de forma ruidosa, com alguns passos em falso, ou de forma forte, sempre escalando em direção a melhor sobrevida. Quando a equipe rodou simulações por computador e as comparou com dados reais de laboratório, especialmente experimentos em que o fármaco foi administrado de forma contínua ou em padrão liga–desliga (uma semana com, uma semana sem), apenas as estratégias em que as células escalam em direção a maior aptidão conseguiram reproduzir o observado: o tratamento intermitente com alta dose suprimiu melhor o número de células do que o tratamento contínuo com o mesmo tempo total e uma quantidade global maior de fármaco.
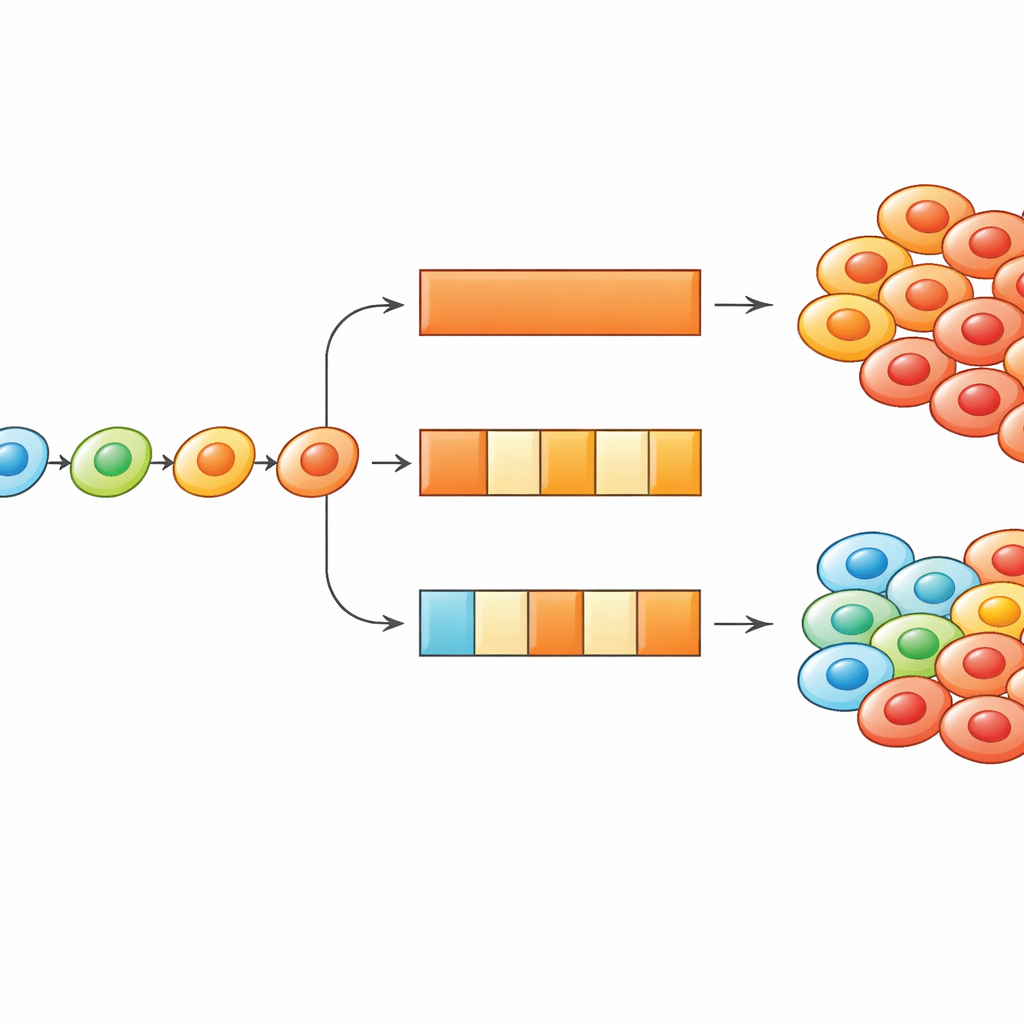
Usando dosagens liga–desliga para virar a adaptação contra o câncer
Indo mais a fundo, os pesquisadores usaram tanto simulações quanto equações mais simples para explorar com que frequência as células podem mudar de estado e quanto duram os períodos com e sem fármaco. Eles descobriram que quando as células se adaptam de modo dirigido, os esquemas de tratamento podem ser ajustados para ou desacelerar essa adaptação, ou explorá‑la. Diminuir a frequência com que as células atualizam seu estado — conceitualmente, frear os mecanismos biológicos que viabilizam a mudança fenotípica — tende a tornar os tratamentos intermitentes mais eficazes, porque as células não conseguem tão rapidamente escalar até estados altamente resistentes. Por outro lado, se as células começam em um estado fortemente resistente, as pausas no uso do fármaco podem dar tempo para que deslizem de volta a estados mais sensíveis, de modo que a reintrodução do medicamento provoque uma onda de mortes celulares. O estudo mostra como o timing da dosagem e a velocidade da adaptação celular juntas determinam qual esquema funciona melhor.
O que isso significa para o cuidado do câncer no futuro
Para o público em geral, a mensagem central é que as células cancerosas não são apenas inimigos fixos; elas mudam de forma. Nesse sistema de melanoma, as células parecem mover‑se ativamente em direção a comportamentos que as ajudam a crescer nas condições que enfrentam. O modelo dos autores sugere que essa adaptação dirigida por si só — sem invocar clones permanentes distintos — pode explicar por que esquemas de administração liga–desliga às vezes superam a dosagem constante, mesmo quando usam menos fármaco no total. Embora esses resultados venham de células cultivadas em laboratório e exijam mais trabalho antes de orientar o tratamento de pacientes, a abordagem oferece um arcabouço prático: ao medir quão rápido e em que direção as células cancerosas se adaptam, os médicos podem eventualmente desenhar cronogramas de tratamento que não só ataquem os tumores, mas também conduzam o «aprendizado» fenotípico das células para becos sem saída em vez de rotas de escape.
Citação: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Palavras-chave: melanoma, resistência a fármacos, plasticidade celular, terapia intermitente, modelagem matemática