Clear Sky Science · pt
Base estrutural da ativação por dimerização da quinol redutase de óxido nítrico de Neisseria meningitidis
Como as bactérias driblam nossa defesa imune
Quando bactérias nocivas invadem o organismo, nossas células imunes liberam moléculas tóxicas, como o óxido nítrico, para eliminá‑las. Alguns patógenos, no entanto, desenvolveram artifícios moleculares para neutralizar esse ataque e sobreviver. Este estudo revela, em detalhe atômico, como uma enzima bacteriana chave se reconfigura em pares para se tornar muito mais eficiente na desintoxicação do óxido nítrico, e por que compreender esse comportamento metamórfico pode abrir novos caminhos para o projeto de antibióticos.
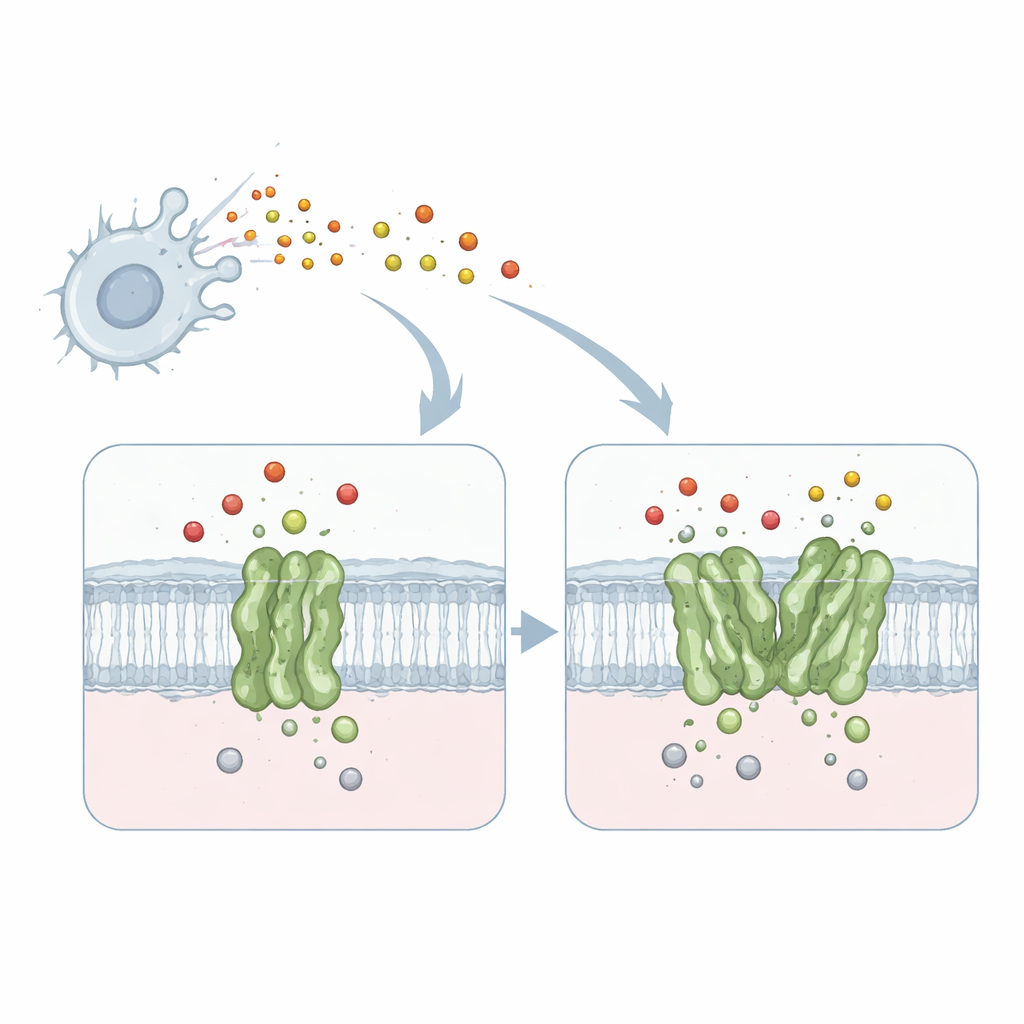
Uma máquina minúscula que desarma um gás tóxico
O trabalho foca em uma proteína de membrana chamada quinol‑dependente redutase de óxido nítrico, ou qNOR, da bactéria causadora de meningite Neisseria meningitidis. A qNOR localiza‑se na membrana celular bacteriana e converte o óxido nítrico — um gás tóxico produzido pelo nosso sistema imune — em produtos menos nocivos. Essa desintoxicação permite que o microrganismo continue respirando e crescendo mesmo em ambientes hostis, como dentro de macrófagos humanos. Porque a respiração e a remoção de óxido nítrico são vitais para a sobrevivência do patógeno, a qNOR é um alvo atraente para novos fármacos antimicrobianos.
Quando um é bom, mas dois são melhores
Estudos bioquímicos anteriores mostraram que a qNOR pode existir como uma única unidade (monômero) ou como um par (dímero), e que o dímero age de duas a quatro vezes mais rápido na neutralização do óxido nítrico. Até agora, não estava claro por que simplesmente emparelhar duas cópias da mesma enzima tinha um impacto tão dramático no desempenho. Para responder a isso, os pesquisadores usaram crio‑microscopia eletrônica de partícula única em alta resolução para capturar estruturas tridimensionais detalhadas tanto do monômero quanto do dímero de qNOR da mesma cepa bacteriana. Obtiveram visões em resolução quase atômica — 1,89 Å para o dímero e 2,25 Å para o monômero — nítidas o bastante para localizar cadeias laterais de aminoácidos individuais, íons metálicos e muitas moléculas de água.
Uma hélice flexível que vira um reforço estabilizante
Surpreendentemente, o coração catalítico da enzima — o centro metálico onde o óxido nítrico é convertido — parecia quase idêntico em ambas as formas. Em vez disso, as diferenças-chave surgiam a alguma distância, numa hélice transmembrana chamada TM10 e em como ela faz contato com outra hélice (TM2) quando duas moléculas de qNOR emparelham. No monômero, a TM10 está frouxamente ancorada e pode oscilar e dobrar substancialmente, como revelado pela análise computacional dos dados de crio‑EM. No dímero, a TM10 de cada parceiro se trava contra a vizinha para formar um feixe de quatro hélices, restringindo muito seu movimento. Essa estabilização reposiciona sutilmente um aminoácido crucial, um glutamato chamado Glu563, aproximando‑o de outro glutamato (Glu494) próximo ao sítio ativo e delineando uma rota mais focalizada para os prótons entrantes necessários para a reação.
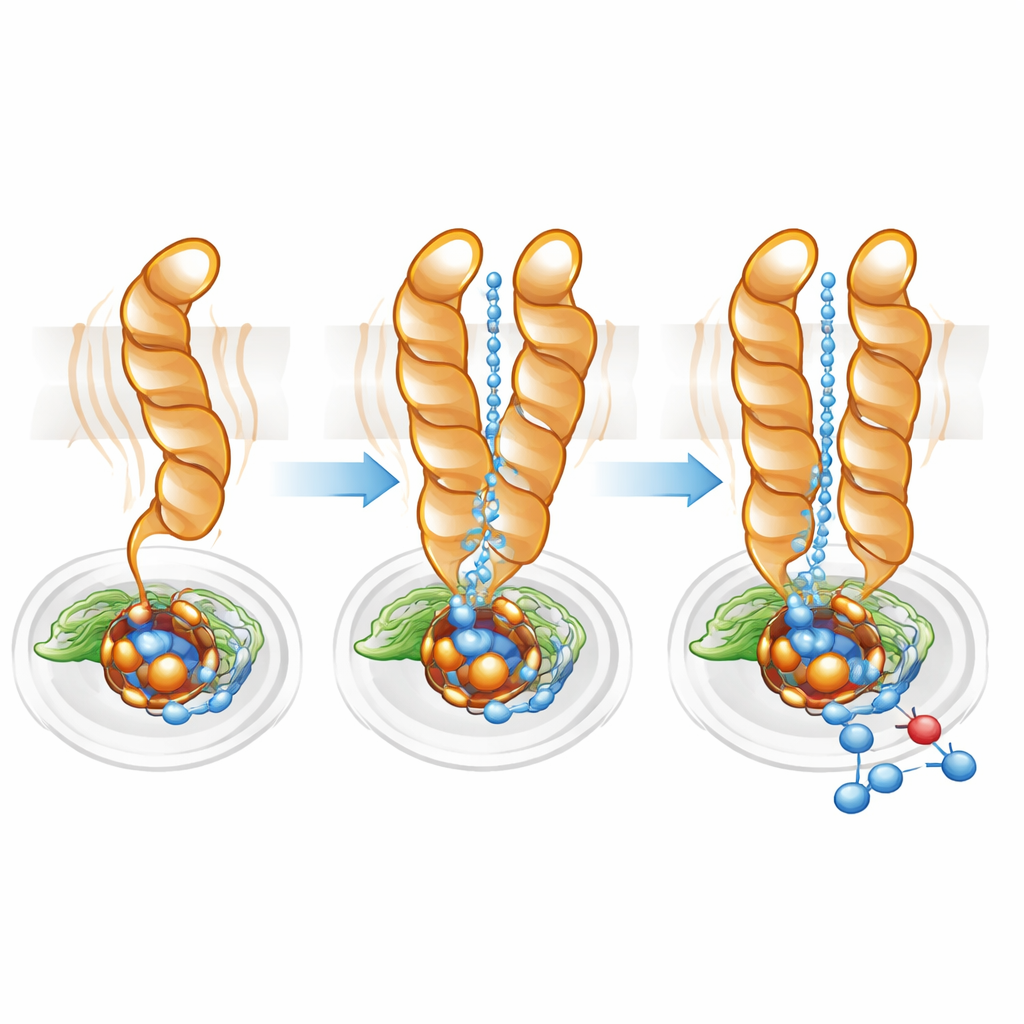
Ajustando fino a via dos prótons
Prótons — íons de hidrogênio carregados positivamente — devem ser entregues de forma eficiente do interior da célula ao sítio ativo enterrado para que a redução do óxido nítrico prossiga. Usando software de mapeamento de trajetórias, a equipe encontrou uma cavidade hidrofílica conectando o citoplasma ao sítio ativo em ambos monômero e dímero. Contudo, no monômero esse canal era mais largo e mais difuso, consistente com a maior mobilidade da TM10. No dímero, a posição travada da TM10 e a orientação favorável do Glu563 ajudaram a definir uma via mais direta e melhor organizada. Mutar o Glu563 para aminoácidos que não podem formar as mesmas interações reduziu a atividade da enzima a menos de 10% do normal e também desestabilizou o dímero, enquanto mutações em posições relacionadas diminuíram a quantidade do ferro não‑heme essencial no sítio ativo. Em conjunto, esses resultados mostram que a formação do dímero e o posicionamento preciso de Glu563 e Glu494 estão intimamente ligados tanto à integridade estrutural quanto à eficiência catalítica.
Transformando conhecimentos estruturais em novos tratamentos
As descobertas revelam uma linha clara desde o emparelhamento proteico na superfície da membrana até ajustes finos no interior do sítio ativo que controlam com que eficiência a qNOR remove o óxido nítrico. Em termos simples, quando duas cópias da enzima se prendem, elas esticam e endurecem um segmento flexível que ajuda a direcionar prótons para o centro reacional, aumentando a produção da enzima. Para o desenvolvimento de fármacos, isso sugere uma estratégia não convencional: em vez de bloquear diretamente o sítio ativo, seria possível projetar moléculas que separem o dímero ou perturbem a interação Glu563–Glu494, forçando a enzima ao estado monomérico lento. Como a qNOR e enzimas relacionadas são cruciais para a sobrevivência de vários patógenos perigosos e resistentes a medicamentos, abordagens guiadas pela estrutura podem contribuir para a próxima geração de antimicrobianos dirigidos.
Citação: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Palavras-chave: desintoxicação de óxido nítrico, respiração bacteriana, enzimas de membrana, crio-microscopia eletrônica, alvos para fármacos antimicrobianos