Clear Sky Science · pt
Multiômica espacial revela características imuno-metabólicas induzidas por eletroporação irreversível na margem inflamatória do câncer de fígado
Por que um novo tratamento para câncer de fígado merece uma atenção maior
A eletroporação irreversível (IRE) é uma técnica mais recente para destruir tumores hepáticos usando pulsos elétricos curtos e de alta voltagem em vez de calor. Como pode poupar vasos sanguíneos e ductos biliares próximos, é especialmente útil para cânceres em locais delicados. Ainda assim, até um terço dos pacientes apresenta recidiva tumoral justamente ao lado da área tratada. Este estudo investiga o que ocorre nessa estreita região de borda após a IRE — e se mudanças ocultas nas células imunes e no metabolismo celular ali podem, silenciosamente, preparar o terreno para o retorno do câncer.
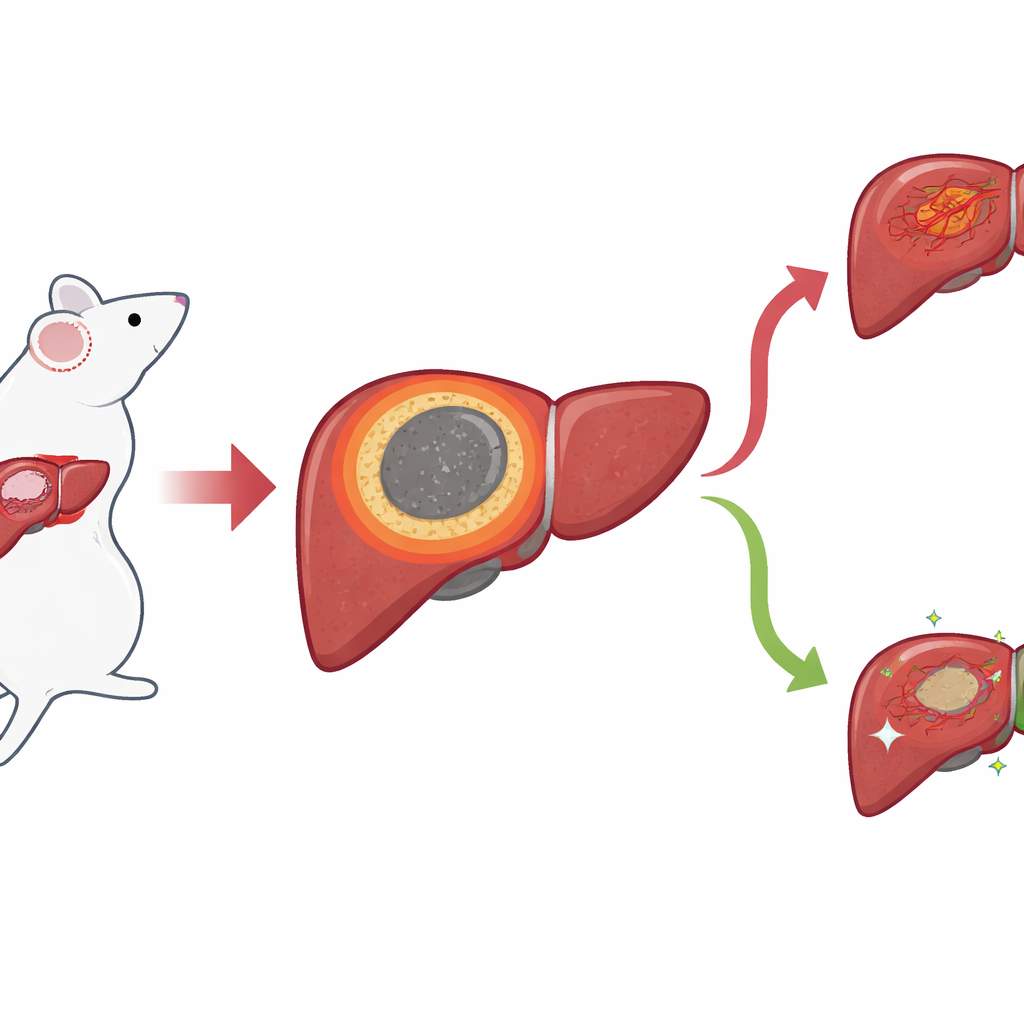
Uma borda estreita com grandes consequências
Usando um modelo murino de câncer de fígado, os pesquisadores focaram o anel fino de tecido que se forma entre o núcleo necrótico (abladido) e o fígado saudável após a IRE. Eles chamam essa zona de margem inflamatória, ou MI. Imagens microscópicas padrão mostraram que essa zona fica exatamente onde as recidivas locais costumam surgir, mas seus limites eram difíceis de definir a olho nu. Para obter um retrato mais nítido, a equipe aplicou métodos “espaciais” que identificam quais genes e pequenas moléculas estão presentes, preservando sua localização no tecido. Com transcriptômica espacial, mapearam a atividade gênica ponto a ponto e descobriram um aglomerado distinto de pontos que se alinhava precisamente com a MI, separando o centro necrótico do fígado e das áreas tumorais normais.
Células imunes se reúnem — mas muitas contêm o ataque
Os cientistas então usaram RNA-seq de célula única e de núcleo único, juntamente com um potente método de perfilagem chamado CyTOF, para catalogar tipos celulares individuais por todo o fígado. Eles descobriram que a MI é dominada por um tipo de célula imune chamado macrófago. Em particular, um subconjunto semelhante a “macrófagos associados a lipídios” (LAMs) inundou a MI nos dias seguintes à IRE. Essas células exibem marcadores de superfície e assinaturas gênicas vinculadas à supressão imune, incluindo altos níveis de PD-L1, uma molécula conhecida por atenuar respostas de células T. Análises de expressão gênica sugeriram que esses macrófagos são hábeis em engolfar material, responder a quimiotáticos e emitir sinais que podem conter as próprias células T necessárias para matar células tumorais. Imagens confirmaram que macrófagos PD-L1-positivos eram muito mais abundantes na MI do que no tecido normal adjacente.
Um ponto quente de química lipídica alterada
Em seguida, a equipe sobrepôs esse panorama imune com metabolômica espacial, uma abordagem de imagem por espectrometria de massa que mapeia a distribuição de centenas de pequenas moléculas. Mostraram que a MI possui uma impressão metabólica diferente tanto do núcleo morto quanto do fígado circundante. Nessa faixa estreita, muitas vias lipídicas foram fortemente ativadas, incluindo a produção de ácidos graxos insaturados, derivados do ácido araquidônico e esfingolipídios. Lipídios sinalizadores chave, como prostaglandinas e leucotrienos — derivados do ácido araquidônico — estavam enriquecidos na MI, enquanto outras rotas enzimáticas para processar a mesma molécula estavam relativamente atenuadas. Outra família lipídica, os esfingolipídios — incluindo ceramidas e esfingomielinas — também se acumulou, sustentada pelo aumento da expressão das enzimas que os sintetizam e remodelam.
Uma mudança em etapas do dano para um nicho rico em combustível
Ao subdividir a margem inflamatória em três camadas finas do núcleo necrótico para fora, os pesquisadores observaram uma mudança gradual na química. Mais próxima da zona necrótica, lipídios complexos e moléculas relacionadas ao colesterol eram mais abundantes, enquanto mais externamente aumentavam pequenas moléculas relacionadas à energia, como glicose e certos aminoácidos. Esse padrão sugere que, em uma curta distância, o tecido transita de um ambiente carregado de lipídios e rico em sinais para outro direcionado a abastecer sobrevivência e crescimento celular. Os autores propõem que esse reprogramamento em etapas ajuda a sustentar os macrófagos imunossupressores, ávidos por lipídios, que dominam a MI e podem silenciosamente preparar o terreno para que células tumorais se restabeleçam.
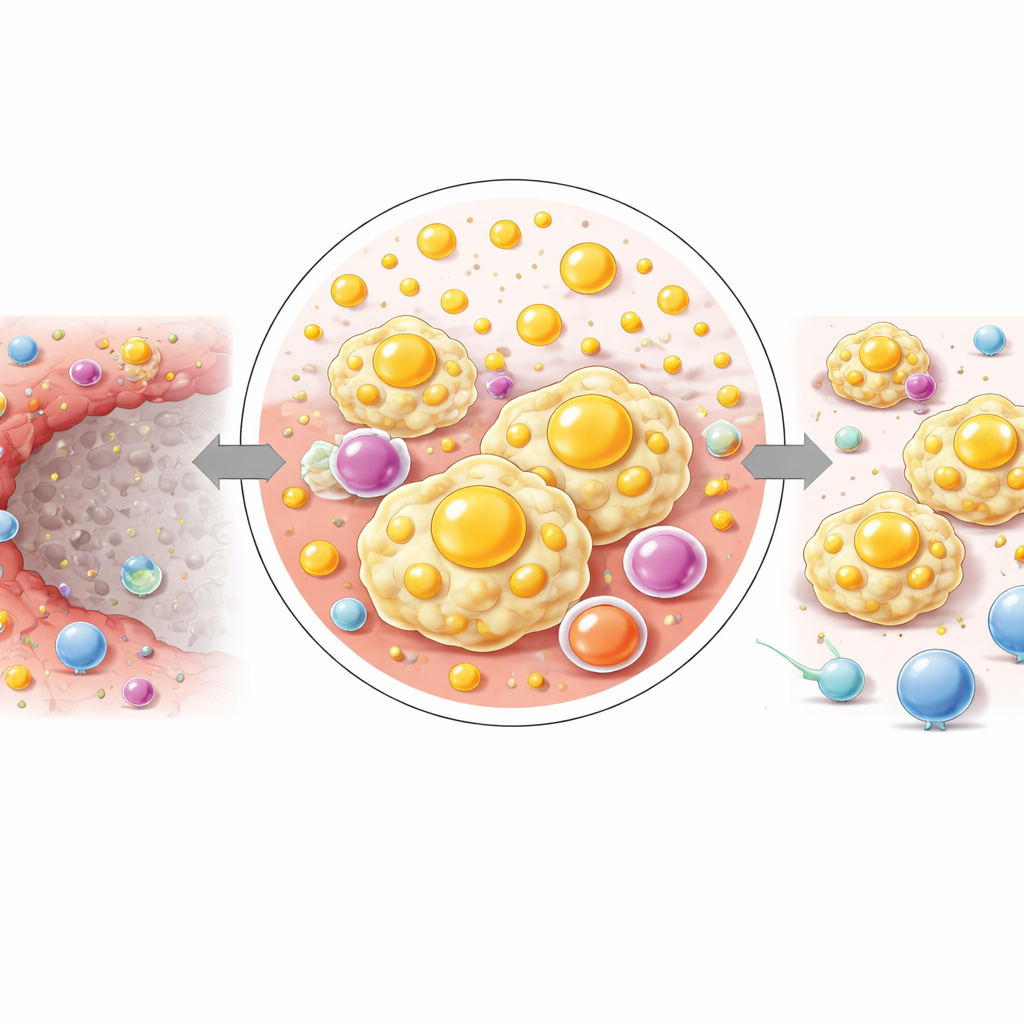
O que isso significa para o cuidado futuro do câncer de fígado
Em termos simples, este trabalho mostra que a IRE faz mais do que matar células tumorais: ela também cria um anel estreito de tecido onde células imunes e a química lipídica juntos constroem um bairro protegido e favorável ao tumor. Os macrófagos nessa zona são abundantes, carregados de lipídios e inclinados a desligar as células T em vez de ajudá‑las. Como essas mudanças estão fortemente ligadas a vias metabólicas específicas, elas apontam para novos ângulos terapêuticos. Combinar IRE com fármacos que alvejarem o metabolismo lipídico ou bloqueiem PD-L1 nessa margem poderia, em princípio, transformar uma borda propensa à recidiva em uma zona que realmente conclui o trabalho contra o câncer de fígado.
Citação: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Palavras-chave: câncer de fígado, ablação tumoral, microambiente imune, macrófagos, metabolismo de lipídios