Clear Sky Science · pt
Ativadores de NRF2 e o inibidor da exportação nuclear, selinexor, restringem coronavírus ao mirar uma rede envolvendo ACE2, TMPRSS2 e XPO1 por um mecanismo independente de NRF2
Fármacos que Ajudam as Células a Dizer “Não” aos Coronavírus
A maioria dos tratamentos contra coronavírus hoje mira o próprio vírus. Mas os vírus são mestres da mudança, e novas variantes podem rapidamente enfraquecer esses fármacos. Este estudo explora uma estratégia diferente: tornar nossas próprias células menos receptivas tanto a coronavírus perigosos como o SARS-CoV-2 quanto a cepas sazonais mais brandas. Ao ajustar como as células lidam com algumas proteínas-chave de controle, os pesquisadores mostram que pequenas moléculas existentes podem reduzir fortemente a infecção em modelos de laboratório, e fazem isso de um modo que não depende da via antiviral pela qual ficaram famosas.
Um Novo ângulo na Defesa contra Coronavírus
A equipe concentrou-se em compostos conhecidos por ativar um programa de proteção celular controlado por uma proteína chamada NRF2. Esses compostos — 4-octil itaconato (4OI), bardoxolona (BARD) e sulforafano (SFN) — foram testados ao lado do selinexor (SEL), um fármaco que bloqueia uma proteína de transporte chamada XPO1, que ajuda a mover outras proteínas para fora do núcleo celular. Em modelos de células pulmonares e renais, todos os quatro fármacos reduziram os níveis de SARS-CoV-2 sem prejudicar as células. Eles também funcionaram contra várias variantes de preocupação. Surpreendentemente, quando o NRF2 foi removido geneticamente, os vírus na verdade se replicaram melhor, provando que o NRF2 é naturalmente protetor — mas os fármacos ainda funcionaram bem, mostrando que seu poder antiviral vem por uma via diferente. 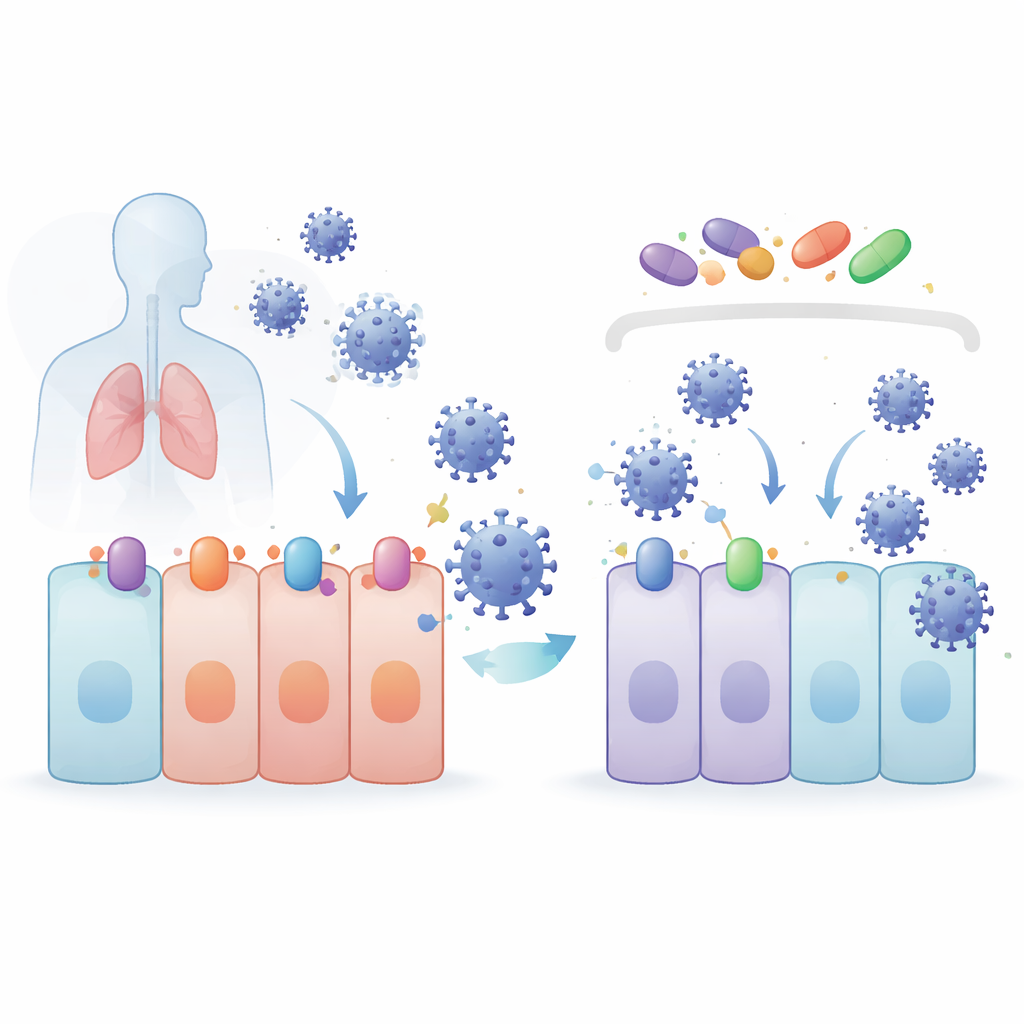
Fechando a Porta de Entrada Viral
Coronavírus iniciam a infecção acoplando-se a proteínas receptoras na superfície celular. Para SARS-CoV-2 e seus parentes próximos, a porta principal é a ACE2, com auxílio de uma enzima cortadora chamada TMPRSS2. A proteína de exportação XPO1 também parece favorecer a infecção. Os pesquisadores descobriram que 4OI, BARD, SFN e SEL reduziram as quantidades de ACE2, TMPRSS2 e XPO1 em células humanas do pulmão. 4OI e SEL foram especialmente potentes quando presentes antes da infecção, e bloquearam a entrada de partículas semelhantes ao vírus cobertas com proteínas spike de coronavírus. Em outras palavras, esses fármacos não apenas retardam o vírus depois que ele entra — eles ajudam a remover as fechaduras e alças que o vírus precisa para abrir a porta em primeiro lugar.
Como as Células Desmontam Auxiliares Virais Chave
Aprofundando, a equipe mostrou que 4OI acelera a degradação da proteína ACE2. Em condições normais, ACE2 persiste por muitas horas; com 4OI, ela desapareceu da superfície celular em uma fração desse tempo. Essa destruição exigiu dois “marcadores” celulares, NEDD4L e MDM2, que fixam bandeiras moleculares de “descartar” em proteínas. Bloquear esses marcadores enfraqueceu a capacidade do 4OI de eliminar ACE2. Surpreendentemente, a maquinaria usual de trituração de proteínas, o proteassoma, não foi a via principal. Em vez disso, ACE2 foi direcionada para o sistema de reciclagem e eliminação da célula, o lisossomo. Os fármacos também reduziram a atividade gênica de ACE2 e XPO1, em parte ao diminuir a ativação de STAT3, uma proteína que normalmente aumenta a leitura do gene ACE2. 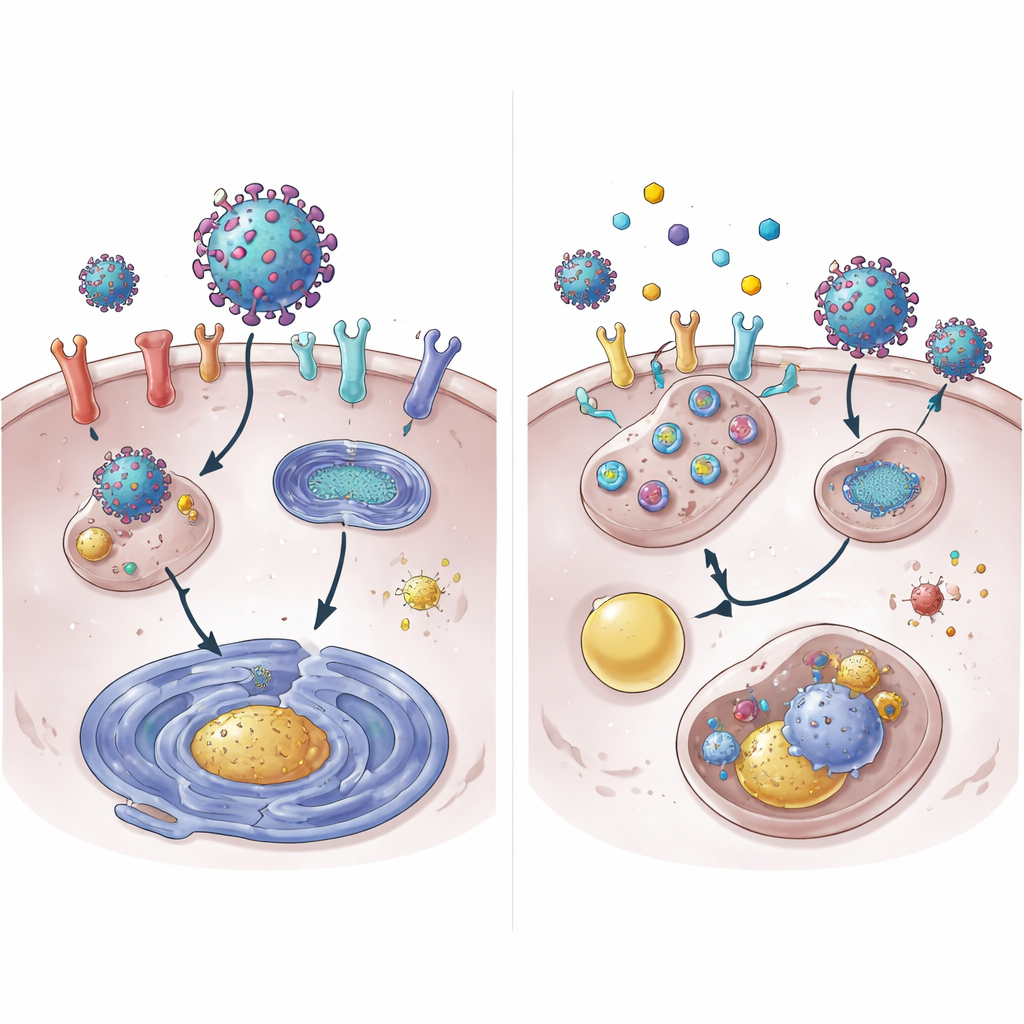
Coronavírus Sazonais e a Conexão com XPO1
Os cientistas voltaram-se então para o hCoV-229E, um coronavírus sazonal que costuma causar resfriados leves mas pode ser perigoso em pessoas com imunidade comprometida. Usando vírus engenheirados que brilham quando se replicam, mostraram que os quatro compostos suprimiram fortemente o 229E em células pulmonares e de vasos sanguíneos, mesmo quando o NRF2 estava ausente. Ao contrário do SARS-CoV-2, esse vírus usa um receptor diferente, ANPEP, que os fármacos não alteraram. Em vez disso, o impacto deles correlacionou-se fortemente com o quanto reduziram XPO1. Reduzir a expressão de XPO1 por si só diminuiu drasticamente a replicação do 229E, e o efeito do selinexor quase desapareceu nessas células com pouco XPO1. Essa hierarquia — SEL mais dependente de XPO1, BARD menos — sugere que cada composto tem uma mistura ligeiramente diferente de alvos, com XPO1 atuando como um hub central para muitas de suas ações antivirais.
O Que Isso Pode Significar para Tratamentos Futuros
Para não especialistas, a mensagem-chave é que é possível combater coronavírus não só atacando o vírus, mas reprogramando de forma leve nossas próprias células para que fiquem mais difíceis de infectar. Em células humanas cultivadas em laboratório, os compostos estudados eliminaram locais de acoplamento cruciais e vias auxiliares das quais SARS-CoV-2 e um coronavírus do resfriado comum dependem, e fizeram isso em grande parte sem a via NRF2 que inicialmente os tornava interessantes. Embora essas descobertas ainda sejam pré-clínicas e não se traduzam diretamente em medicamentos, elas destacam um caminho promissor: fármacos que simultaneamente reduzem a entrada viral, atenuam inflamação prejudicial e protegem tecidos ao mirar uma rede compartilhada de proteínas do hospedeiro como ACE2, TMPRSS2 e XPO1.
Citação: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Palavras-chave: antivirais direcionados ao hospedeiro, entrada de coronavírus, ACE2 e TMPRSS2, ativadores de NRF2, inibição de XPO1