Clear Sky Science · pt
Quantificação ultrarrápida e específica de miRNA via cinética de extinção de fluorescência em única molécula
Por que testes rápidos para doenças importam
Diagnosticar doenças como câncer ou infecções virais frequentemente depende de detectar vestígios minúsculos de material genético no sangue ou em outros fluidos corporais. Os testes de referência atuais podem ser muito precisos, mas costumam ser lentos, caros ou têm dificuldade em identificar sinais muito raros. Este estudo apresenta um novo método baseado em microscopia, chamado Q‑FISH, capaz de ler essas pistas genéticas em menos de um segundo. Se convertido em ferramentas clínicas, essa velocidade e precisão poderiam facilitar a detecção precoce de doenças, acompanhar a resposta a tratamentos e personalizar o cuidado para cada paciente.
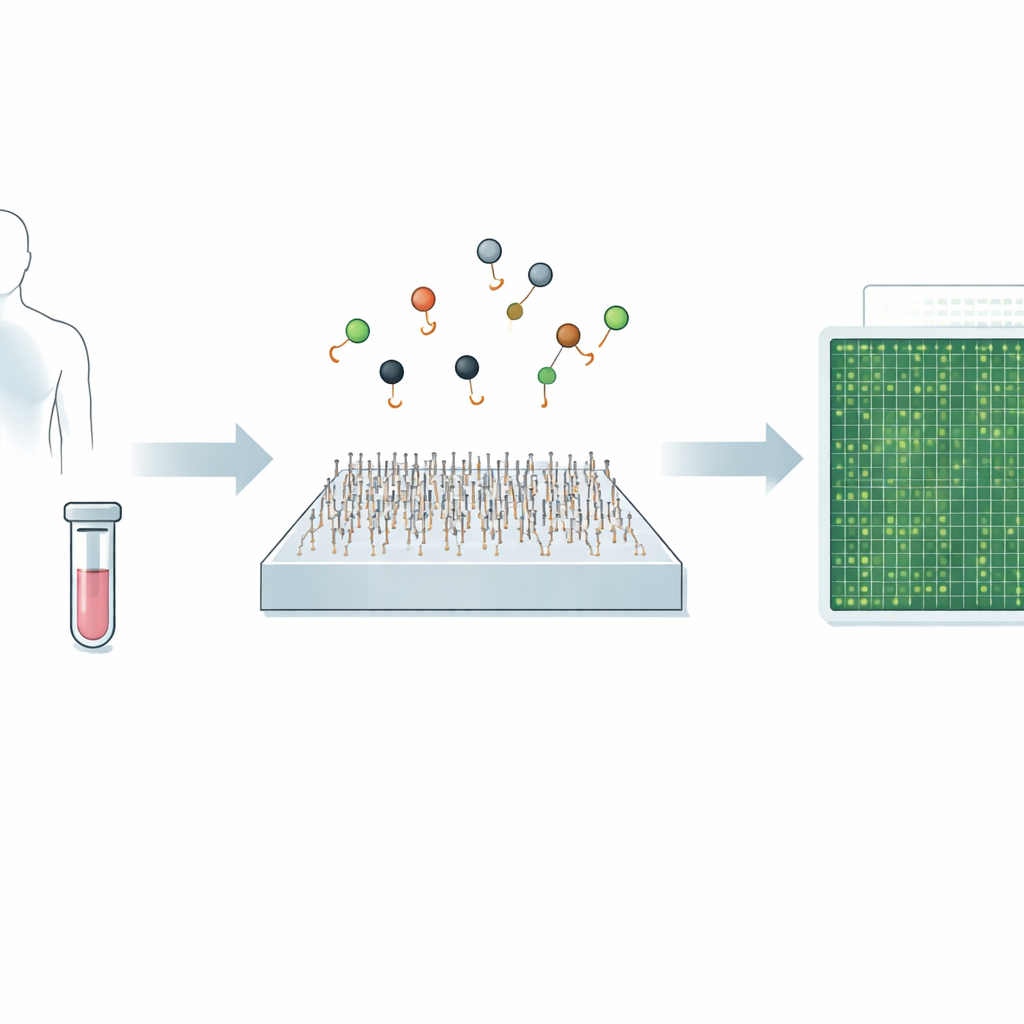
Uma nova maneira de ver mensagens genéticas minúsculas
O trabalho se concentra em microRNAs — pequenos trechos de RNA que ajudam a controlar o uso dos nossos genes e que estão fortemente ligados a muitos cânceres, doenças cardíacas, infecções e distúrbios cerebrais. Por serem tão curtos e frequentemente diferirem por apenas um ou dois blocos, métodos padrão como PCR e sequenciamento de nova geração podem ter dificuldades para separar tipos muito próximos, sobretudo quando estão em níveis muito baixos. Abordagens recentes de imageamento de única molécula melhoraram essa especificidade ao rastrear como sondas individuais se ligam e se desligam, mas ainda eram relativamente lentas, demorando cerca de dez minutos para analisar um único alvo.
Observando o piscar da luz para encontrar o alvo certo
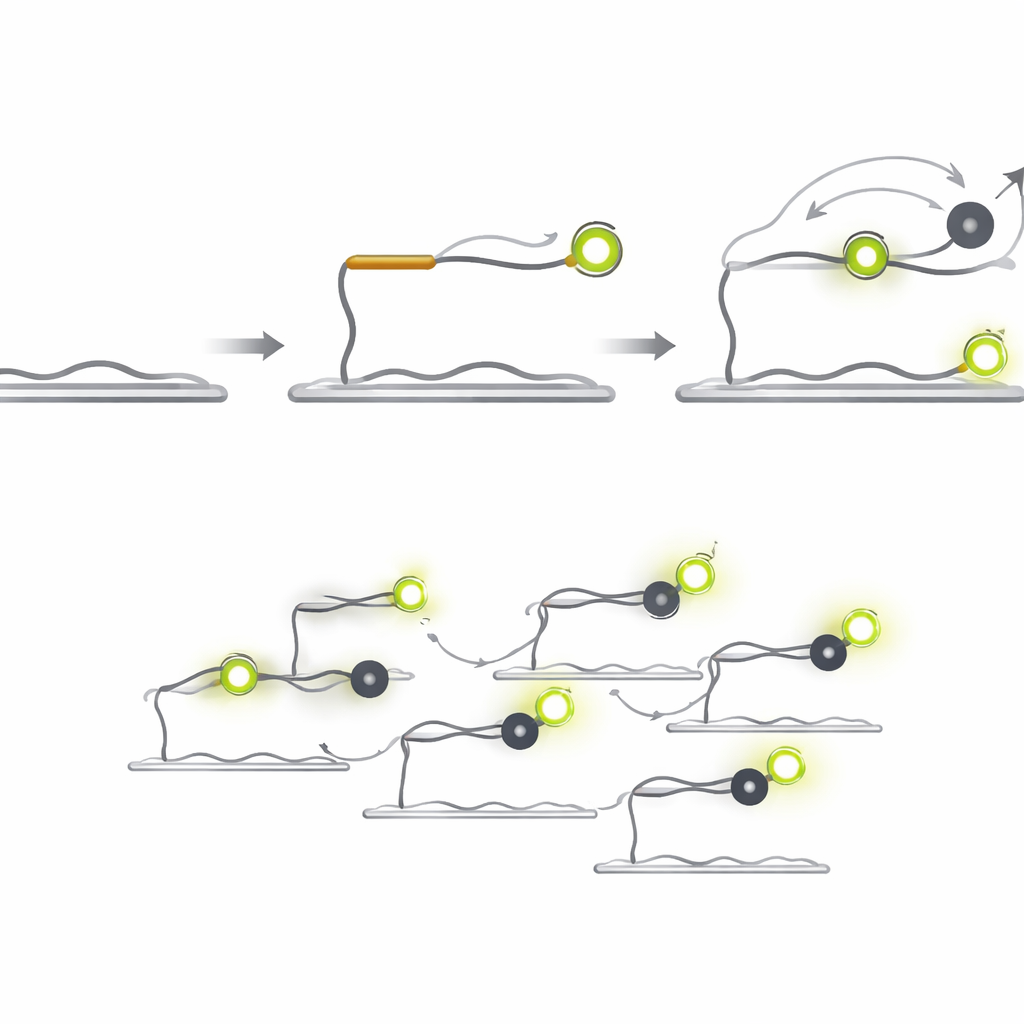
Q‑FISH inverte o problema ao explorar os breves piscos de luz de moléculas individuais. O método usa duas sondas de DNA curtas que reconhecem posições adjacentes em um microRNA alvo. Uma sonda carrega um corante fluorescente que brilha sob um laser, enquanto a outra traz um “quencher” que absorve a luz quando chega perto. A sonda fluorescente se liga ao alvo e permanece tempo suficiente para ser vista, ao passo que a sonda com quencher foi projetada para se ligar e desprender-se muito rapidamente. Cada vez que o quencher pousa próximo ao corante, a luz cai de repente; quando ele se afasta, a luz volta a subir. Registrando esses rápidos flashes de liga/desliga de moléculas individuais e analisando quanto tempo duram os períodos claros e escuros, o sistema pode decidir se há um alvo real presente.
De minutos para milissegundos
Como a sonda quencher não emite luz própria, ela pode ser usada em concentrações muito maiores do que sondas fluorescentes sem criar brilho de fundo. Encurtar a sonda quencher aumenta a rapidez com que ela se desprende, e elevar sua concentração aumenta a frequência com que ela pousa. Juntas, essas escolhas de projeto levam a um salto dramático na velocidade. Em testes com um microRNA relacionado ao câncer chamado let‑7a, o Q‑FISH alcançou mais de 70% da eficiência máxima de detecção em apenas um segundo de observação. Métodos comparáveis de única molécula precisaram de dezenas a centenas de segundos para atingir desempenho similar, tornando o Q‑FISH mais de 600 vezes mais rápido em termos práticos.
Separando sinais quase idênticos e medindo amostras reais
Os pesquisadores também demonstraram que o Q‑FISH consegue distinguir entre vários membros da família de microRNA let‑7, que compartilham quase a mesma sequência mas têm papéis diferentes no controle de genes ligados ao câncer. Eles usaram duas estratégias de multiplexação. Em uma, diferentes sondas quencher foram introduzidas uma após outra, cada uma ajustada para um microRNA ligeiramente diferente; em outra, as sondas foram marcadas com cores distintas e imageadas ao mesmo tempo. Em ambos os casos, a leitura dos padrões de piscar permitiu à equipe identificar corretamente qual microRNA era qual em cerca de um segundo. Por fim, aplicaram o método a RNA total extraído de tecidos humanos de fígado e pulmão. Ao adicionar quantidades conhecidas de microRNAs sintéticos e contar os pontos resultantes, construíram curvas de calibração e então determinaram os níveis naturais presentes nos tecidos, revelando diferenças claras entre órgãos.
O que isso pode significar para testes futuros
Em conjunto, o estudo mostra que o Q‑FISH pode identificar microRNAs específicos com altíssima precisão, mesmo quando são quase idênticos entre si, e pode fazê‑lo em velocidades que superam de longe métodos anteriores de única molécula. Embora os experimentos tenham sido realizados em amostras preparadas usando um microscópio especializado, a ideia subjacente — usar eventos rápidos de extinção de luz em vez de depender apenas de ligações lentas — pode ser adaptada a muitos tipos de marcadores genéticos, incluindo fragmentos de DNA tumoral no sangue. Com engenharia adicional e preparação de amostras simplificada, essa abordagem pode ajudar a aproximar diagnósticos moleculares rápidos, altamente multiplexados e extremamente sensíveis do uso clínico cotidiano.
Citação: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Palavras-chave: detecção de microRNA, imageamento de única molécula, diagnósticos moleculares, extinção de fluorescência, biópsia líquida