Clear Sky Science · pt
Uma estratégia em dois passos mediada por actina permite que Campylobacter jejuni promova agregação mitocondrial e homeostase de ferro, para sobrevivência e persistência intracelular
Por que essa pequena batalha dentro das células importa
O envenenamento alimentar por frango malcozido é frequentemente atribuído a uma bactéria chamada Campylobacter jejuni. A maioria das pessoas se recupera, mas esse micro-organismo é surpreendentemente apto a sobreviver em muitos ambientes, o que facilita sua disseminação da fazenda até o prato. Este estudo examina o que ocorre quando a bactéria se esconde dentro de uma ameba de vida livre — um microrganismo comum de água doce — e revela um truque de sobrevivência notavelmente sofisticado que gira em torno de remodelar o esqueleto interno da célula, agrupar os “pacotes de energia” chamados mitocôndrias e controlar o ferro e a química oxidativa prejudicial. Compreender essa fase oculta de seu ciclo de vida pode apontar para novas maneiras de reduzir a contaminação antes que a bactéria chegue às pessoas.
Um micróbio que treina dentro de amebas
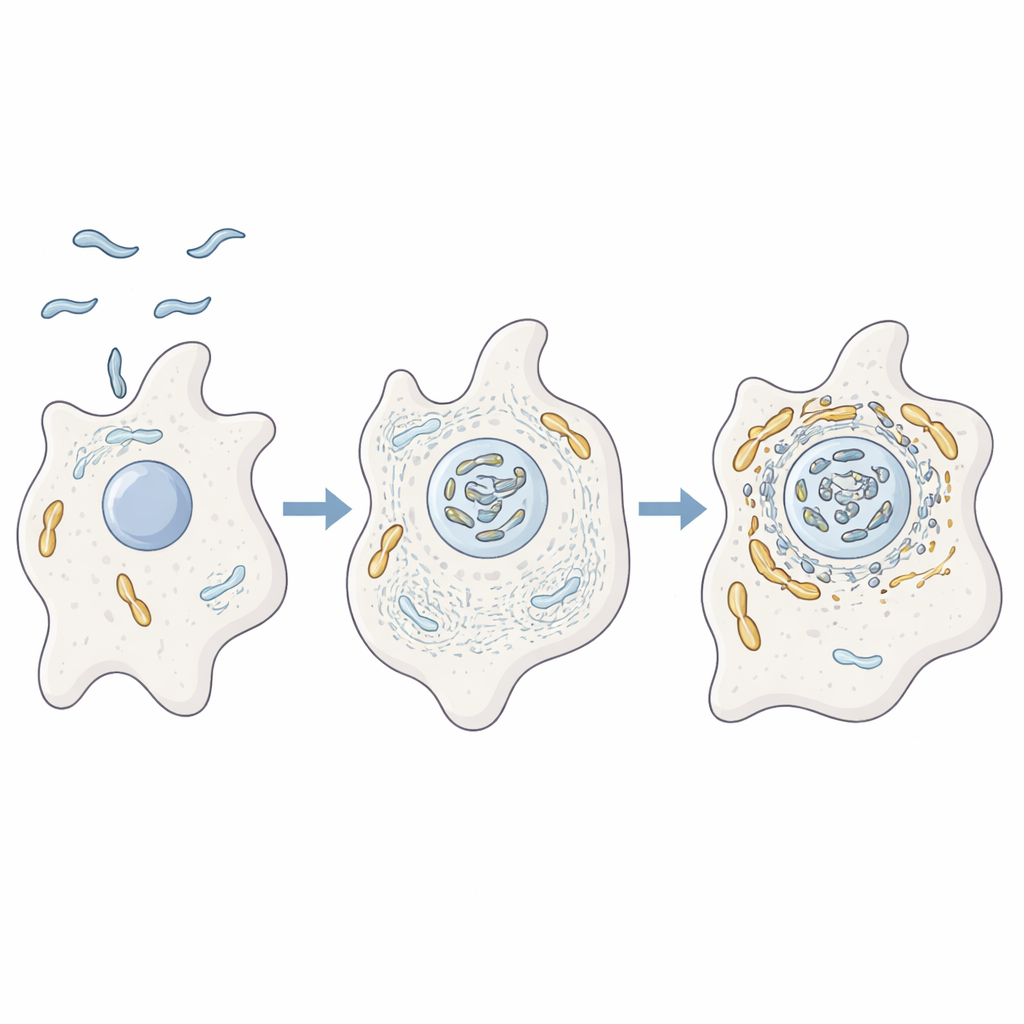
Os autores estudaram como C. jejuni se comporta dentro da ameba Acanthamoeba castellanii, um organismo unicelular que vive no solo e na água. Essas amebas funcionam como campos de treinamento para muitas bactérias causadoras de doenças, oferecendo proteção contra condições adversas e contra desinfetantes. Usando análise proteica avançada, microscopia e mutantes genéticos, os pesquisadores mostraram que, quando C. jejuni infecta amebas, ele fica associado de perto às mitocôndrias do hospedeiro. Ao mesmo tempo, o andaime interno da ameba feito de actina, junto com proteínas que regulam sua forma e movimento, apresenta forte enriquecimento perto dessas mitocôndrias, sugerindo que a bactéria está ativamente rearranjando a arquitetura interna da célula hospedeira.
Dobrar o esqueleto celular para mover os pacotes de energia
Para testar se a actina realmente dirige essa interação, a equipe bloqueou a formação de filamentos de actina ou seu ramificar em redes. Nessas condições, as mitocôndrias deixaram de se reunir perto das bactérias e permaneceram dispersas como pontos, e a sobrevivência bacteriana diminuiu. Em seguida, focaram em duas proteínas bacterianas auxiliares, CiaD e CiaI, que são injetadas nas células hospedeiras através do flagelo bacteriano, uma cauda em forma de chicote. CiaD aumentou o crescimento de actina e promoveu projeções pontiagudas na superfície da ameba, ajudando a célula a englobar as bactérias. Uma vez dentro, observou-se que as mitocôndrias se agrupavam ao redor do compartimento bacteriano de forma dependente de actina, posicionando a bactéria em uma zona privilegiada rica em maquinário energético do hospedeiro.
Um interruptor molecular que remodela mitocôndrias
Enquanto CiaD é chave para a entrada, CiaI controla o que acontece a seguir. Quando os pesquisadores deletaram o gene de CiaI, C. jejuni deixou de induzir forte agregação mitocondrial e sobreviveu mal dentro das amebas. Adicionar CiaI purificada ligada a pequenas esferas, sem qualquer bactéria viva, foi suficiente para causar fusão e aglomeração das mitocôndrias próximas e para remover localmente a actina. Testes bioquímicos mostraram que CiaI se liga a moléculas portadoras de energia de forma cooperativa, comportando-se como um interruptor molecular que pode ligar ou desligar sua atividade dependendo das condições dentro do hospedeiro. Os autores propõem que, depois que o crescimento de actina induzido por CiaD aproxima as mitocôndrias, CiaI promove a degradação local da actina e remodela a rede mitocondrial em agregados densos envolvendo o compartimento que contém a bactéria.
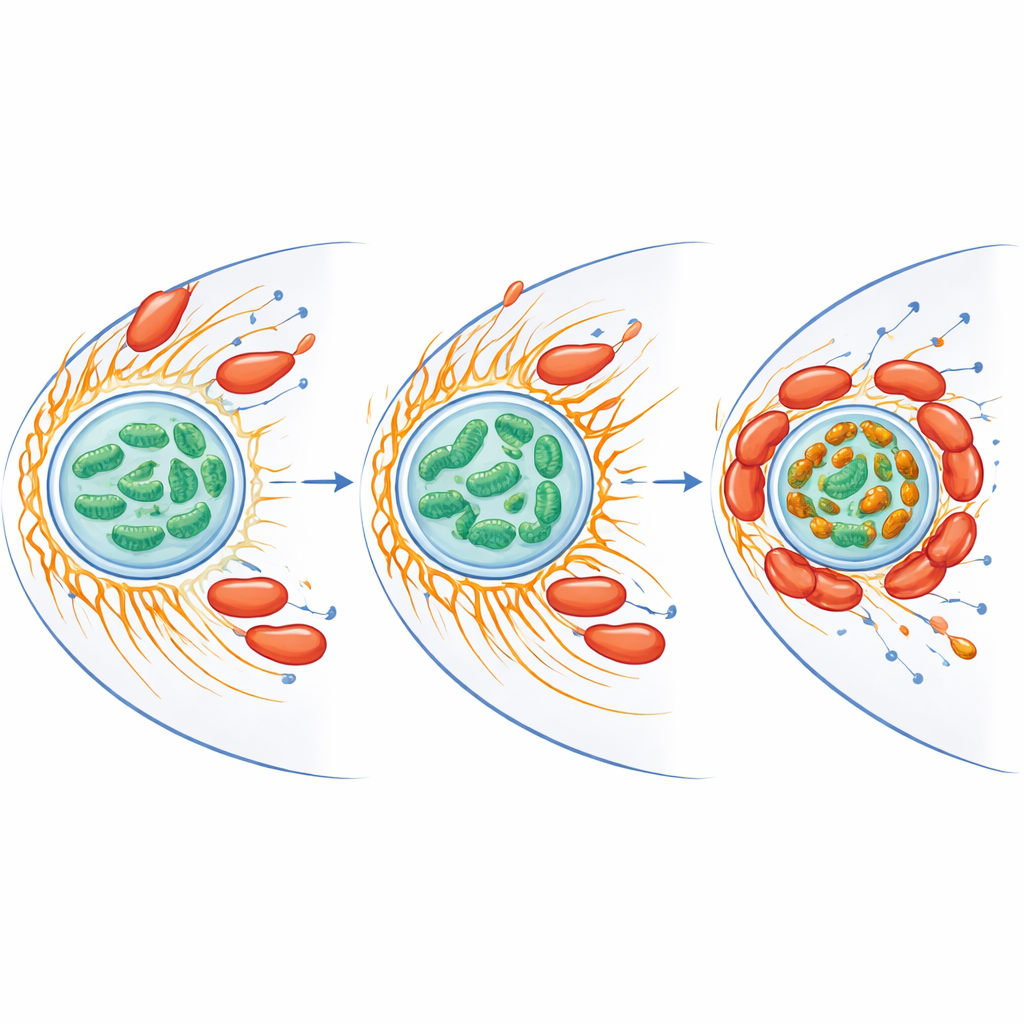
Reconfigurando o ferro e o estresse dentro da célula hospedeira
As mitocôndrias fazem mais do que produzir energia — elas também lidam com o ferro e produzem espécies reativas de oxigênio, formas quimicamente agressivas de oxigênio que podem matar micróbios. Os pesquisadores descobriram que a infecção reduziu o ferro livre geral dentro das mitocôndrias, mas, ao mesmo tempo, criou aglomerados brilhantes ricos em ferro onde as mitocôndrias se agrupavam ao redor das bactérias. Proteínas envolvidas no manejo do ferro e na defesa contra estresse oxidativo aumentaram tanto no hospedeiro quanto na bactéria. Quando a equipe removeu o ferro livre usando um agente quelante, o estouro de espécies reativas de oxigênio da ameba caiu e a sobrevivência de C. jejuni aumentou dramaticamente. Mitocôndrias em células infectadas também exibiram um potencial de membrana mais alto, um sinal de atividade elevada, sugerindo que a bactéria impulsiona os pacotes de energia do hospedeiro para um estado que favorece sua própria persistência enquanto limita a química oxidativa danosa.
O que isso significa para segurança alimentar e infecção
Em conjunto, os resultados suportam uma estratégia em dois passos: primeiro, CiaD estimula o crescimento de actina para ajudar a bactéria a entrar nas amebas e a atrair mitocôndrias para o sítio de entrada; segundo, CiaI desmonta localmente a actina e remodela as mitocôndrias em aglomerados ricos em ferro envolvendo o compartimento bacteriano, ao mesmo tempo em que atenua as defesas oxidativas do hospedeiro. Esse controle finamente ajustado da forma celular, uso de energia e balanço metálico ajuda C. jejuni a sobreviver dentro das amebas e provavelmente contribui para sua capacidade de persistir no ambiente e depois infectar humanos. Ao revelar os jogadores-chave nessa disputa microscópica, o estudo aponta para novos alvos — como as proteínas Cia, os contatos actina-mitocôndria ou as vias de manejo do ferro — que poderiam ser interrompidos para reduzir contaminação e doenças.
Citação: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Palavras-chave: Campylobacter, amebas, mitocôndrias, citoesqueleto de actina, homeostase do ferro