Clear Sky Science · pt
Regulação em múltiplas camadas dos receptores kainato GluK3 é mediada por subunidades Neto e zinco
Por que interruptores minúsculos do cérebro importam
Cada pensamento, memória e estado de ânimo no cérebro depende de interruptores microscópicos que permitem a entrada e saída de partículas carregadas nas células nervosas. Este estudo concentra‑se em um desses interruptores, um receptor pouco conhecido chamado GluK3. Ao revelar como proteínas parceiras e íons de zinco afinam o comportamento do GluK3, o trabalho oferece pistas sobre como os circuitos cerebrais mantêm o equilíbrio — e como esse equilíbrio pode se deslocar em transtornos como epilepsia, depressão e esquizofrenia.
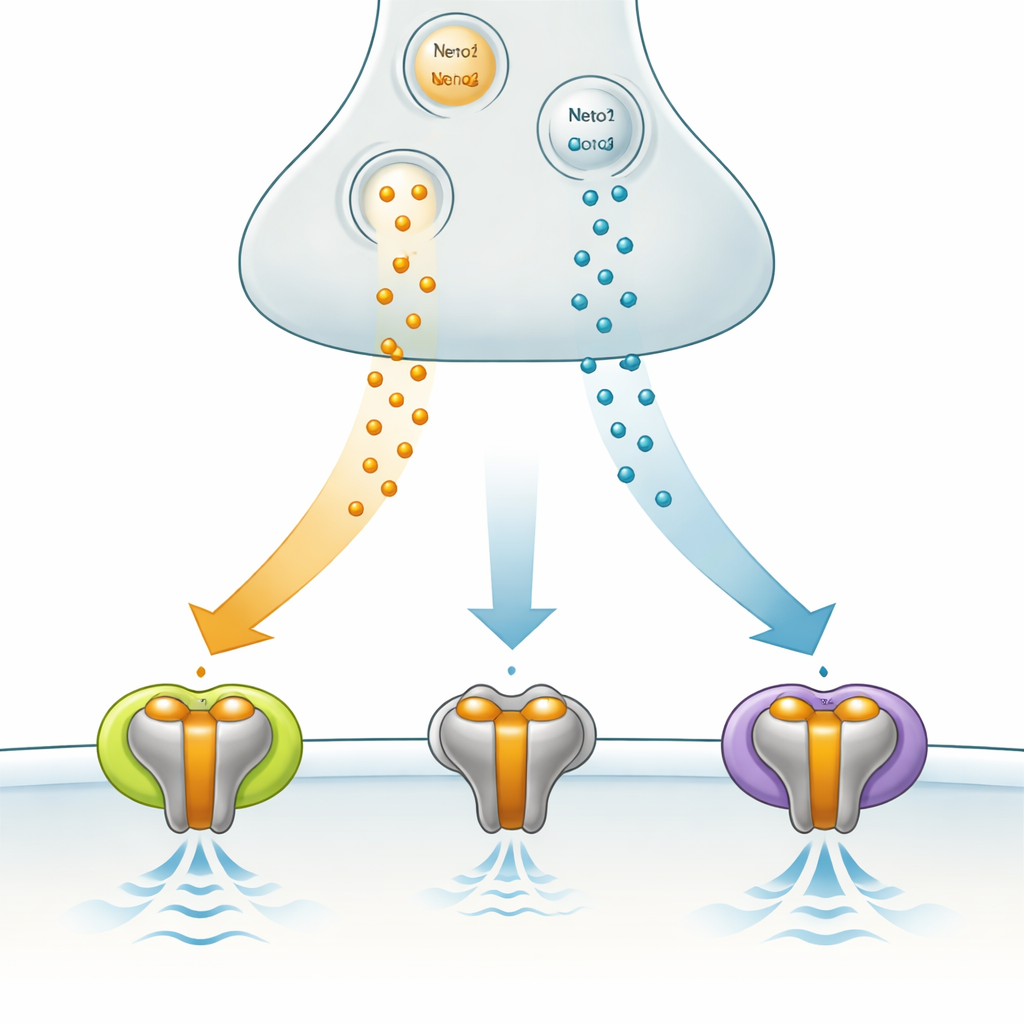
Uma portinha de sinal especializada no cérebro
GluK3 pertence à família dos receptores kainato, parte do grupo maior dos receptores de glutamato que mediam a comunicação rápida entre neurônios. Diferentemente de alguns de seus parentes, GluK3 não simplesmente liga ou desliga sinais; age mais como um filtro que responde melhor a rajadas breves e intensas do mensageiro químico glutamato. Está enriquecido em regiões do cérebro como o hipocampo, crucial para memória e para a padronização de ritmos de rede, e alterações na função do GluK3 têm sido associadas a comportamentos relacionados à ansiedade. Essas características tornam o GluK3 um alvo promissor, porém ainda pouco compreendido, para modular a atividade cerebral em saúde e doença.
Proteínas auxiliares que puxam as cordas
A equipe examinou como duas proteínas auxiliares, Neto1 e Neto2, alteram o comportamento do GluK3 em células humanas geneticamente modificadas para produzir esses componentes. Ambas as auxiliares retardaram a velocidade com que o GluK3 se fecha após ser ativado e reduziram uma forma natural de bloqueio interno que normalmente limita o fluxo de corrente. No entanto, tiveram efeitos opostos na rapidez com que o GluK3 pode ser reutilizado. Com Neto1, os receptores se recuperaram rapidamente, prontos para responder a sinais rápidos e repetidos. Com Neto2, a recuperação tornou‑se muito mais lenta, favorecendo a integração de sinais ao longo de intervalos maiores. Em essência, ao escolher diferentes proteínas auxiliares, uma sinapse pode decidir se o GluK3 se comporta como um detector de disparo rápido ou como um sensor mais lento e de média.
Zinco como uma segunda camada de controle
Muitos terminais nervosos que liberam glutamato também liberam zinco, que pode se ligar aos receptores e alterar seu funcionamento. Trabalhos anteriores mostraram que o zinco aumenta de forma incomum a atividade do GluK3, ao passo que tende a atenuar outros tipos de receptor. Aqui, os autores descobriram que esse aumento depende fortemente de qual proteína Neto está presente. Quando o GluK3 atua sozinho, o zinco aproximadamente dobra o tempo em que o receptor permanece ativo e aumenta modestamente a corrente. A adição de Neto1 reduz esse efeito. Por contraste, quando o GluK3 se associa ao Neto2, zinco e Neto2 atuam em conjunto para amplificar muito a corrente, bem mais do que qualquer um deles isoladamente. Isso sugere que sinapses ricas em Neto2 e zinco podem amplificar fortemente sinais mediados por GluK3 durante atividade intensa, enquanto sinapses ricas em Neto1 permanecem mais contidas.
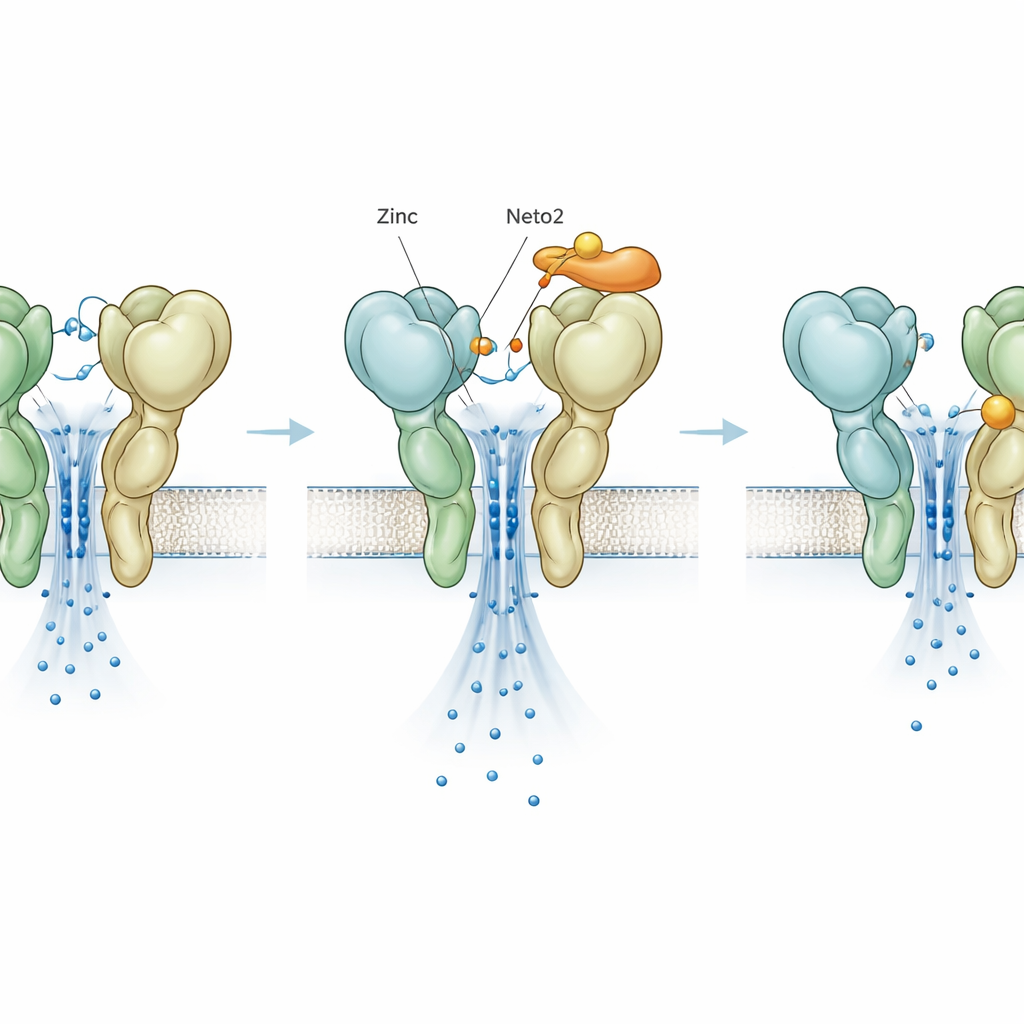
Um freio oculto revelado por mutação
Para separar as ações do zinco daquelas das proteínas auxiliares, os pesquisadores criaram uma alteração de uma única letra no GluK3, chamada D759G, que remove um sítio conhecido de ligação ao zinco. Como esperado, essa mutação por si só tornou o receptor mais estável e mais lento para se desligar, imitando o efeito habitual do zinco. Surpreendentemente, quando o zinco foi adicionado a esse mutante, ele deixou de aumentar a atividade; em vez disso, acelerou o desligamento e reduziu a corrente, revelando um segundo sítio de zinco previamente oculto que age como um freio. Neto1 e Neto2 ainda exerceram seus efeitos característicos sobre o mutante, mostrando que sua influência central não depende do sítio original de zinco. Ainda assim, essa ação inibitória de zinco agora descoberta foi modulada de modo diferente pelas duas auxiliares, adicionando mais um botão ajustável ao sistema.
Vendo estrutura por trás do comportamento
Para conectar função e forma, a equipe usou microscopia crioeletrônica para visualizar o receptor GluK3 mutante congelado em um estado não ativado. As imagens revelaram que a região que se liga ao glutamato forma uma unidade mais compacta e densamente empacotada no mutante D759G em comparação com o GluK3 normal. Esse aperto estrutural provavelmente torna mais difícil para o receptor assumir uma conformação de desligamento, explicando por que o mutante, como o GluK3 ligado ao zinco, permanece ativo por mais tempo. Ao mesmo tempo, as imagens mostraram que nem todas as partes do receptor estavam travadas em uma única disposição, apontando para uma arquitetura intrinsecamente flexível que é especialmente sensível a pequenos estímulos químicos.
O que isso significa para a saúde do cérebro
Tomado em conjunto, o estudo retrata o GluK3 não como um simples interruptor liga‑desliga, mas como um hub finamente ajustável onde glutamato, proteínas auxiliares e zinco convergem. Neto1 e Neto2 definem quão rápido os sinais se apagam e com que rapidez os receptores podem responder novamente, enquanto o zinco pode tanto potencializar quanto, em certas condições, restringir a atividade por meio de múltiplos sítios de ligação. Como GluK3, proteínas Neto e zinco coexistem em sinapses envolvidas na memória e estão implicados em epilepsia e condições psiquiátricas, compreender esse controle em múltiplas camadas pode orientar terapias futuras que reajustem suavemente a sinalização sináptica em vez de suprimi‑la por completo.
Citação: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Palavras-chave: receptores kainato, GluK3, proteínas Neto, zinco sináptico, plasticidade sináptica