Clear Sky Science · pt
Abuso de drogas viciantes e depressão — um foco na epigenética
Por que esta pesquisa importa na vida cotidiana
Drogas viciantes e depressão costumam ser tratadas como problemas distintos, mas frequentemente ocorrem juntas na mesma pessoa. Esta revisão explica como o uso prolongado de substâncias como metanfetamina, cocaína, opioides e cannabis pode deixar “cicatrizes moleculares” duradouras no cérebro que aumentam o risco de depressão. Ao desvendar essas alterações ocultas, o artigo aponta para futuros testes que poderiam identificar quem é mais vulnerável — e para tratamentos mais precisos que talvez revertam o dano em vez de apenas mascarar os sintomas.
Como dependência e baixo ânimo se entrelaçam
Os autores começam delineando a estreita ligação clínica entre abuso de drogas e depressão. Pessoas que usam substâncias viciantes repetidamente têm muito mais probabilidade de relatar tristeza persistente, perda de prazer, problemas de sono e pensamentos suicidas. Regiões cerebrais que controlam recompensa, motivação, memória e tomada de decisões — a área tegmentar ventral, o núcleo accumbens, o córtex pré-frontal e o hipocampo — são centrais em ambas as condições. A exposição crônica a drogas perturba neurotransmissores como dopamina e serotonina, hormônios do estresse controlados pelo eixo hipotálamo–hipófise–adrenal, sinais do sistema imune e o suprimento de energia dos neurônios. Juntas, essas alterações tornam o cérebro menos resiliente ao estresse e mais propenso a estados depressivos, mesmo muito tempo após a última dose.
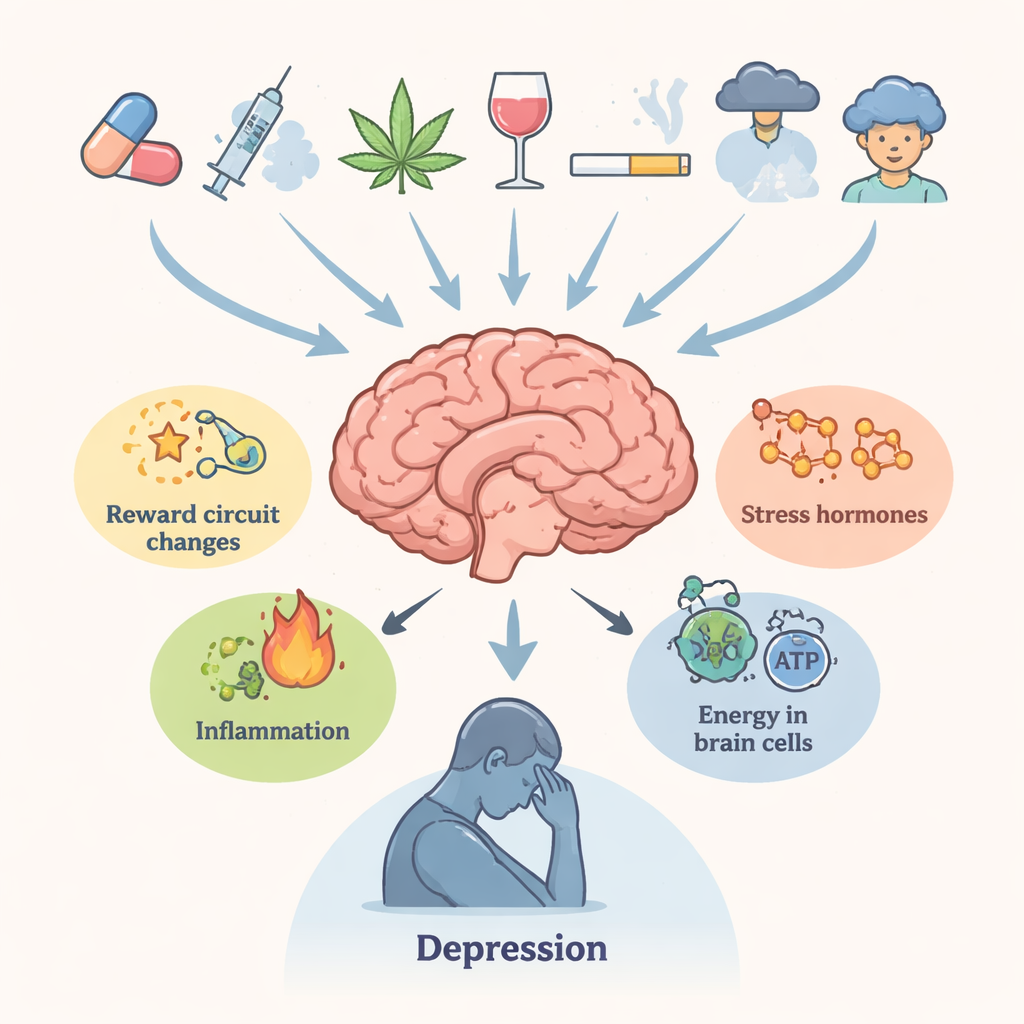
Drogas que remodelam a química do cérebro
A revisão percorre várias classes principais de drogas. Estimulantes do tipo anfetamina e seus análogos, incluindo os sintéticos chamados “bath salts”, provocam grandes surtos de dopamina e outros transmissores que, ao longo do tempo, danificam terminações nervosas, desequilibram o glutamato, sobrecarregam o retículo endoplasmático e empurram as células para formas prejudiciais de autodigestão (autofagia). O uso de cannabis na adolescência está ligado à depressão posterior e ao risco de suicídio, provavelmente por meio de alterações duradouras em receptores canabinoides, na estrutura da substância branca e na sensibilidade dos circuitos de dopamina. Opioides, embora aliviem a dor, podem desencadear inflamação, falha mitocondrial e redução de sinais de apoio ao crescimento como o fator neurotrófico derivado do cérebro (BDNF). A cocaína ativa repetidamente o sistema de estresse e altera reguladores-chave como FKBP5, contribuindo para ansiedade e baixo ânimo durante a abstinência. Em cada caso, as perturbações biológicas tendem a persistir, ajudando a explicar por que os sintomas emocionais podem durar além da intoxicação evidente.
Epigenética: a memória da exposição
Para entender por que os efeitos das drogas perduram, os autores concentram-se na epigenética — marcas químicas e interruptores moleculares que ajustam a atividade gênica sem alterar as letras do DNA. Drogas viciantes modificam a metilação do DNA (uma marca nas bases de citosina), mudam grupos químicos nas histonas que empacotam o DNA e alteram RNAs não codificantes que afinam quais proteínas são produzidas. Por exemplo, metanfetamina e cocaína deslocam padrões de metilação em regiões cerebrais relacionadas à recompensa, alterando os níveis de enzimas que adicionam ou removem essas marcas. Opioides e estimulantes remodelam a acetilação e metilação das histonas em genes que controlam receptores de glutamato, sinalização de estresse e estrutura sináptica. Dezenas de microRNAs, RNAs longos não codificantes e RNAs circulares aumentam ou diminuem com a exposição às drogas, influenciando coletivamente inflamação, crescimento neuronal e a força das sinapses. Essas alterações epigenéticas atuam como uma “memória” molecular do histórico de uso de drogas.
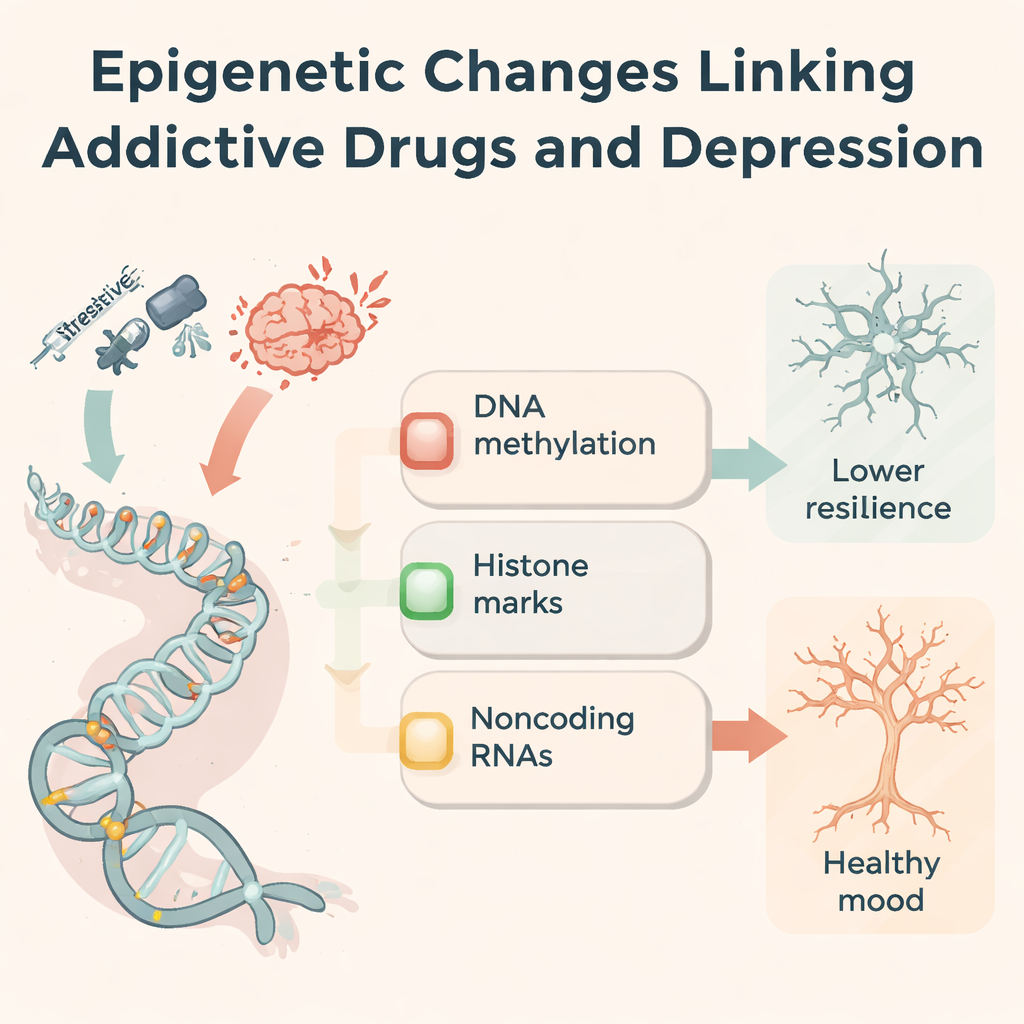
Vias moleculares compartilhadas na depressão e na dependência
A mesma maquinaria epigenética também aparece em pessoas e animais com depressão que nunca usaram drogas. Experiências estressantes podem alterar a metilação de receptores de hormônios do estresse (como NR3C1 e FKBP5), reduzir fatores de crescimento benéficos como o BDNF e reconfigurar vias imunes e de glutamato. Muitos dos mesmos RNAs não codificantes alterados por drogas também estão desregulados na depressão, afetando como novos neurônios nascem, como a microglia responde à inflamação e quão fortes são as conexões sinápticas. Os autores propõem um quadro em três partes: regulação da resposta ao estresse, remodelamento dos circuitos de recompensa e plasticidade sináptica. Ao longo desses eixos, dependência e depressão convergem repetidamente em um pequeno conjunto de genes e marcas, sugerindo uma razão biológica para a frequente coocorrência dos dois transtornos.
O que isso significa para prevenção e tratamento futuros
Para concluir, a revisão argumenta que mudanças epigenéticas poderiam se tornar biomarcadores de alerta precoce e alvos para tratamentos de nova geração. Fármacos de ação ampla que removem marcas epigenéticas já mostraram alguns efeitos semelhantes a antidepressivos em animais, mas são muito imprecisos para uso humano rotineiro. Novas ferramentas — como editores do epigenoma baseados em CRISPR e terapias que modulam microRNAs ou RNAs longos específicos — podem um dia ajustar genes problemáticos em células cerebrais particulares enquanto poupam outras. Os autores alertam que a maior parte dos dados atuais vem de roedores e de tecido cerebral em massa, e que a biologia humana é mais complexa. Ainda assim, ao revelar como drogas viciantes e depressão escrevem no mesmo “caderno” molecular, este trabalho oferece um caminho esperançoso rumo a terapias mais personalizadas e duradouras.
Citação: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Palavras-chave: dependência e depressão, epigenética, abuso de drogas, metilação do DNA, RNA não codificante