Clear Sky Science · pt
Heterogeneidade entre neurônios VIP e GRP sustenta a sinalização do receptor AVP no núcleo supraquiasmático de camundongos
Por que nosso relógio biológico é tão difícil de reajustar
Quem já saiu de um voo longo desorientado ou sofreu com turnos noturnos sabe que nosso relógio interno não gosta de mudanças bruscas de horário. Este artigo investiga uma pergunta bem específica no cerne desse problema: dentro do relógio mestre do cérebro, por que algumas células nervosas sentem fortemente um sinal de tempo enquanto suas vizinhas em grande parte o ignoram? Ao rastrear um único sinal químico por esse pequeno circuito relógio em camundongos, os autores revelam um subgrupo oculto de células que ajudam a determinar quão teimoso nosso relógio biológico é quando enfrenta o “jet lag”. 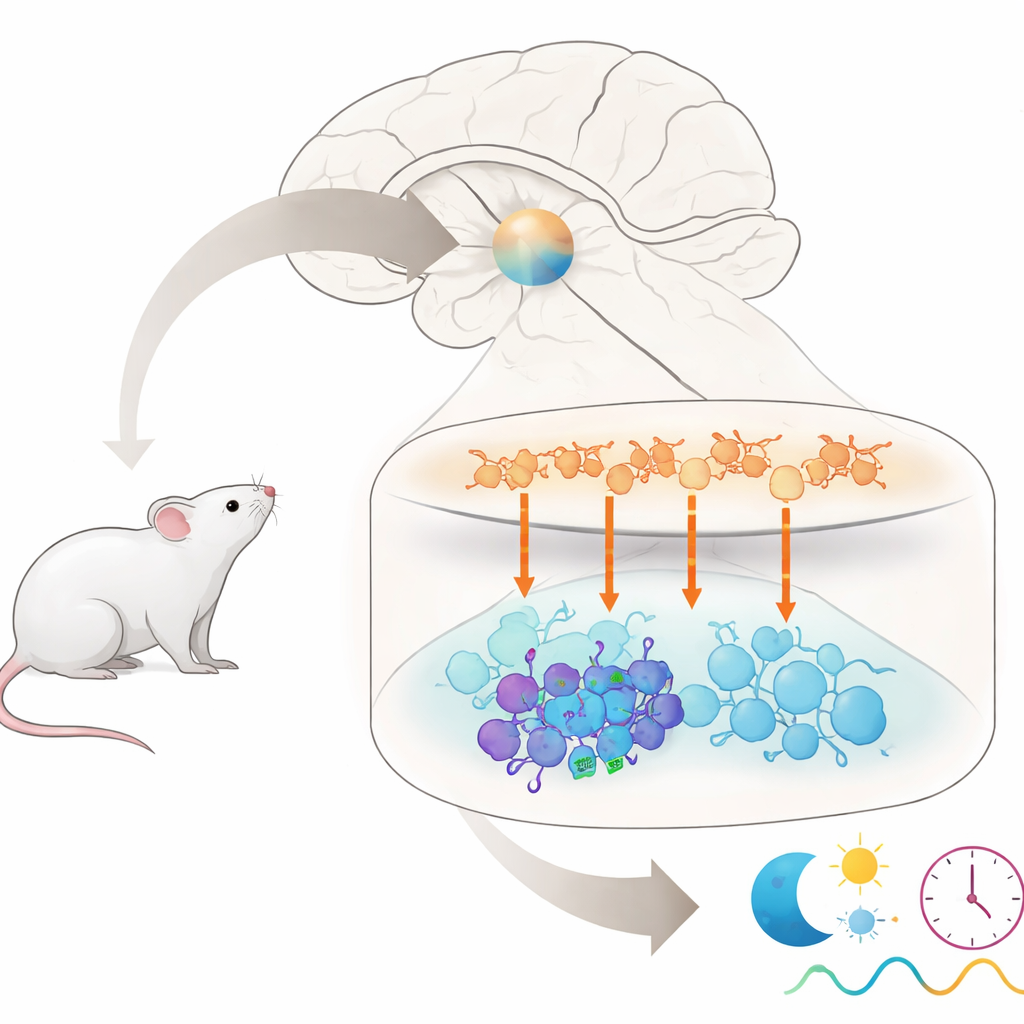
Um relógio minúsculo com muitos participantes diferentes
O relógio mestre em mamíferos fica em uma pequena região do cérebro chamada núcleo supraquiasmático, ou NSQ. Embora contenha apenas cerca de 20 mil neurônios, é composto por vários grupos distintos que se comunicam usando mensageiros químicos diferentes. Células na região superior, a “casca”, liberam principalmente um mensageiro chamado arginina vasopressina (AVP), enquanto células na região inferior, o “núcleo”, costumam liberar outros mensageiros, incluindo o peptídeo intestinal vasoativo (VIP) e o peptídeo liberador de gastrina (GRP). Juntos, esses grupos devem permanecer sincronizados para gerar os ritmos de 24 horas que governam sono, liberação hormonal e muitas outras funções do corpo. Mas quais exatamente células no núcleo escutam sinais das células AVP da casca ainda não estava claro.
Seguindo a conexão do emissor ao receptor
Os pesquisadores primeiro mapearam como células AVP da casca se conectam fisicamente a células VIP e GRP no núcleo. Eles usaram um vírus para marcar as fibras de saída e potenciais pontos de contato dos neurônios AVP em camundongos e, em seguida, coraram fatias cerebrais para ver onde essas fibras terminavam. Descobriram que as fibras AVP formavam aparentes pontos de contato tanto em células VIP quanto em células GRP, porém em proporções diferentes: aproximadamente um quarto das células VIP e mais da metade das células GRP exibiam essas aposições. Isso mostrou que neurônios AVP alcançam ambos os tipos de células do núcleo, mas ainda não revelou quais realmente respondem ao sinal. Para testar isso, a equipe usou optogenética—ativando neurônios AVP com luz azul—e procurou c-Fos, um marcador de ativação celular, em neurônios VIP e GRP.
Um pequeno subgrupo de VIP que realmente “ouve” AVP
Quando os neurônios AVP foram estimulados pela luz, muitas células AVP ativaram c-Fos, como esperado. Importante, um pequeno subconjunto de células VIP no núcleo também apresentou ativação de c-Fos, mesmo não expressando diretamente a proteína sensível à luz. Isso indicou que eram ativadas indiretamente pela entrada AVP. Em contraste, células GRP raramente mostraram c-Fos, apesar de receberem contatos AVP. Os autores então procuraram a mensagem gênica do receptor de AVP conhecido como V1a nessas populações usando métodos sensíveis de imagem de RNA. Descobriram que V1a estava presente apenas em uma minoria das células VIP e era quase indetectável nas células GRP. Assim, entre os muitos neurônios VIP, um pequeno subgrupo V1a-positivo parece especialmente sintonizado para receber e responder aos sinais de AVP, enquanto a maioria das células GRP não o é. 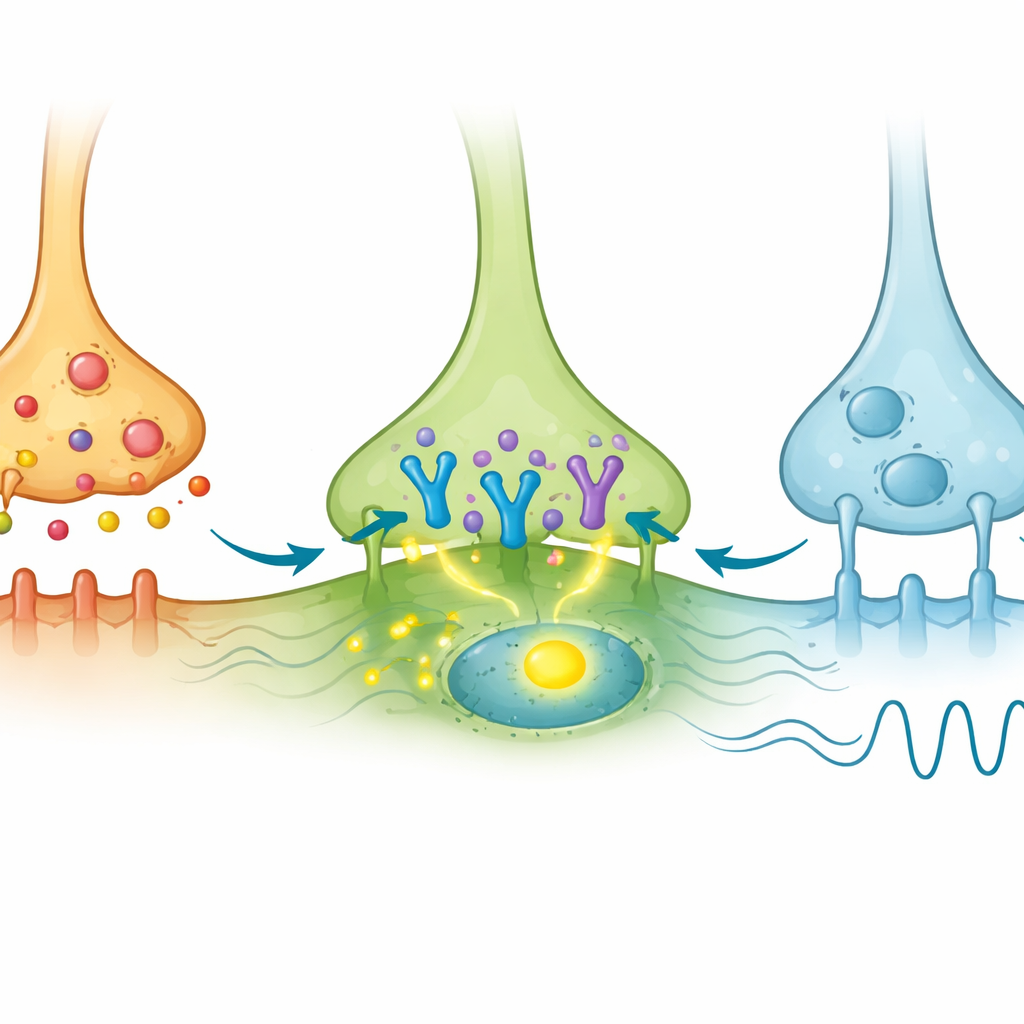
Como um pequeno grupo celular molda a recuperação do jet lag
Para sondar a função desses neurônios VIP portadores de V1a, os pesquisadores criaram camundongos nos quais o receptor V1a foi removido apenas das células VIP. Esses animais mantiveram um comprimento de ritmo diário normal em escuridão constante, mostrando que esse receptor em neurônios VIP não é necessário para definir o ritmo básico do relógio. Contudo, quando o ciclo claro–escuro foi subitamente adiantado ou atrasado em oito horas para mimetizar jet lag, os camundongos modificados ajustaram seus padrões de atividade mais rapidamente do que seus parentes normais, especialmente após adiantamentos e em machos. Em outros experimentos, deletar V1a por todo o cérebro ou especificamente no NSQ produziu comportamento similar de “resistência ao jet lag”. Os novos resultados sugerem, portanto, que um grupo surpreendentemente pequeno de neurônios VIP que carregam receptores V1a pode ter uma influência desproporcional sobre o quão rígido ou flexível o relógio global é.
O que isso significa para nossa noção de tempo
Em termos práticos, este estudo mostra que, dentro do relógio central do cérebro, neurônios produtores de AVP atuam como cronometradores em um nível superior, enviando sinais por meio de receptores V1a a um conjunto seleto de neurônios VIP no nível inferior. Essas poucas células VIP ajudam toda a rede a resistir a mudanças súbitas no ciclo claro–escuro, desacelerando a velocidade com que o relógio se reajusta após uma mudança. Remover seu receptor sensível à AVP torna o sistema mais disposto a se deslocar, facilitando ajustes tipo jet lag em camundongos. Ao mapear essa diversidade oculta entre neurônios do relógio, o trabalho oferece um diagrama de conexão mais detalhado de como nossa sensação interna de tempo é estabilizada—e sugere que modular seletivamente vias semelhantes em humanos pode um dia ajudar a gerir jet lag ou outros distúrbios rítmicos.
Citação: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Palavras-chave: relógio circadiano, núcleo supraquiasmático, sinalização de vasopressina, neurônios VIP, jet lag