Clear Sky Science · pt
Proteína codificada pelo vírus da peste suína africana MGF 505–3R prejudica a imunidade inata via degradação de MyD88 mediada por ubiquitina
Por que isso importa para a saúde animal e além
A peste suína africana devastou granjas de porcos ao redor do mundo, ameaçando o abastecimento de alimentos e causando enormes perdas econômicas. O vírus responsável é letal em parte porque consegue escapar dos sistemas de alerta precoces do organismo. Este estudo revela como uma proteína viral, chamada MGF 505–3R, sabota discretamente um interruptor de alarme chave dentro das células e mostra que um pequeno fragmento dessa proteína também pode ser transformado em uma ferramenta anti-inflamatória poderosa em camundongos.
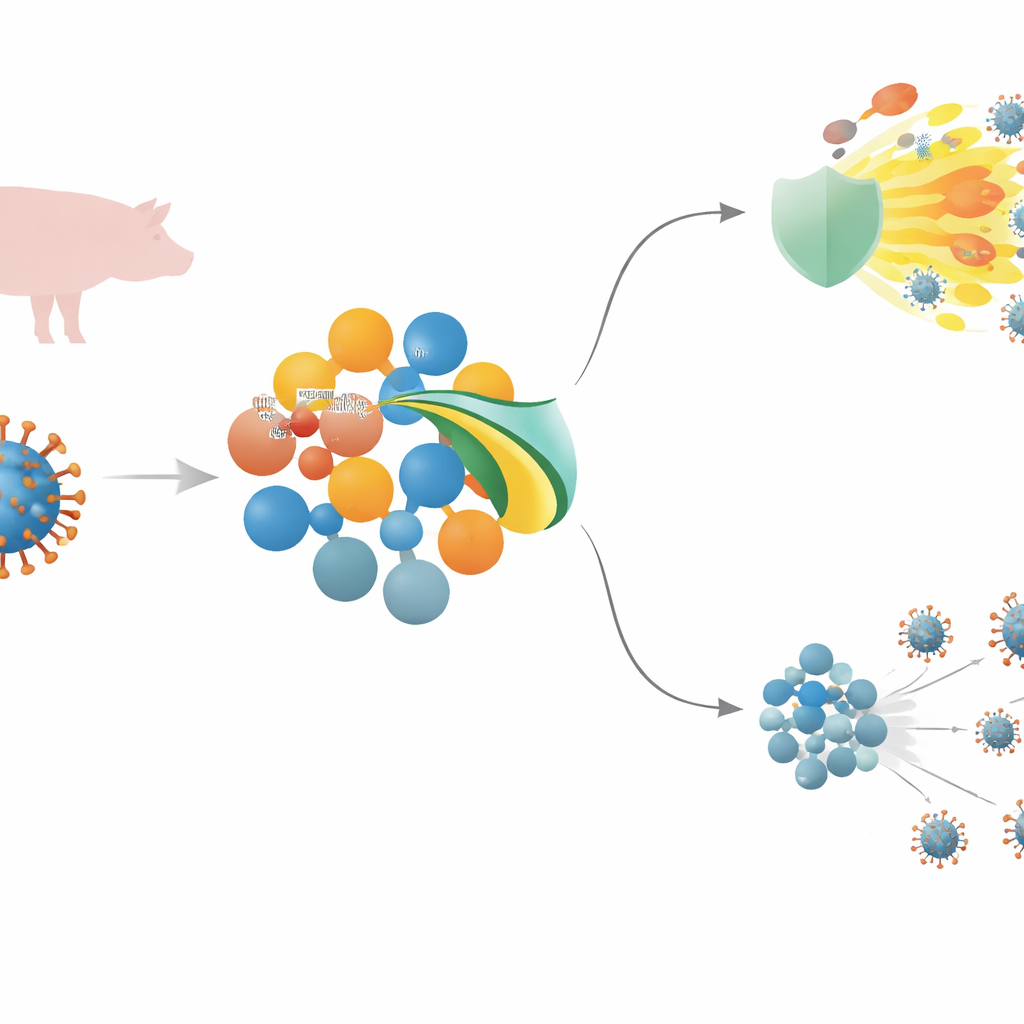
Um vírus letal para suínos e a primeira linha de defesa do organismo
O vírus da peste suína africana (ASFV) é um grande vírus de DNA que pode matar quase todos os porcos infectados. Para se estabelecer, ele precisa enganar a imunidade inata — a defesa rápida e de linha de frente que detecta invasores e desencadeia inflamação e moléculas antivirais. Central nessa resposta está uma cadeia de sinalização que inclui sensores na superfície celular, uma proteína de retransmissão chamada MyD88 e um interruptor mestre conhecido como NF–κB, que juntos impulsionam a produção de mensageiros inflamatórios e interferons antivirais. O ASFV carrega muitos genes que se acredita interferirem nesses sinais, mas para vários deles, incluindo MGF 505–3R, seus truques exatos não eram bem compreendidos.
Como o vírus corta os fios do alarme imunológico
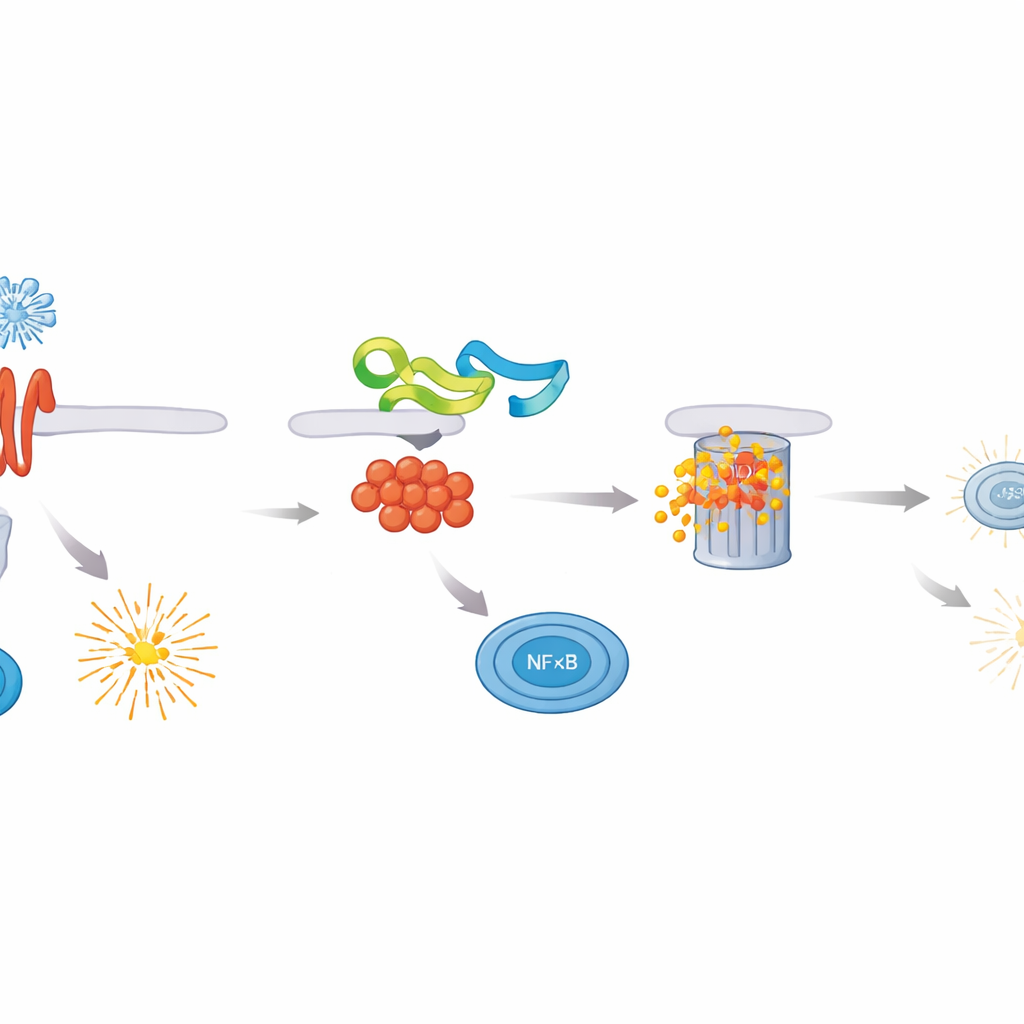
Os pesquisadores triaram proteínas do ASFV quanto à capacidade de atenuar a atividade de NF–κB e descobriram que MGF 505–3R era um inibidor particularmente potente. Quando essa proteína viral estava presente, células expostas a diferentes gatilhos imunes produziram muito menos citocinas inflamatórias e níveis muito mais baixos de interferons tipo I e tipo III. Uma inspeção mais detalhada mostrou que MGF 505–3R age diretamente sobre MyD88, o adaptador central que conecta muitos sensores imunológicos ao NF–κB. MGF 505–3R se liga a MyD88 e o marca para eliminação pelo maquinário de degradação proteica da célula, usando uma forma de marcação chamada ubiquitinação ligada a K48. À medida que MyD88 é degradado, o NF–κB deixa de translocar para o núcleo e ativar genes protetores, deixando as células mais permissivas ao crescimento viral.
Aproximando-se de um fragmento pequeno, mas poderoso
Para localizar a parte crucial de MGF 505–3R, a equipe criou versões encurtadas da proteína e testou seus efeitos. Descobriram que os aminoácidos 89–277 eram necessários e suficientes para se ligar a MyD88, promover sua ubiquitinação e bloquear a ativação do NF–κB. Guiados por previsões computacionais da estrutura proteica, isolaram dois pequenos peptídeos dessa região. Um deles, pep3R–1, destacou-se: reduziu fortemente a atividade do NF–κB, bloqueou a fosforilação e a translocação nuclear da subunidade p65 do NF–κB e diminuiu a expressão de citocinas inflamatórias e interferons em células imunes estimuladas com múltiplos sinais de perigo. Em cultura celular, tanto a MGF 505–3R em comprimento total quanto pep3R–1 não só atenuaram a sinalização antiviral como também permitiram que um vírus de teste se replicasse com mais eficiência, enfatizando quão potente é essa via para controlar infecções.
Transformando um truque viral em um potencial medicamento
A equipe então investigou se o peptídeo poderia ser aproveitado para acalmar inflamação prejudicial em vez de ajudar vírus. Em um modelo murino de colite desencadeada por um químico chamado DSS, os animais normalmente perdem peso, desenvolvem diarreia com sangue e apresentam danos severos e infiltração de células imunes no cólon. Camundongos tratados com pep3R–1 se saíram muito melhor: os escores de doença foram mais baixos, os cólons estavam mais longos e saudáveis, e o exame microscópico revelou estrutura tecidual preservada com muito menos células inflamatórias. Os níveis de moléculas inflamatórias chave como TNF–α, IL–1β, IL–6 e de uma enzima associada ao influxo de leucócitos foram todos reduzidos no tecido do cólon e no sangue. Em um experimento separado, pep3R–1 também atenuou a resposta inflamatória a uma toxina bacteriana sistêmica, indicando que pode reduzir tanto tempestades inflamatórias locais quanto sistêmicas.
O que isso significa para porcos, pessoas e tratamentos futuros
Este trabalho mostra que a proteína do ASFV MGF 505–3R ajuda o vírus a prosperar ao desmontar um retransmissor imune central, MyD88, suprimindo assim tanto as defesas inflamatórias quanto as de interferon. Ao mesmo tempo, um pequeno fragmento dessa proteína viral, pep3R–1, pode ser reaproveitado para reduzir com segurança a inflamação excessiva em camundongos, inclusive em um modelo de doença intestinal. Embora muito ainda precise ser feito — como melhorar estabilidade, entrega e testes em mais contextos de doença — o estudo revela tanto um ponto fraco crítico que estratégias antivirais poderiam mirar quanto um plano promissor para projetar novos fármacos anti-inflamatórios à base de peptídeos inspirados na evasão imune viral.
Citação: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Palavras-chave: Peste suína africana, imunidade inata, NF-kappaB, MyD88, peptídeo anti-inflamatório