Clear Sky Science · pt
Homeostase do ferro anormal media prejuízo das células ciliadas cocleares e perda auditiva em camundongos deficientes em Gprasp2
Por que isso importa para a audição no dia a dia
A perda auditiva costuma ser vista como mero "desgaste", mas para muitas pessoas ela é causada por defeitos genéticos ocultos. Este estudo revela como um gene pouco estudado, GPRASP2, ajuda a proteger as delicadas células sensoriais do ouvido interno contra danos induzidos por ferro. Ao mostrar exatamente como as coisas dão errado quando esse gene está ausente, o trabalho abre caminho para diagnósticos mais precisos e futuras terapias para problemas auditivos hereditários e possivelmente para transtornos de humor relacionados.
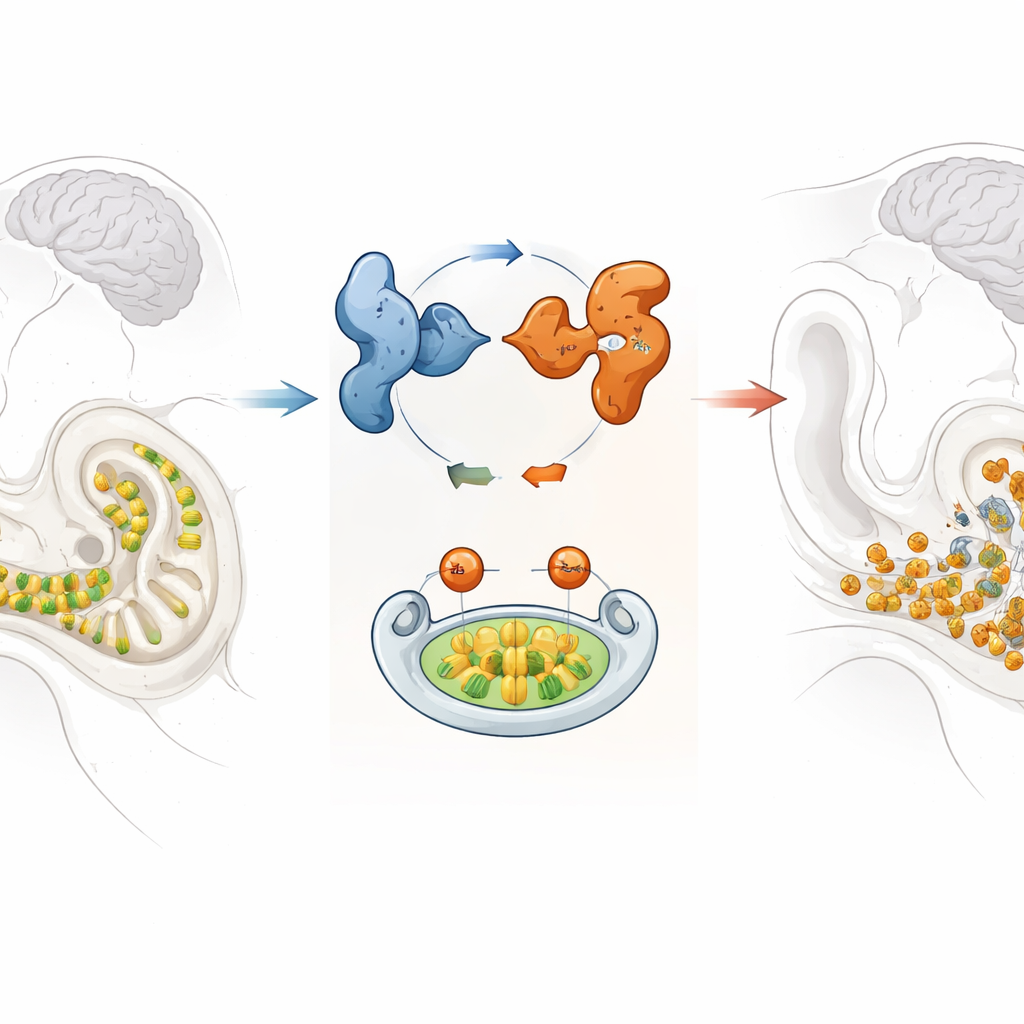
Um sensor de som frágil no ouvido interno
Dentro da cóclea enrolada do ouvido interno ficam fileiras de células ciliadas que convertem pequenas vibrações em sinais elétricos que o cérebro consegue interpretar. Uma vez que essas células são perdidas, elas não se regeneram, por isso mantê‑las saudáveis é crítico para a audição ao longo da vida. Os pesquisadores se concentraram em GPRASP2, um gene previamente encontrado mutado em uma família com perda auditiva sindrômica ligada ao X, o que significa que a condição afeta principalmente homens e pode vir acompanhada de sintomas adicionais. Embora se soubesse que GPRASP2 é ativo no cérebro e no ouvido interno, seu papel exato na audição permanecia obscuro.
O que acontece quando o gene está ausente
Para imitar a condição humana, a equipe usou edição genética CRISPR para criar camundongos que não possuem uma cópia funcional do gene Gprasp2. Esses animais apresentaram perda auditiva evidente em uma ampla faixa de frequências quando testados com registros elétricos sensíveis do nervo auditivo. Suas respostas a sons altos repentinos estavam atenuadas, mas o equilíbrio e as habilidades motoras eram em grande parte normais, apontando para um problema específico na audição em vez de um distúrbio motor geral. Curiosamente, os camundongos também exibiram comportamentos semelhantes à depressão em vários testes padrão, sugerindo que esse gene conecta audição e humor por meio de suas ações tanto no ouvido quanto no cérebro.
Danos dentro da cóclea
Ao examinar os ouvidos internos de camundongos deficientes em Gprasp2, os cientistas descobriram que muitas células ciliadas externas estavam ausentes ou deslocadas, e as células remanescentes frequentemente apresentavam feixes distorcidos de pequenas projeções que normalmente atuam como diapasões. Também observaram alterações na estria vascular, um tecido altamente ativo que mantém o fluido e o ambiente elétrico especiais necessários para a audição. Em nível microscópico, marcadores de morte celular e estresse oxidativo estavam elevados nas células ciliadas externas e nas células nervosas vizinhas, indicando que essas estruturas estavam sob forte ataque de moléculas reativas e mais propensas a morrer.
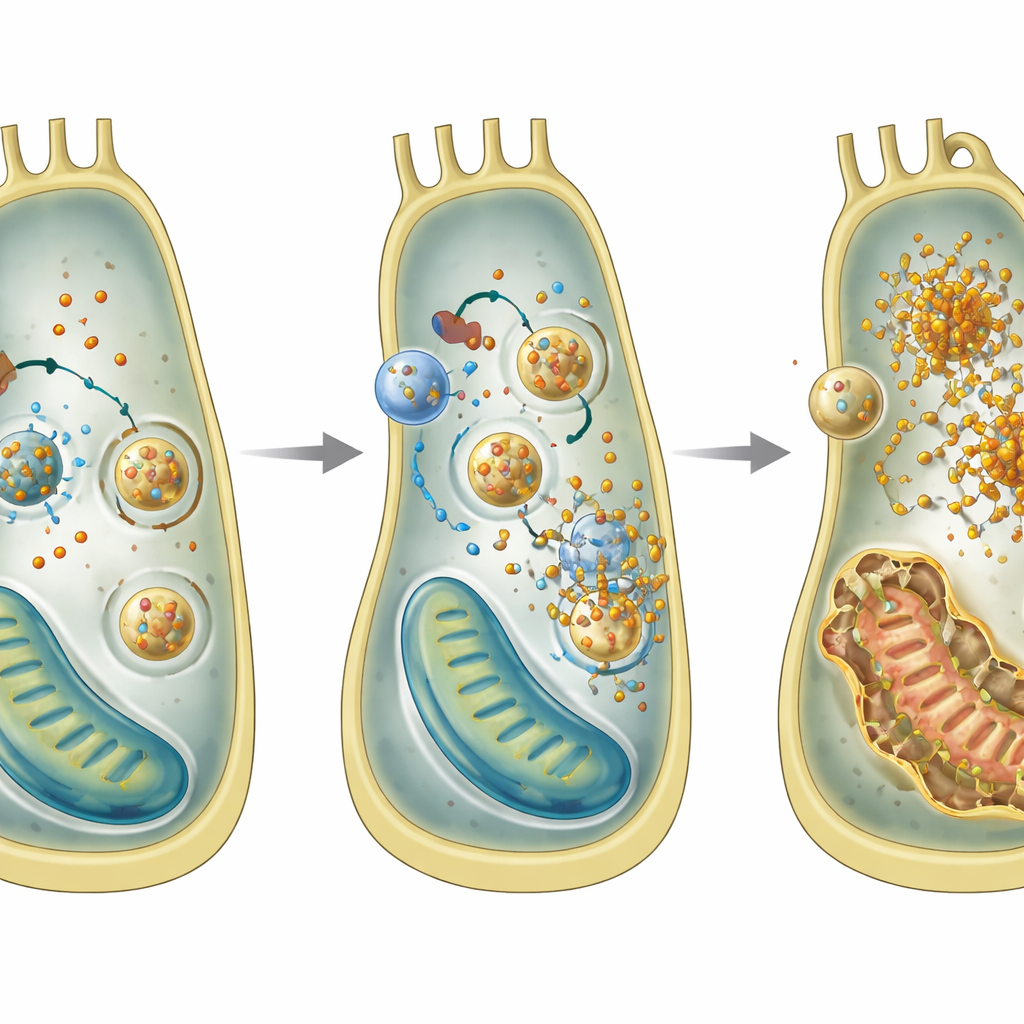
Sobrecarga de ferro e reciclagem descontrolada
Aprofundando, a equipe utilizou uma linhagem celular do ouvido interno para explorar o que dá errado dentro de células individuais sem GPRASP2. Eles descobriram um padrão característico de uma forma de morte celular chamada ferroptose, que é impulsionada pelo ferro e pela peroxidação lipídica. Células sem Gprasp2 acumularam mais ferro ferroso, produziram mais espécies reativas de oxigênio, tiveram níveis reduzidos do antioxidante glutationa e mostraram mitocôndrias danificadas. Análises de genes e proteínas apontaram para um aumento da ferritinofagia, um processo no qual partículas de armazenamento de ferro são entregues a compartimentos de reciclagem e degradadas, liberando ferro extra na célula. Bloquear essa etapa de reciclagem reduziu o acúmulo de ferro, apoiando a ideia de que a ferritinofagia excessiva é central para o dano.
Uma proteína parceira chave que mantém o ferro sob controle
Os pesquisadores então investigaram como GPRASP2 regula essa maquinaria de manejo do ferro. Mapeando proteínas que interagem com GPRASP2, identificaram a NCAM1, uma molécula de adesão celular mais conhecida por seus papéis em aprendizado, memória e humor. Demonstraram que GPRASP2 se liga fisicamente à NCAM1, e que a perda de GPRASP2 causa queda nos níveis de NCAM1 nas células ciliadas e em células auditivas cultivadas. Níveis baixos de NCAM1 foram ligados ao aumento da ferritinofagia e à sobrecarga de ferro. Restaurar NCAM1 em células deficientes em Gprasp2 reduziu os níveis de ferro e atenuou reguladores chave da ferritinofagia, mesmo que a autofagia geral permanecesse ativa. Isso sugere que GPRASP2 ajusta finamente uma via específica de reciclagem do ferro através da NCAM1, em vez de ligar ou desligar todo o sistema de reciclagem.
O que isso significa para a audição e além
Em termos simples, este trabalho mostra que GPRASP2 atua como um gerente de segurança para o ferro dentro das células ciliadas cocleares. Quando o GPRASP2 está presente, ele coopera com a NCAM1 para impedir que ferro armazenado em excesso seja devolvido à célula, mantendo o dano oxidativo sob controle. Quando o gene é perturbado, o manejo do ferro sai do equilíbrio, as células "enferrujam" de dentro para fora, e células ciliadas cruciais morrem, levando à perda auditiva. Como GPRASP2 e NCAM1 também funcionam no cérebro, essa mesma via pode ajudar a explicar alterações de humor observadas em alguns pacientes. Entender esse modo de falha baseado no ferro oferece um alvo claro para futuros fármacos ou terapias gênicas voltadas a preservar a audição em pessoas com distúrbios genéticos relacionados ao GPRASP2 ou com mecanismos semelhantes.
Citação: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Palavras-chave: perda auditiva hereditária, células ciliadas cocleares, homeostase do ferro, ferroptose, GPRASP2