Clear Sky Science · pt
Ativação do receptor acoplado à proteína G codificado pelo citomegalovírus UL33 por um peptídeo N-terminal inato
Como um Vírus Comum Reconecta Nossas Células
O citomegalovírus humano (HCMV) infecta silenciosamente a maioria das pessoas no planeta e, na maioria das vezes, passa despercebido. Ainda assim, em recém‑nascidos, pacientes transplantados e outros com o sistema imunológico comprometido, pode causar doenças graves. Este estudo revela, em detalhe molecular, como uma proteína viral chamada UL33 age como um interruptor interno que empurra constantemente as células infectadas a favorecer o vírus. Compreender esse interruptor oculto ajuda a explicar como o HCMV persiste por toda a vida e aponta para novas maneiras de desativá‑lo sem prejudicar a sinalização celular normal.
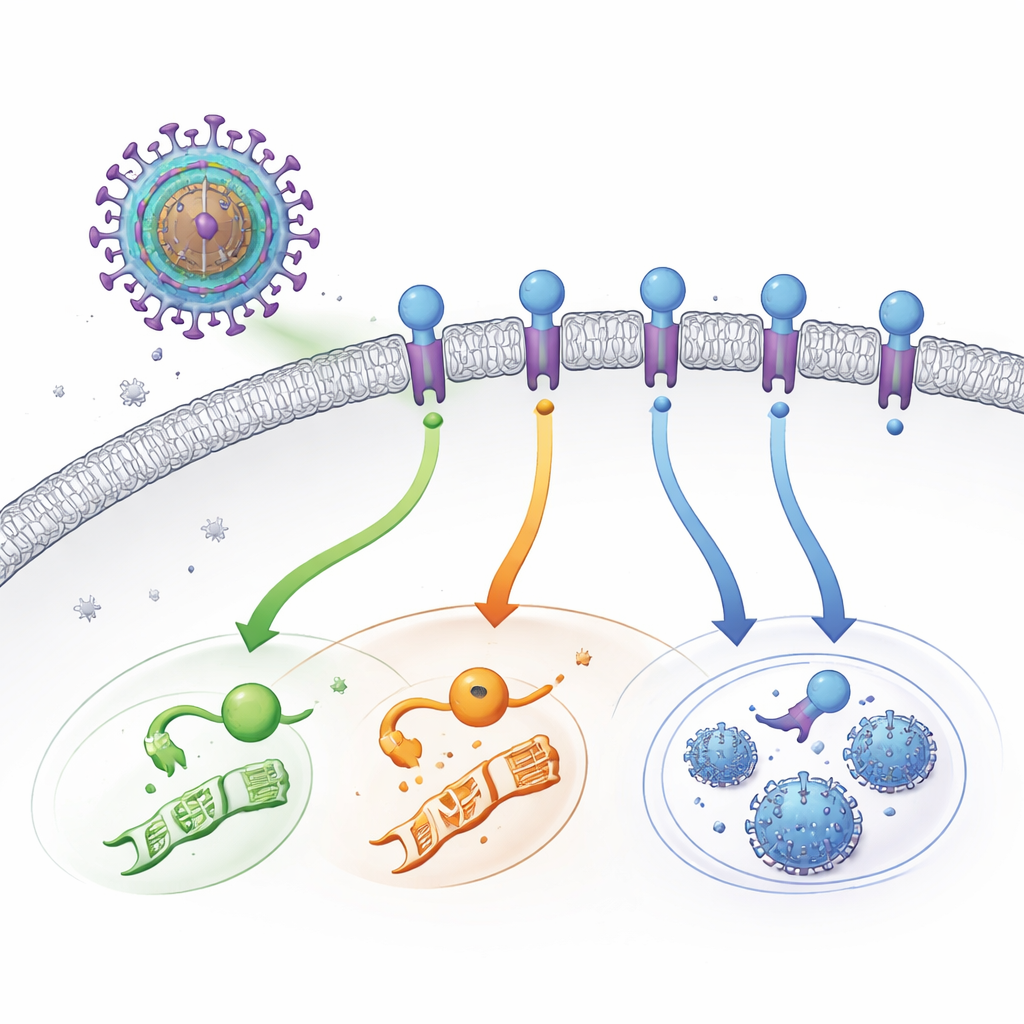
Um Interruptor Viral Furtivo na Superfície Celular
O HCMV carrega suas próprias versões de receptores de superfície celular — proteínas que normalmente detectam hormônios ou sinais imunes. UL33 é um desses receptores virais. Ao contrário dos receptores típicos, que aguardam um sinal externo, UL33 está “sempre ativo”. Uma vez inserido na membrana externa da célula infectada, pode acionar várias das principais vias de comunicação da célula ao mesmo tempo. Essas vias controlam processos como atividade gênica, metabolismo e a decisão entre permanecer latente ou produzir mais vírus. Por anos, os cientistas sabiam que UL33 era ativo, mas não sabiam o que o ativava, especialmente porque nunca foi encontrado um molécula ativadora externa (ligante).
Um Auto‑acionador: o Receptor que Traz Sua Própria Chave
Usando crio‑microscopia eletrônica avançada, os autores capturaram imagens tridimensionais de UL33 ligado a um dos parceiros de sinalização da célula, uma proteína G chamada Gs. As imagens mostram que o início da proteína UL33 — sua curta cauda N‑terminal — dobra‑se de volta para um bolso no próprio receptor, muito parecido com uma chave deixada permanentemente na fechadura. Essa cauda “presa” encaixa‑se em um pequeno bolsão lateral que, em receptores humanos relacionados, normalmente receberia parte de uma proteína de sinalização imune chamada quimiocina. Ao ocupar esse bolsão desde o início, UL33 impede que quimiocinas externas se liguem, explicando por que ele se comporta como um receptor “órfão” que não responde aos mensageiros normais do hospedeiro.
Átomos Cruciais no Interruptor Viral
Para confirmar que essa cauda embutida é realmente o gatilho, a equipe alterou sistematicamente blocos construtores individuais de UL33 em células humanas. Eles focaram-se nos primeiros aminoácidos da cauda e nos pontos correspondentes dentro do bolsão que a seguram. Quando substituíram esses resíduos-chave por outros mais neutros ou removeram um deles completamente, a capacidade de sinalização de UL33 caiu para quase zero — embora os receptores alterados ainda alcançassem a superfície celular em quantidades normais. Em outras palavras, a proteína estava presente, mas muda. Isso mostra que a cauda não é apenas enfeite estrutural; é a peça autoativadora essencial que mantém UL33 ligado.
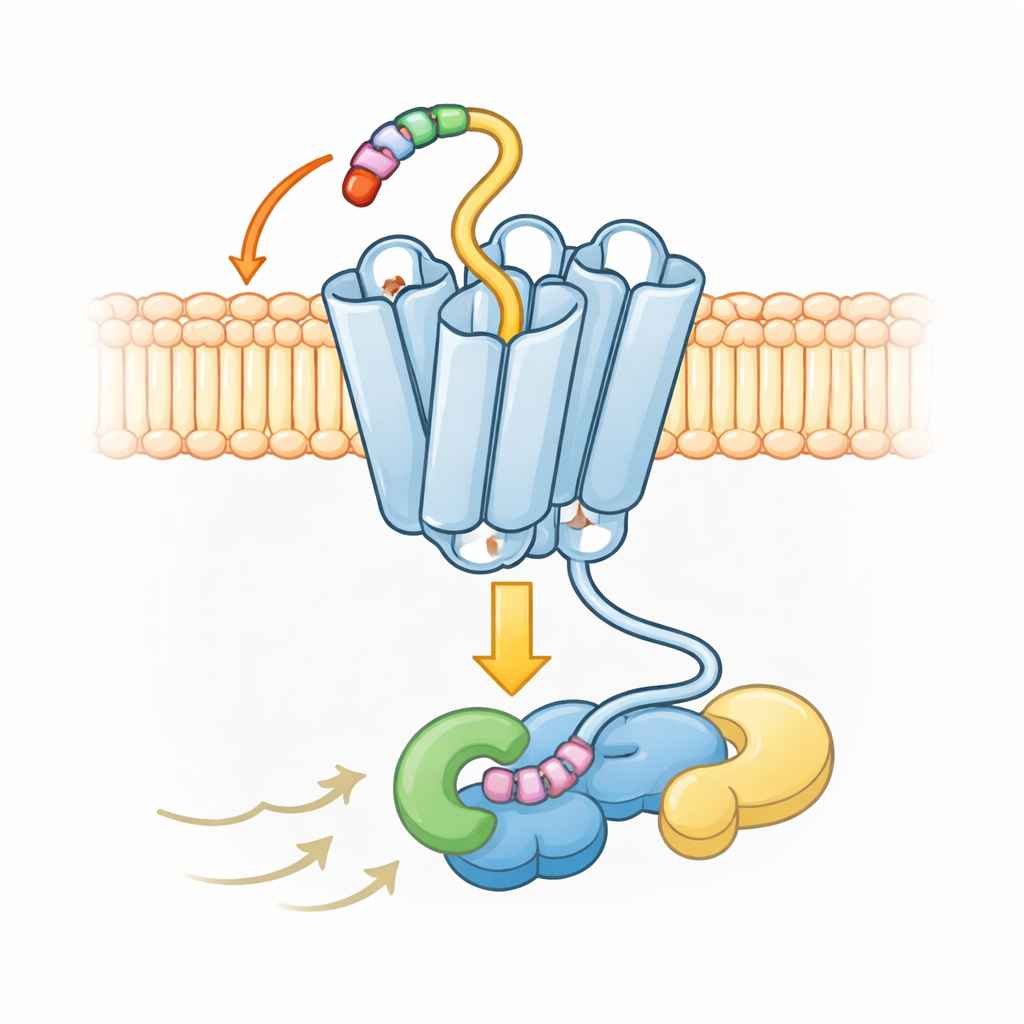
Uma Forma Incomum para Sinalização Ampla, mas Controlada
Os mapas estruturais também revelam que UL33 adota uma conformação ativa ligeiramente diferente em comparação com receptores humanos típicos. Na maioria dos receptores dessa família, uma das sete hélices próximo ao interior da célula se projeta para fora dramaticamente quando o receptor é ativado, abrindo uma grande cavidade para que as proteínas G se acomodem. Em UL33, essa hélice permanece muito mais próxima do centro, criando um encaixe mais apertado. Apesar disso, UL33 ainda pode engajar vários tipos de proteínas G — Gs, Gq e Gi — fazendo contatos precisos com a ponta da proteína G que se encaixa no receptor. Esses contatos favorecem algumas proteínas G e excluem outras, como o grupo G12/13, permitindo que o vírus direcione as respostas da célula sem desencadear sinalização descontrolada.
Novas Vulnerabilidades para um Vírus Antigo
Ao combinar imagens estruturais com testes funcionais, o estudo pinta um quadro claro: UL33 é um receptor viral auto‑iniciador cuja própria cauda atua como um ativador permanentemente ligado. Esse design permite ao HCMV ajustar de forma sutil, porém persistente, a sinalização da célula hospedeira para apoiar a replicação e a reativação viral, especialmente ao reforçar vias que ativam genes virais. Ao mesmo tempo, o trabalho expõe pontos fracos que drogas poderiam explorar, como um túnel estreito que leva ao bolsão onde a cauda se liga. Moléculas projetadas para encaixar nessa região ou desalojar a cauda podem silenciar a atividade de UL33 e reduzir o dano viral, poupando os receptores normais do organismo. Para pacientes em risco por HCMV, mirar esse “interruptor mestre” viral pode, um dia, oferecer uma forma mais precisa de manter o vírus sob controle.
Citação: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Palavras-chave: citomegalovírus, GPCR viral, sinalização celular, estrutura por crio‑EM, direcionamento de fármacos