Clear Sky Science · pt
Investigando as respostas de biofilmes de Salmonella ao tratamento com antibióticos usando espectroscopia óptica fototérmica no infravermelho
Por que as cidades pegajosas de germes importam
Muitos microrganismos causadores de doenças preferem viver em comunidades densamente agrupadas chamadas biofilmes, onde as células aderem umas às outras e a superfícies dentro do corpo ou em dispositivos médicos. Nessas “cidades” viscosas, os micróbios podem resistir a antibióticos que normalmente os matariam. Este estudo apresenta uma nova maneira de observar biofilmes em detalhes finos, revelando quais células estão ativamente crescendo e como reagem quando fármacos potentes são adicionados. Compreender esses padrões de atividade invisíveis pode ajudar médicos a desenhar tratamentos que finalmente rompam as defesas teimosas dos biofilmes.
Vida oculta dentro das cidades bacterianas
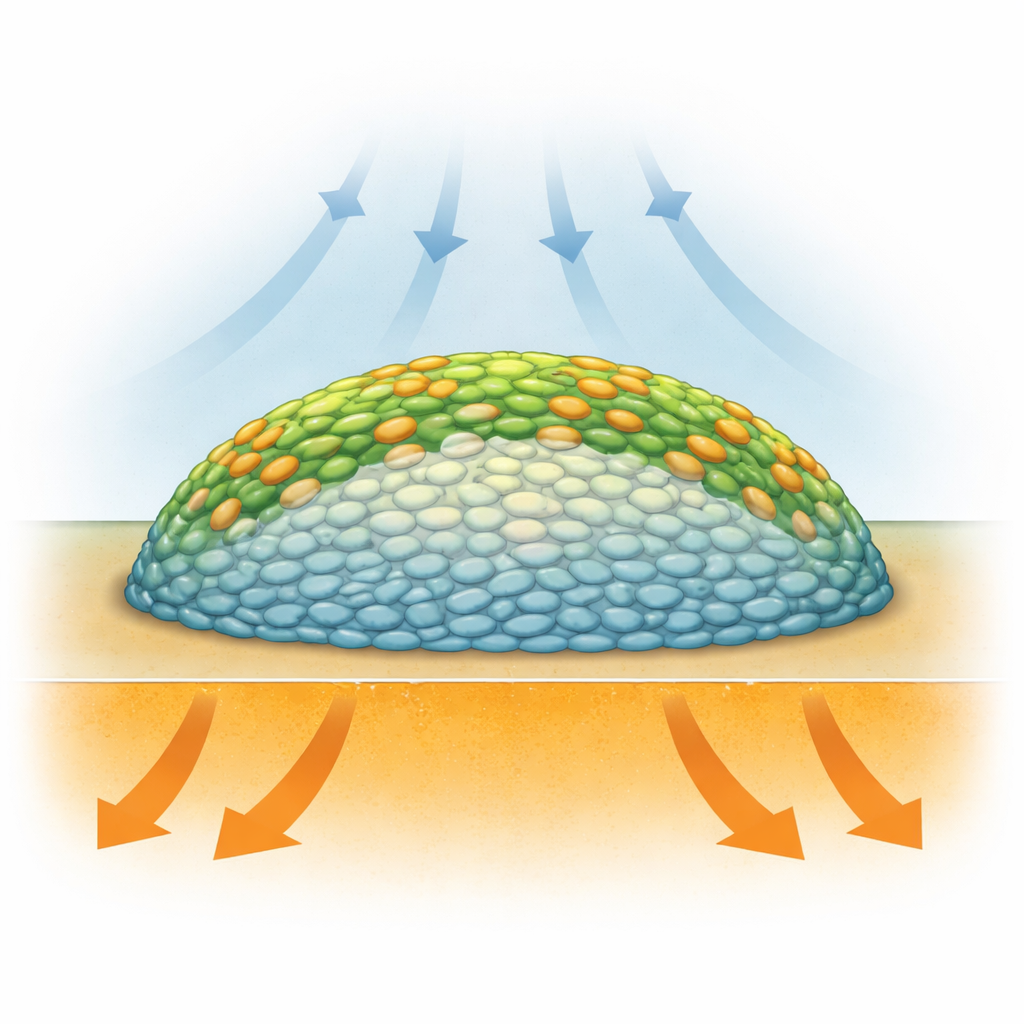
Biofilmes não são apenas aglomerados aleatórios de germes: são estruturas em camadas onde as bactérias vivem em condições muito diferentes dependendo de sua posição. Células na parte externa têm maior acesso ao oxigênio do ar, enquanto as enterradas no centro ficam privadas de oxigênio e podem reduzir seu metabolismo ou entrar em dormência. Métodos anteriores, como microscopia de fluorescência, podiam mostrar a estrutura, mas frequentemente exigiam corantes adicionados ou marcadores genéticos que podem alterar a biologia, e não mediam diretamente o que as células faziam quimicamente. Os pesquisadores precisavam de uma forma de “ver” a química de biofilmes vivos, camada por camada, sem destruí-los ou alterá-los fortemente.
Ver a química com luz invisível
A equipe recorreu a uma técnica chamada espectroscopia óptica fototérmica no infravermelho (O-PTIR), que usa pulsos de luz infravermelha invisível e um laser visível para detectar pequenas vibrações em moléculas. Essas vibrações funcionam como impressões digitais de componentes celulares chave, como proteínas, lipídios e DNA. Para rastrear o metabolismo — o uso ativo de nutrientes — alimentaram biofilmes de Salmonella Typhimurium com uma forma especial de açúcar em que os átomos de carbono eram ligeiramente mais pesados que o usual (um isótopo estável conhecido como carbono-13). Quando as células estão ativas crescendo e sintetizando proteínas, incorporam esses átomos mais pesados em suas estruturas, o que causa deslocamentos sutis, mas detectáveis, no sinal infravermelho. Ao criocortar o biofilme e escanear seções transversais finas, os pesquisadores produziram mapas químicos que mostram onde no biofilme esse carbono pesado foi incorporado.
Anéis de atividade e núcleos silenciosos
A imagem infravermelha de biofilmes de Salmonella não tratados revelou um padrão marcante: as regiões externas e as camadas de superfície mostraram forte incorporação do carbono pesado, enquanto um grande núcleo central exibiu muito pouco. Em outras palavras, o biofilme comportou-se como um anel de células ativas circundando um interior silencioso. A análise estatística dos espectros infravermelhos confirmou que os sinais relacionados a vibrações de proteínas se deslocaram mais nas camadas externas do que no centro, indicando maior produção proteica nas bordas. Essas descobertas reforçam a ideia de que a disponibilidade de oxigênio, maior próximo à superfície, é o principal motor das “zonas quentes” metabólicas neste modelo de colônia, mesmo que nutrientes entrem por baixo. O estudo forneceu uma das visões mais claras e de maior resolução até agora sobre como o metabolismo é estratificado dentro de um biofilme.
Como antibióticos diferentes remodelam a atividade do biofilme
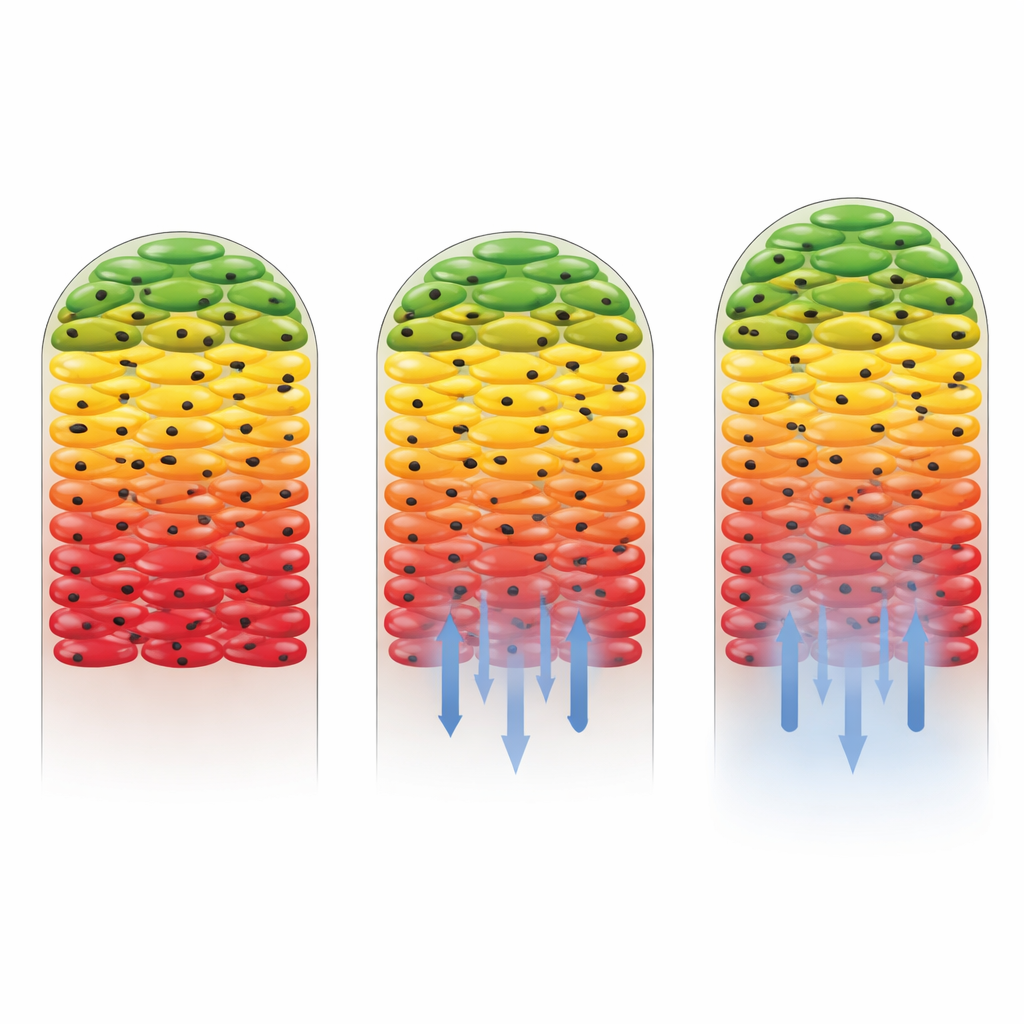
Os pesquisadores então perguntaram o que acontece quando antibióticos são introduzidos. Usaram dois fármacos: canamicina, à qual a cepa de Salmonella é sensível, e gentamicina, à qual a cepa havia sido geneticamente configurada para ser em grande parte não-suscetível. Quando a gentamicina estava presente, o padrão geral de camadas externas ativas e núcleo silencioso mal mudou, mostrando que as células resistentes continuaram a crescer e a incorporar carbono pesado em grande parte do biofilme. Em contraste, a canamicina reduziu dramaticamente a atividade metabólica, especialmente perto da base do biofilme, onde a concentração do fármaco era maior. Apenas uma faixa fina de células mais distante da fonte do antibiótico ainda mostrou sinais de captação de carbono. Isso revelou não só que o fármaco foi eficaz, mas também que a própria estrutura do biofilme ajudou a proteger algumas células ao enfraquecer o antibiótico conforme ele difundia para o interior.
Novas janelas para tratar infecções difíceis
Do ponto de vista leigo, a mensagem principal é que este trabalho oferece um “microscópio químico” poderoso para observar como comunidades bacterianas vivem e sobrevivem a tratamentos em três dimensões. Ao combinar um método de imagem infravermelha não destrutivo com uma forma segura de carbono pesado, os pesquisadores puderam localizar onde as bactérias estavam ativamente crescendo e como essa atividade mudava sob diferentes antibióticos. Seus resultados confirmam que biofilmes abrigam uma mistura de células ativas e quase dormentes, e que fármacos eficazes ainda podem ser atenuados pela barreira física do biofilme. No futuro, essa abordagem poderia ser usada para testar novas terapias, explorar como diferentes espécies cooperam ou compartilham resistência em biofilmes mistos e, em última instância, ajudar a desenhar estratégias mais inteligentes para eliminar infecções persistentes.
Citação: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Palavras-chave: biofilmes, Salmonella, resistência a antibióticos, imagens no infravermelho, marcação por isótopos estáveis