Clear Sky Science · pt
Seleção de modelos em pesquisa pré-clínica de terapias com ácidos nucleicos
Transformando genes em medicamentos
As terapias com ácidos nucleicos são um novo tipo de medicamento que não atuam bloqueando proteínas, como a maioria das drogas, mas sim um passo antes, ao nível das nossas mensagens genéticas. Esta revisão explica como os cientistas escolhem os modelos laboratoriais e animais adequados para testar esses fármacos que miram o RNA antes que cheguem aos pacientes. Um leitor leigo pode se interessar porque escolhas inteligentes de modelos podem significar tratamentos para doenças genéticas mais rápidos, mais seguros e mais eficazes, incluindo distúrbios infantis raros e condições mais comuns, como doenças cardíacas.
O que torna essas terapias genéticas diferentes?
As terapias com ácidos nucleicos (TANs) incluem cadeias curtas chamadas oligonucleotídeos antissenso (ASOs) e pequenos RNAs interferentes (siRNAs). Em vez de depender da forma e da química de alvos proteicos, esses fármacos reconhecem seus alvos por regras de pareamento de bases — o mesmo emparelhamento A‑T e G‑C que sustenta o DNA. Isso os torna programáveis: uma vez conhecida a sequência de RNA que se quer alterar, frequentemente é possível projetar muitos candidatos rapidamente, sem anos de química tradicional. A parte difícil deixa de ser “Conseguimos fabricar um composto ativo?” e passa a ser “Como medir se ele realmente funciona em um contexto biológico realista?” Porque até uma única diferença de letra na sequência pode determinar a atividade, escolher os sistemas de teste adequados torna-se crítico.
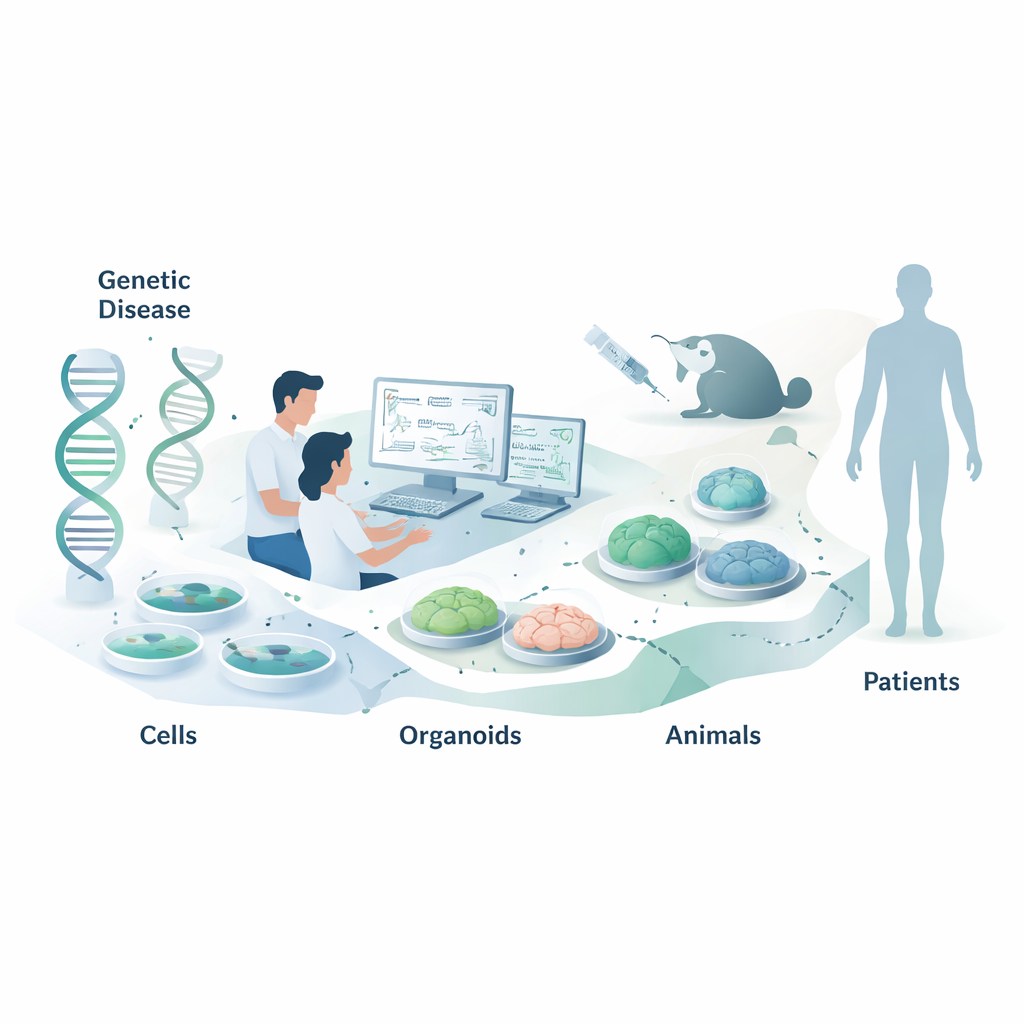
Testes celulares simples: rápidos, mas não suficiente
A primeira parada para a maioria das TANs é um painel de linhagens celulares relativamente fáceis de cultivar, como células HeLa ou HEK293, que já expressam o RNA alvo. Os pesquisadores adicionam grandes bibliotecas de ASOs ou siRNAs candidatos e então medem quanto o RNA alvo e sua proteína caem, usando técnicas como PCR e Western blot. Eles também podem trabalhar com células de pacientes, que capturam melhor o histórico genético individual e permitem testar drogas “seletivas por alelo” que silenciam apenas a cópia defeituosa de um gene. Quando o gene natural não é convenientemente expresso, cientistas às vezes introduzem mini‑genes artificiais ou plasmídeos repórter que brilham quando o RNA é cortado ou corretamente empalmeado. Esses sistemas são poderosos para comparar muitos desenhos rapidamente, mas podem deixar de capturar detalhes importantes, como a estrutura natural do RNA ou o processamento específico de tipos celulares, então os resultados precisam ser confirmados em contextos mais realistas.
Do conserto molecular ao comportamento celular real
Muitas TANs visam não apenas destruir RNA defeituoso, mas repará‑lo alterando o empalme, o processo que costura os trechos da mensagem gênica. ASOs cuidadosamente projetados podem levar células a pular um éxon nocivo, restaurar uma peça ausente ou impedir a inserção de um “pseudo‑éxon” que quebra o código. Para ver se tais mudanças realmente melhoram a função celular, os pesquisadores vão além de leituras simples de níveis de RNA e proteína. Em células derivadas de pacientes, testam se a atividade enzimática retorna, se o transporte de íons em células pulmonares se normaliza ou se vias de sinalização em células imunes respondem corretamente. Cada vez mais, usam organoides tridimensionais — mini‑tecidos cultivados a partir de células‑tronco de pacientes — que podem imitar batimentos cardíacos, atividade de redes cerebrais ou outros comportamentos complexos. Esses modelos 3‑D são mais próximos de órgãos reais, mas são mais difíceis, mais lentos e mais caros de executar, de modo que as equipes precisam equilibrar realismo e capacidade de triagem.
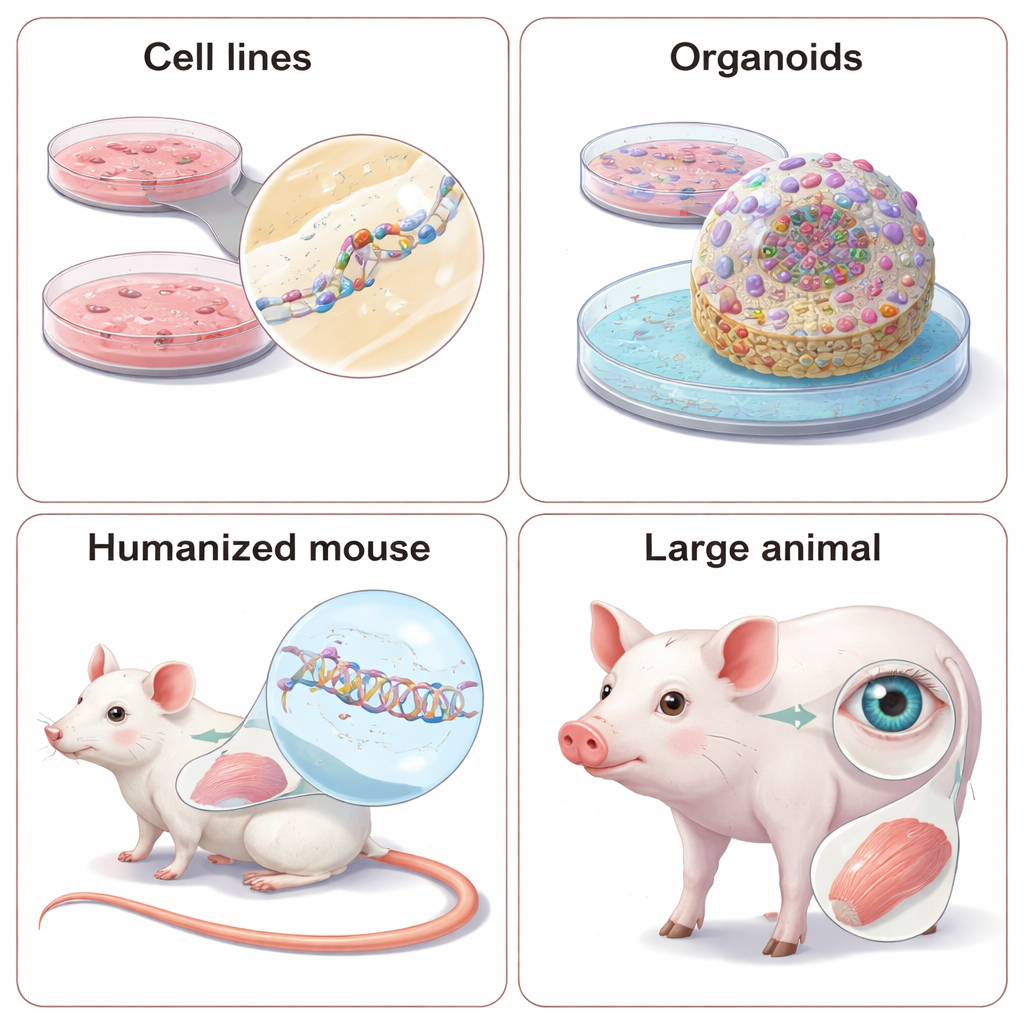
Por que os animais ainda importam — e como torná‑los mais humanos
Algumas características da doença, como metabolismo do organismo inteiro, interações entre órgãos ou comportamento, simplesmente não podem ser capturadas em placas. Para isso, as TANs são testadas em animais vivos. Como esses fármacos dependem de sequências exatas de RNA, os cientistas enfrentam uma escolha: projetar drogas “substitutas” que combinem com a versão do gene do animal, ou reengenheirar o animal para carregar sequências genéticas humanas. ASOs e siRNAs substitutos podem revelar se reduzir um gene melhora os sintomas em modelos murinos bem estabelecidos, mas eles não reproduzem perfeitamente a droga que mira o alvo humano. Modelos humanizados — camundongos ou até mini‑porcos com trechos ou cópias inteiras de genes humanos — permitem testar o candidato clínico real, mas exigem tempo e custo significativos, e diferenças sutis na regulação gênica entre espécies ainda podem causar surpresas. A revisão também destaca o uso crescente de animais de grande porte, especialmente para doenças do olho e do músculo, onde a anatomia se assemelha mais à humana.
Olhando adiante: modelos mais inteligentes e menos conjectura
Os autores concluem que não existe um único “melhor” modelo para fármacos de ácidos nucleicos; em vez disso, cada projeto precisa de um caminho sob medida que comece por ensaios rápidos e simples e avance para sistemas mais complexos e relevantes para o humano. À medida que reguladores e financiadores pressionam para reduzir o uso de animais, espera‑se que organoides sofisticados, dispositivos organ‑on‑a‑chip e modelos computacionais assumam mais do trabalho, especialmente quando combinados com ferramentas de aprendizado de máquina que preveem quais sequências e químicas funcionarão melhor. Em última análise, ao entender os pontos fortes e os pontos cegos de cada modelo — e ao compartilhar melhores práticas e dados por todo o campo — os pesquisadores podem transformar de forma mais confiável ideias genéticas programáveis em medicamentos seguros e eficazes para pacientes.
Citação: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Palavras-chave: terapias com ácidos nucleicos, oligonucleotídeos antissenso, siRNA, modelos pré-clínicos, terapia gênica