Clear Sky Science · pt
Ligação seletiva de cátions divalentes remodela a mecânica do nucleossomo e libera a dinâmica das caudas de histona
Como íons minúsculos ajudam a gerenciar nosso DNA
Dentro de cada célula, metros de DNA precisam ser dobrados, empacotados e, ainda assim, acessíveis sob demanda. Este artigo explora como dois íons minerais comuns em nossas células, magnésio e cálcio, remodelam sutilmente a forma como o DNA se enrola em torno das proteínas, influenciando o quão compactado está nosso material genético e com que facilidade ele pode ser lido. Ao simular essas interações em detalhe atômico, os autores revelam que variações nos níveis de íons podem endurecer ou relaxar estruturas locais do DNA e alterar o comportamento de caudas proteicas flexíveis que ajudam a organizar os cromossomos.
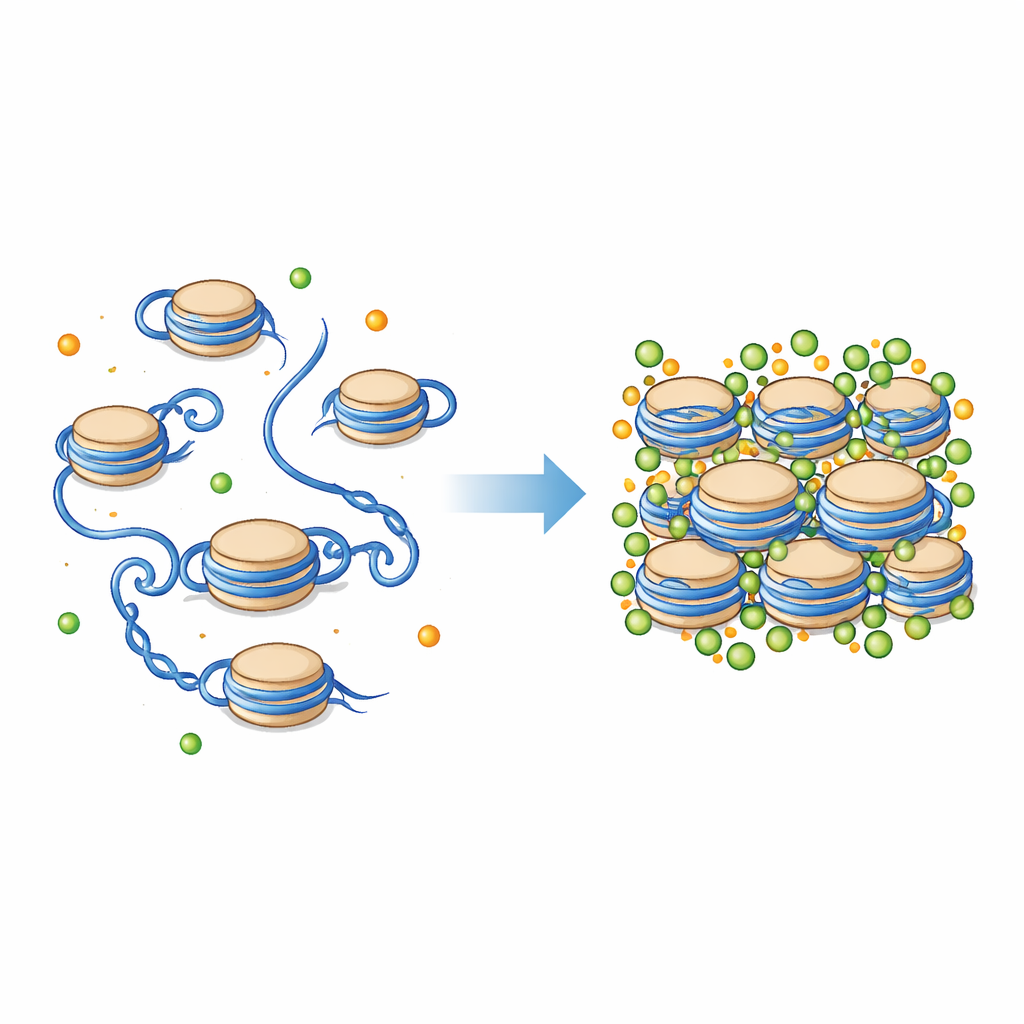
A conta no coração do empacotamento cromossômico
O DNA em nossas células não fica solto; ele se enrola em carretéis proteicos chamados nucleossomos. Cada nucleossomo é um trecho curto de DNA enrolado em torno de um conjunto de proteínas histonas, com caudas flexíveis que se estendem para fora. Juntas, essas unidades formam a estrutura básica de “contas em um fio” da cromatina, que pode então se dobrar em fibras mais compactas. O ambiente ao redor dos nucleossomos está cheio de partículas carregadas, incluindo magnésio (Mg²⁺) e cálcio (Ca²⁺). Esses íons são conhecidos por ajudar a condensar os cromossomos, mas exatamente como influenciam os detalhes mecânicos minuciosos dos nucleossomos e de suas caudas de histona tem sido difícil de observar diretamente.
Simulando um mundo atômico congestionado
Para desvendar esses detalhes, os autores executaram 81 microssegundos de simulações computacionais de grande escala nas quais cada átomo de DNA, proteína, água e íons foi modelado explicitamente. Eles variaram sistematicamente os níveis de magnésio e cálcio, testaram diferentes maneiras de descrever o comportamento dos íons nas simulações e estudaram nucleossomos com e sem suas caudas de histona. Ao comparar os padrões de ligação de íons simulados com medições experimentais, identificaram um modelo refinado que melhor corresponde a como nucleossomos reais atraem esses íons, onde o magnésio prefere fendas do DNA e o cálcio mais frequentemente se prende ao esqueleto do DNA e a certos sítios ácidos nas proteínas.
Como os íons comprimem o DNA e enrijecem o núcleo
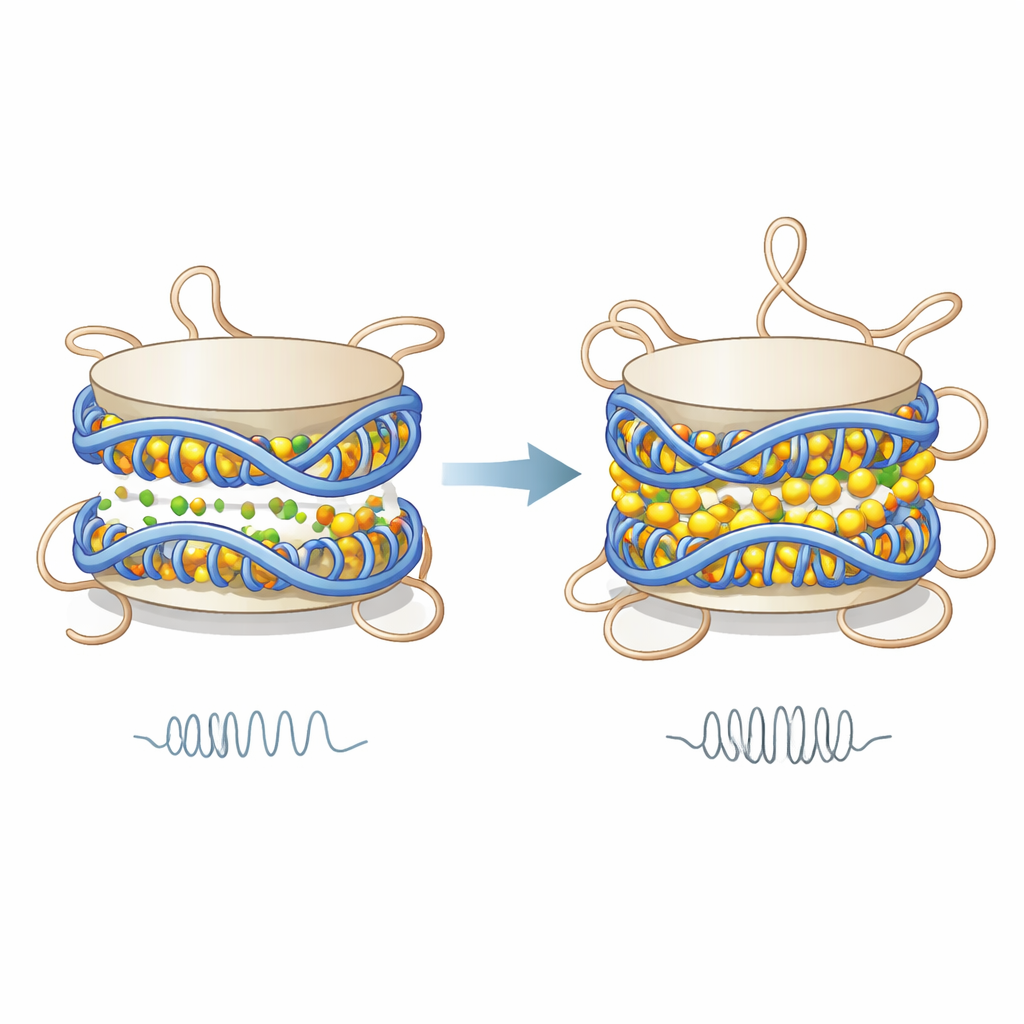
As simulações mostram que íons divalentes se aglomeram ao longo da superfície do DNA e no espaço estreito entre as duas voltas de DNA que enrolam cada nucleossomo. Ao neutralizar parcialmente a forte carga negativa do DNA, esses íons reduzem a repulsão elétrica entre voltas vizinhas do DNA. O resultado é que as duas espirais de DNA se aproximam, o nucleossomo fica ligeiramente mais curto e sua rigidez mecânica aumenta, conforme medido por um modelo que trata o nucleossomo como um pequeno cilindro elástico. Esse aumento de rigidez não decorre de desprendimento do DNA ou de um desenrolamento importante; em vez disso, surge de mudanças sutis no espaçamento e de movimentos mais coordenados de regiões específicas do DNA, que passam a se mover juntas como uma unidade mais rígida.
Libertando as caudas proteicas flexíveis
Enquanto o núcleo de DNA se torna mais compacto e rígido, as caudas flexíveis das histonas respondem de modo oposto. Em condições de baixo teor de íons, aminoácidos carregados positivamente nessas caudas aderem ao DNA carregado negativamente, formando muitos contatos estáveis. Quando magnésio ou cálcio se ligam ao longo do DNA, eles fazem o screening dessas cargas, enfraquecendo a atração entre caudas e DNA. Os autores observam que os contatos entre caudas — especialmente as provenientes da histona H3 — e o DNA diminuem, os tempos de residência no DNA ficam mais curtos e as caudas exploram uma gama maior de posições. Isso significa que as caudas interagem com o DNA em encontros mais frequentes, porém mais breves, tornando-se mais dinâmicas e potencialmente mais livres para alcançar nucleossomos vizinhos.
O que isso significa para o controle gênico e o estado da cromatina
Em conjunto, esses achados delineiam um papel duplo para magnésio e cálcio na cromatina. Ao apertar o enrolamento do DNA e aumentar a rigidez dos nucleossomos, eles promovem uma cromatina mais compacta e menos flexível. Ao mesmo tempo, ao afrouxar os contatos entre cauda de histona e DNA e aumentar o movimento das caudas, expõem-se sítios-chave que podem ser quimicamente modificados ou reconhecidos por proteínas regulatórias. Como as concentrações iônicas no núcleo flutuam com sinais e uso de energia, este trabalho sugere que pequenas mudanças químicas no ambiente celular podem afinar tanto a sensação mecânica dos nucleossomos quanto a acessibilidade de suas caudas regulatórias, ajudando a abrir ou fechar janelas de oportunidade para a atividade gênica.
Citação: Hu, G., Zhang, H., Xu, W. et al. Selective binding of divalent cations reshapes nucleosome mechanics and unlocks histone tail dynamics. Commun Biol 9, 365 (2026). https://doi.org/10.1038/s42003-026-09648-1
Palavras-chave: cromatina, mecânica do nucleossomo, íons de magnésio e cálcio, caudas de histona, regulação gênica