Clear Sky Science · pt
Análise estrutural revela que moléculas de água mediam a autoativação de GPR99
Por que esse receptor é importante para a inflamação
Nossas vias aéreas e outros tecidos estão constantemente detectando sinais químicos que indicam infecção ou irritação. Um desses sensores, uma proteína chamada GPR99 que se localiza na superfície celular, está surgindo como um interruptor importante em doenças inflamatórias, como asma e pólipos nasais. Este estudo explica, em detalhe atômico, como GPR99 pode se ativar sozinho mesmo sem um gatilho químico externo — e como pequenos agrupamentos de água o ajudam a fazer isso — oferecendo pistas para o desenho de novos medicamentos anti-inflamatórios.
Um interruptor embutido dentro de um sensor celular
GPR99 pertence a uma grande família de proteínas de superfície celular que transmitem mensagens do exterior para o interior da célula, frequentemente mudando de forma e recrutando proteínas parceiras chamadas proteínas G. Ao contrário da maioria desses receptores, GPR99 é incomumente ativo mesmo quando nenhuma molécula sinalizadora está ligada. Os autores mostram que uma alça flexível no lado externo de GPR99, conhecida como a segunda alça extracelular, funciona como uma chave interna: ela se dobra dentro do bolso de ligação habitual, imitando um sinal ativador e ligando o receptor por si só.
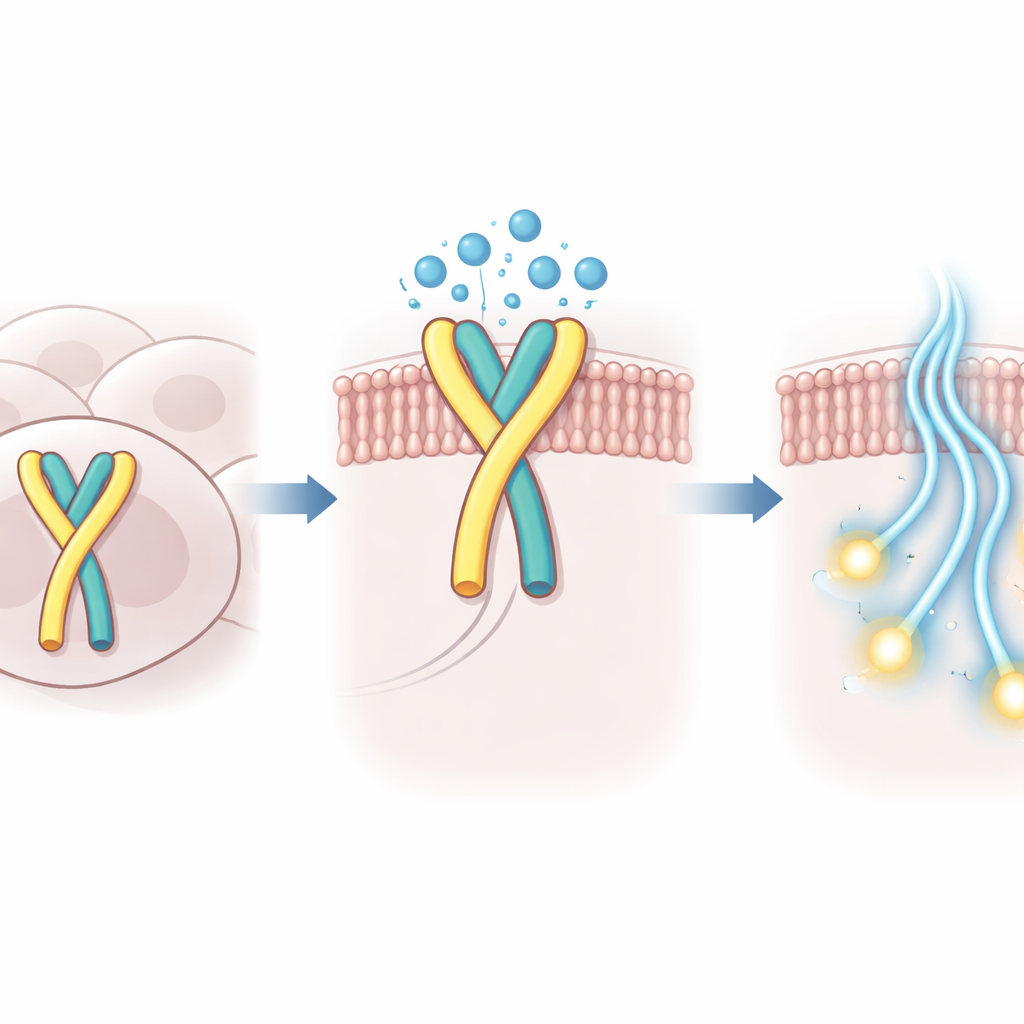
Como a água ajuda a manter o interruptor no lugar
Usando criomicroscopia eletrônica de alta resolução, os pesquisadores capturaram a estrutura tridimensional do GPR99 humano ligado à sua proteína G parceira nesse estado autoativado. No bolso de ligação onde normalmente se sentariam moléculas externas, eles observaram não apenas a alça recolhida, mas também um pequeno aglomerado de moléculas de água ordenadas. Essas moléculas de água formam uma ponte polar entre a alça e a proteína circundante, compensando a inserção mais rasa da alça e estabilizando a forma ativa do receptor. Quando aminoácidos chave na alça ou no bolso vizinho foram alterados de modo a enfraquecer esses contatos mediados por água, a atividade intrínseca do GPR99 caiu drasticamente em testes celulares.
Reorganizando o funcionamento interno para sinalização constante
A equipe comparou sua estrutura autoativada com outros membros da família, incluindo um receptor intimamente relacionado que se liga ao subproduto metabólico succinato e uma forma ativa de GPR99 ligada ao metabólito 2‑oxoglutarato. Eles descobriram que o GPR99, na ausência de qualquer ligante externo, já está totalmente preparado em uma conformação ativa: vários “microswitches” conservados dentro de seu núcleo helicoidal adotam formas normalmente vistas apenas quando esses receptores são estimulados. Posições críticas que costumam ajudar a manter receptores em um estado desligado são substituídas ou reorientadas no GPR99, afrouxando restrições internas e favorecendo a configuração aberta que recebe a proteína G parceira.
Transmitindo a mensagem para o interior da célula
No lado interno da membrana, a estrutura revela como o GPR99 envolve a proteína G do tipo Gq que transmite seu sinal. Uma cauda helicoidal da proteína G se encaixa em uma cavidade aberta pelo balanço para fora de uma das hélices do GPR99, formando uma rede de contatos polares e hidrofóbicos com as alças internas e a cauda do receptor. Mutações que perturbam essa interface também reduzem a sinalização, confirmando que a autoativação criada pela alça externa e pelo aglomerado de água é eficientemente acoplada aos parceiros intracelulares. Juntas, essas imagens estruturais conectam alterações na superfície externa do receptor às ondas de sinalização de cálcio que ele desencadeia dentro das células.
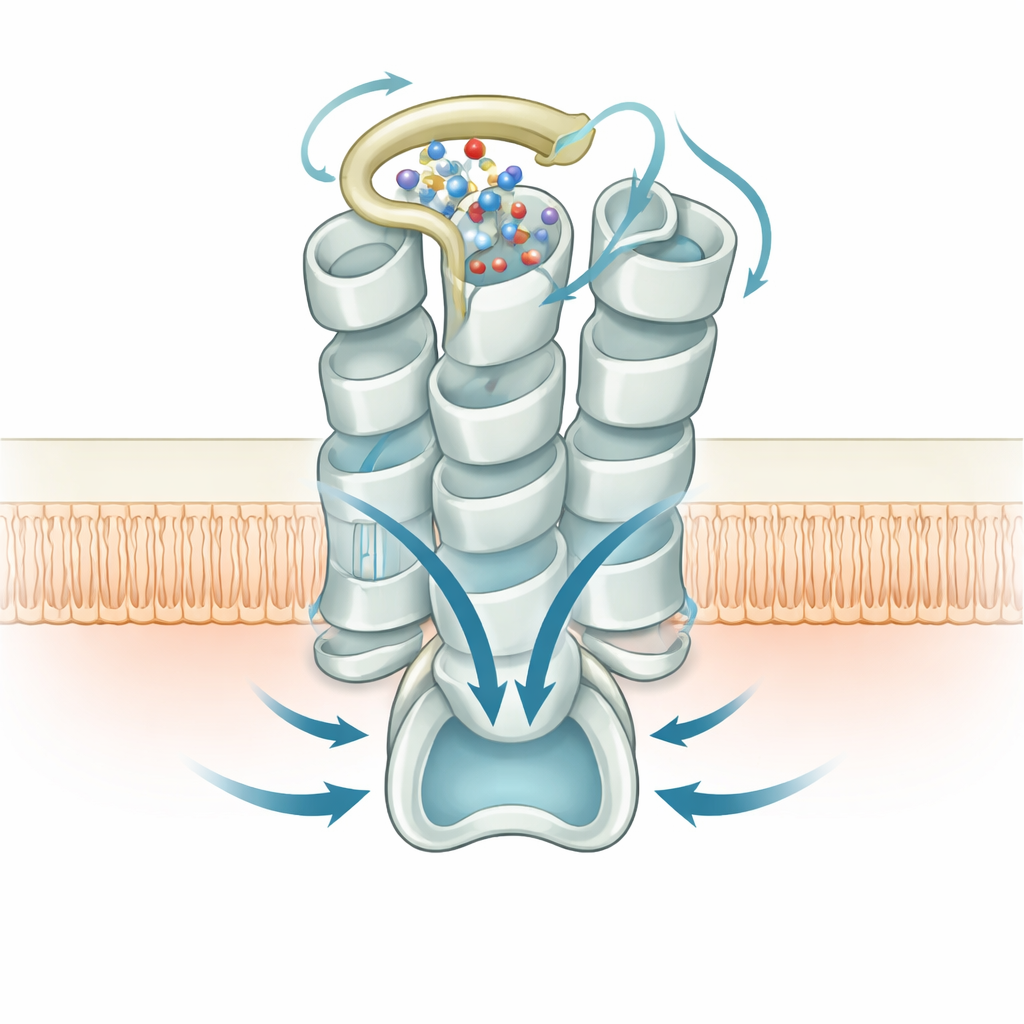
Implicações para a respiração e além
Os autores sugerem que a atividade intrínseca do GPR99, reforçada por moléculas de água estruturais, pode manter os tecidos das vias aéreas em um modo de “prontidão” — preparados para liberar muco e montar uma resposta imune quando lipídios inflamatórios ou mudanças metabólicas aparecem. Como o GPR99 é altamente ativo mesmo sem sinais externos, e porque sua ativação depende de um arranjo específico de alça e água, essas percepções estruturais oferecem alvos concretos para designers de fármacos. Moléculas pequenas que perturbem esse interruptor interno ou sua rede de água poderiam reduzir a inflamação excessiva, enquanto compostos que ajustem finamente a interação poderiam aproveitar a sensibilidade do GPR99 para benefício terapêutico.
Citação: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Palavras-chave: GPR99, ativação de GPCR, biologia estrutural, inflamação, sinalização mediada por água