Clear Sky Science · pt
Mecanismo estrutural do bloqueio por anticorpo anti-MHC-I dos receptores inibitórios das células NK na imunidade antitumoral
Desbloqueando os assassinos silenciosos do corpo
Nosso sistema imune possui um conjunto de sentinelas poderosos chamados células natural killer (NK) que detectam e destroem células cancerosas e infectadas por vírus. Ainda assim, os tumores frequentemente aprendem a silenciar esses sentinelas. Este trabalho revela, em detalhe atômico, como um anticorpo especialmente projetado pode remover esse “botão de mudo”, reativando as NK para que ataquem os tumores com mais eficácia. O estudo combina biologia estrutural de ponta com experimentos em camundongos para mostrar como um anticorpo pode complementar imunoterapias existentes contra o câncer.
As etiquetas de identificação imune em nossas células
Cada célula do nosso corpo exibe na superfície “etiquetas de identificação” moleculares chamadas moléculas MHC de classe I. Essas etiquetas ajudam as células do sistema imune a distinguir tecido normal de células perigosas que se tornaram cancerosas ou foram infectadas por vírus. As NK vasculham constantemente essas etiquetas. Quando detectam padrões normais, receptores inibitórios nas NK enviam um sinal de acalmar que previne o ataque. Tumores frequentemente mantêm essas etiquetas visíveis, usando-as como um escudo protetor: enquanto o sinal inibitório fluir, as NK seguram o gatilho e o câncer pode crescer.
Um anticorpo que agarra o escudo
Os pesquisadores estudaram um anticorpo monoclonal chamado B1.23.2 que se liga fortemente a muitas variantes humanas de MHC de classe I em células tumorais. Usando crio-microscopia eletrônica e cristalografia de raios X, eles mapearam exatamente como esse anticorpo se posiciona na superfície do MHC. B1.23.2 prende-se a uma crista conservada da molécula de MHC — uma hélice α2 — sem tocar sua cadeia leve parceira e apenas percebendo de forma tênue o peptídeo apresentado. Isso significa que o anticorpo pode reconhecer uma ampla gama de moléculas humanas MHC-A, -B e -C com afinidade muito alta, sendo relativamente insensível aos fragmentos proteicos específicos que o MHC exibe.
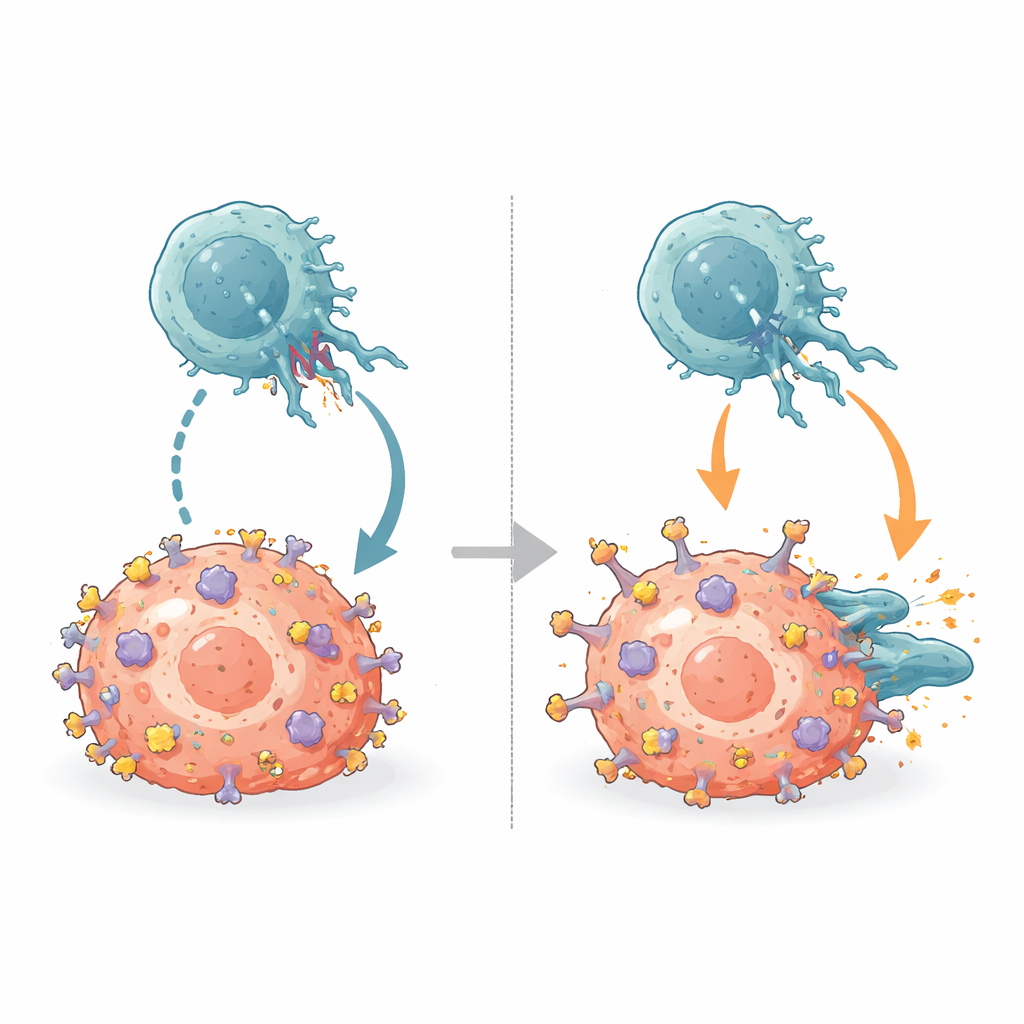
Superando os freios do sistema imune
As NK carregam receptores inibitórios chamados KIRs que normalmente se acoplam à mesma crista α2 do MHC. Ao alinhar as novas estruturas anticorpo–MHC com estruturas conhecidas de KIR–MHC, a equipe mostrou que B1.23.2 ocupa fisicamente o exato trecho do MHC que os KIRs precisam agarrar. O sítio de ligação do anticorpo e as pegadas dos KIRs se sobrepõem de forma tão extensa que ambos simplesmente não podem se ligar ao mesmo tempo. B1.23.2 também se liga ao MHC mais fortemente do que os KIRs, o que significa que vence essa disputa molecular. Como resultado, quando o anticorpo reveste as moléculas de MHC nas células tumorais, os KIRs nas NK não conseguem mais transmitir seus sinais inibitórios, deslocando o equilíbrio em direção à ativação das NK.
Ajustando o encaixe e ampliando o alcance
Embora B1.23.2 tenha como alvo principalmente a superfície conservada do MHC, os autores descobriram que pequenas diferenças no peptídeo ligado ao MHC podem ajustar sutilmente a força do anticorpo. Ao trocar sistematicamente um único resíduo de aminoácido na posição do peptídeo, eles mostraram mudanças modestes na ligação — geralmente em torno de até dez vezes — sem perder o reconhecimento geral. Também investigaram por que certos tipos comuns de MHC, como HLA-A*02:01, escapam da ligação. Ao transplantar resíduos de contato chave de uma variante de MHC responsiva para HLA-A*02:01, a equipe engenheirou versões que o anticorpo passou a reconhecer, confirmando precisamente quais posições formam a superfície crítica de ancoragem. Essas descobertas sugerem que variantes futuras de anticorpos poderiam ser projetadas para cobrir ainda mais tipos de MHC ou, alternativamente, evitar seletivamente outros.
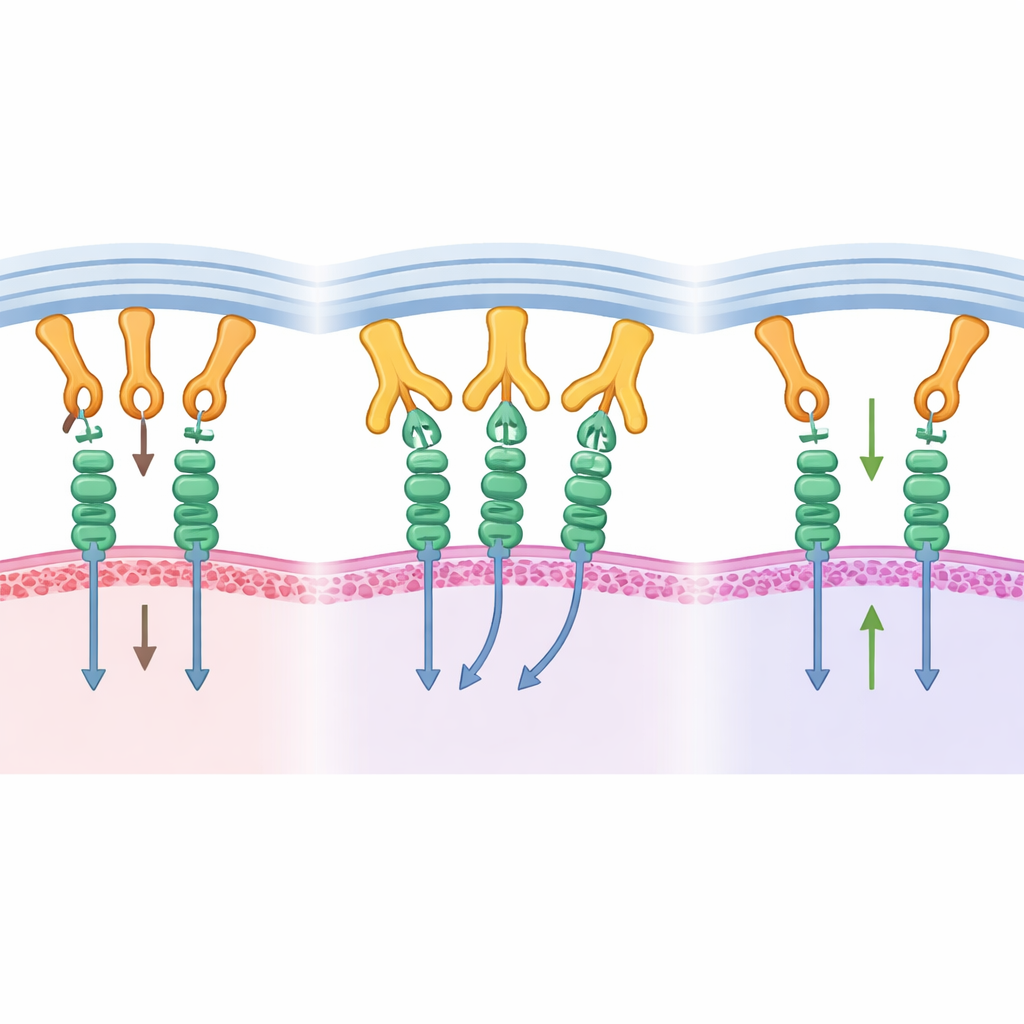
Transformando insight estrutural em controle tumoral
Esse bloqueio molecular realmente ajuda a combater tumores? Para testar isso, os pesquisadores usaram um modelo murino humanizado com um câncer pancreático humano. Eles engenheiraram uma forma de B1.23.2 que não pode sinalizar através de sua cauda Fc, de modo que quaisquer efeitos viriam principalmente do bloqueio da interação MHC–KIR. Quando os camundongos receberam o anticorpo juntamente com células NK humanas, os tumores cresceram muito mais devagar. As NK exibiram proliferação aumentada, maior atividade de vias de crescimento e sinalização, e maior produção de moléculas inflamatórias associadas à destruição de células cancerosas. Dentro dos tumores, as NK mostraram mais receptores ativadores, consistente com a liberação do constante input inibitório.
O que isso pode significar para terapias futuras contra o câncer
De forma direta, este estudo mostra como um único anticorpo pode escorregar entre as células tumorais e os freios do sistema imune, interrompendo o sinal de “não atacar” que normalmente mantém as NK silenciosas. Ao mapear a interação em resolução atômica e confirmar seus efeitos em animais, o trabalho oferece um roteiro para uma nova classe de tratamentos: anticorpos que se ligam às etiquetas de identificação do tumor em vez dos próprios receptores imunes. Esses agentes poderiam ser combinados com inibidores de checkpoint existentes ou terapias celulares para mobilizar tanto NK quanto células T, fornecendo ao sistema imune outro ângulo de ataque contra cânceres de difícil tratamento.
Citação: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Palavras-chave: células natural killer, MHC de classe I, imunoterapia contra o câncer, anticorpos monoclonais, receptores inibitórios