Clear Sky Science · pt
Migração celular confinada periódica impulsiona reorganização da cromatina parcialmente reversível em linhagens de células cancerosas
Como células cancerosas espremidas lembram o estresse sofrido
As células cancerosas que se desprendem de um tumor precisam rastejar por fendas minúsculas nos tecidos e vasos sanguíneos do corpo. Para isso, elas comprimem seu interior macio — e especialmente o núcleo, que abriga o DNA — através de espaços às vezes menores do que o próprio núcleo. Este estudo investiga o que acontece com a organização do DNA durante essas espremidas repetidas e formula uma pergunta central: o núcleo simplesmente retorna ao normal, ou conserva uma espécie de “memória mecânica” que pode facilitar a disseminação do câncer?
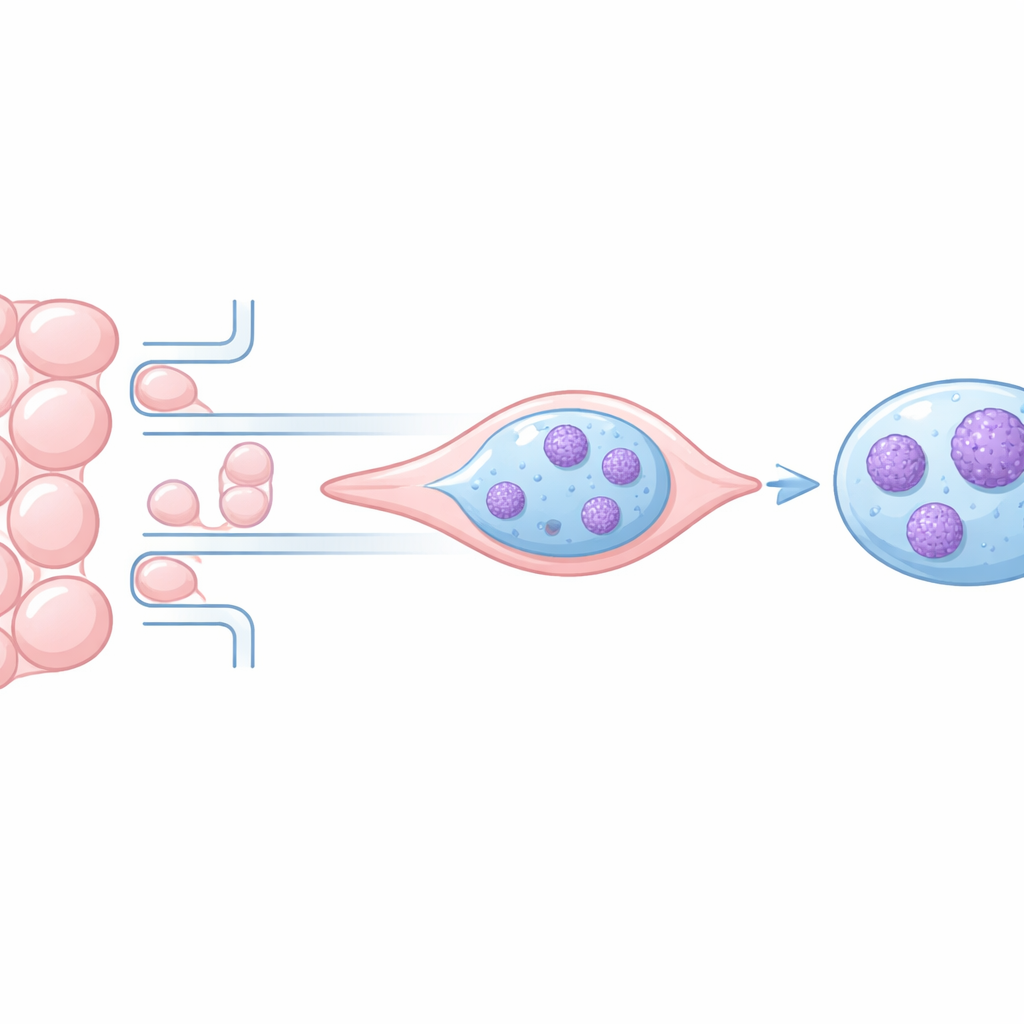
Por que o empacotamento do DNA importa quando células se movem
Dentro do núcleo, o DNA é enrolado em torno de proteínas e dobrado em cromatina, que pode estar mais frouxa ou mais condensada. Regiões mais abertas tendem a ser ativas, abrigando genes frequentemente usados, enquanto regiões muito compactas são mais silenciosas. Quando células migram por espaços estreitos, o núcleo se deforma, e trabalhos anteriores mostraram que isso pode compactar temporariamente a cromatina e até danificar o DNA. Mas não estava claro se essas alterações reverteriam por completo ou deixariam marcas duradouras que poderiam modificar o comportamento agressivo das células cancerosas.
Um labirinto minúsculo para espremer células cancerosas individuais
Os pesquisadores construíram um dispositivo microfluídico personalizado — um chip transparente contendo dezenas de canais microscópicos que alternam repetidamente entre segmentos largos e estreitos. Duas diferentes linhagens de células cancerosas, ambas geneticamente modificadas para que sua cromatina brilhe ao microscópio, foram guiadas a rastejar por esses canais usando um atrativo químico. Imagens em lapso de tempo de alta resolução permitiram à equipe acompanhar cada núcleo celular em movimento, medindo o tamanho nuclear e mapeando, quadro a quadro, aglomerados brilhantes de cromatina altamente condensada em mais de 100 células individuais.
O que acontece ao núcleo sob pressão
Sempre que uma célula entrava numa constrição estreita, seu núcleo encolhia abruptamente em área projetada, refletindo uma redução reversível no volume nuclear. Ao mesmo tempo, a fração do núcleo ocupada por cromatina altamente condensada disparava — frequentemente de duas a três vezes — e depois retornava ao nível basal quando a célula saía para uma região mais larga. Esse padrão repetiu-se ao longo de várias constrições sucessivas e em ambos os tipos celulares, sugerindo que a quantidade global de cromatina densa é uma resposta flexível e de curto prazo ao estresse mecânico, em vez de uma mudança permanente. No entanto, uma análise mais detalhada dos padrões de fluorescência revelou que pixels com intensidade muito alta e muito baixa aumentaram durante a compressão, sugerindo uma rearrumação interna mais complexa do que uma simples compactação uniforme.
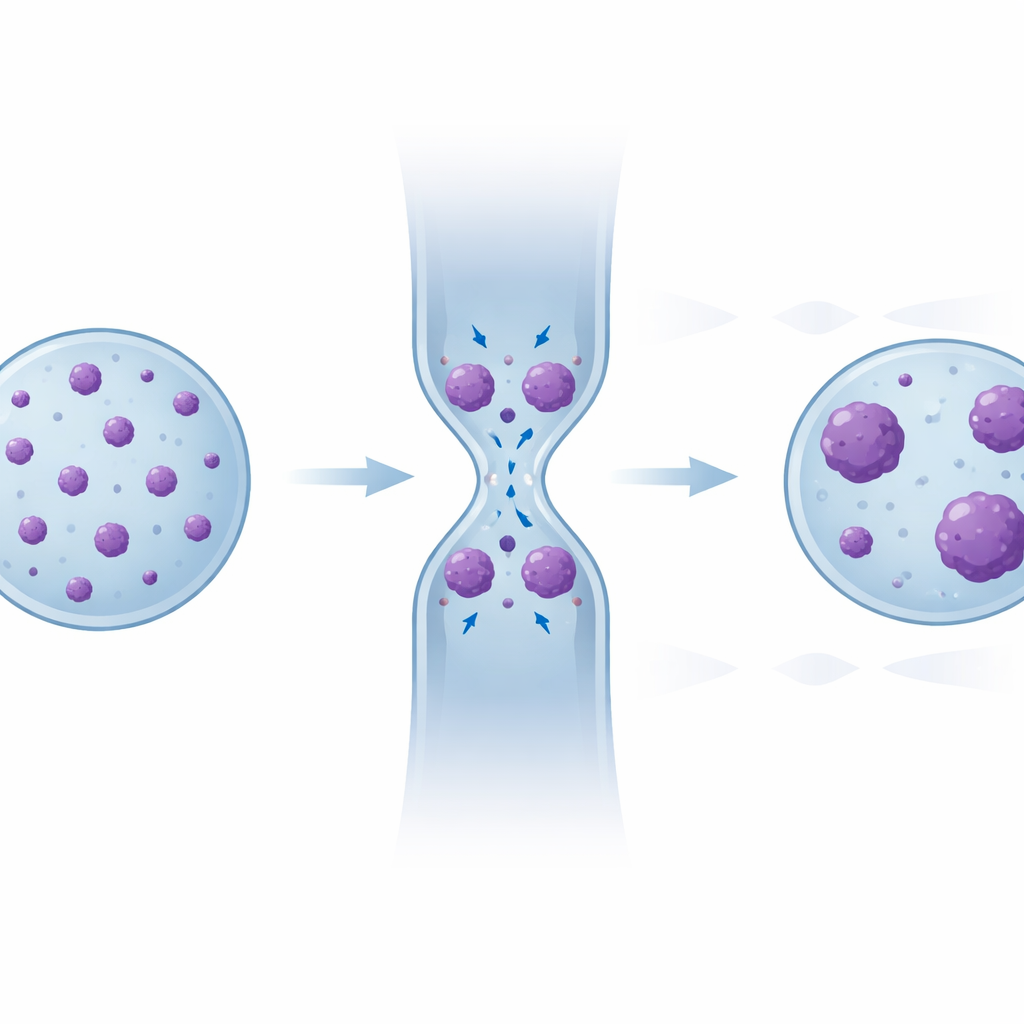
Memória escondida no padrão dos aglomerados de DNA
Para revelar essa reorganização oculta, a equipe examinou cada aglomerado condensado de cromatina individual — seu tamanho e quantos desses aglomerados cada núcleo continha — antes, durante e depois do confinamento. Durante a compressão, aglomerados pequenos tendiam a se fundir em outros maiores. Depois que o núcleo relaxava, a área condensada total retornava ao nível original, mas o padrão não: em comparação ao estado inicial, células que passaram por várias constrições exibiam, no geral, menos aglomerados, tendendo para tamanhos maiores. Comparações estatísticas confirmaram que as distribuições nas regiões de “recuperação” posteriores se pareciam cada vez mais com as observadas durante o confinamento. Marcação por imunofluorescência mostrou ainda que muitas dessas regiões densas se sobrepunham a marcas estabelecidas de cromatina “silenciosa”, e um modelo computacional que representava a cromatina como um polímero interativo reproduziu essa relaxação parcial (mas não completa) simplesmente a partir da física de segmentos de DNA adesivos trazidos para perto pela deformação.
O que isso significa para a disseminação do câncer e futuras terapias
Em termos práticos, o estudo mostra que, quando núcleos de células cancerosas são repetidamente espremidos, o empacotamento do DNA se comporta como uma bola de estresse com memória. O núcleo pode recuperar seu tamanho, e a quantidade total de compactação pode ser restabelecida, mas o padrão detalhado dos aglomerados de DNA denso não retorna por completo ao estado original. Após muitos ciclos de compressão, o núcleo acaba com menos regiões densas, porém maiores, o que pode alterar quais genes ficam mais ou menos acessíveis. Essa “memória mecânica” poderia ajudar células cancerosas a tolerar melhor deformações futuras enquanto invadem novos tecidos. Entender e, eventualmente, atacar essa ligação entre forças físicas e organização do DNA pode abrir novas formas de limitar a metástase, interrompendo como as células cancerosas se adaptam ao estresse mecânico.
Citação: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Palavras-chave: migração celular confinada, condensação da cromatina, mecânica nuclear, memória mecânica, metástase do câncer