Clear Sky Science · pt
PTBP1 apoia a espermatogênese de camundongos facilitando a organização do citoesqueleto via via mTORC2–PKCα em células de Sertoli
Por que este estudo importa para a fertilidade masculina
A infertilidade masculina muitas vezes parece misteriosa, mas em sua essência depende de uma parceria bem ajustada entre os espermatozoides em desenvolvimento e as células “ordenhadoras” que os sustentam. Este estudo investiga um dos auxiliares moleculares ocultos dentro dessas células de suporte e mostra como sua falha pode interromper a produção de espermatozoides. Entender essa camada escondida de controle pode apontar caminhos para novos diagnósticos ou tratamentos para certas formas de infertilidade masculina.
As células de suporte que tornam o esperma possível
Os espermatozoides são produzidos dentro de longos tubos enrolados no testículo chamados túbulos seminíferos. Revestindo esses tubos estão as células de Sertoli, um tipo especializado de célula de suporte que acolhe as células germinativas em desenvolvimento, as nutre e as orienta enquanto se dividem e amadurecem em espermatozoides. As células de Sertoli também constroem uma parede protetora conhecida como barreira sangue–testículo, que separa as células em estágio inicial do sistema imunológico. Para realizar tudo isso, elas dependem de um andaime interno de filamentos de actina e microtúbulos que se remodela constantemente conforme ondas de células germinativas percorrem os túbulos. Se esse andaime for perturbado, a barreira vaza e as células germinativas em maturação podem se desprender ou morrer, ameaçando a fertilidade.
Um pequeno gerenciador de RNA com um grande trabalho
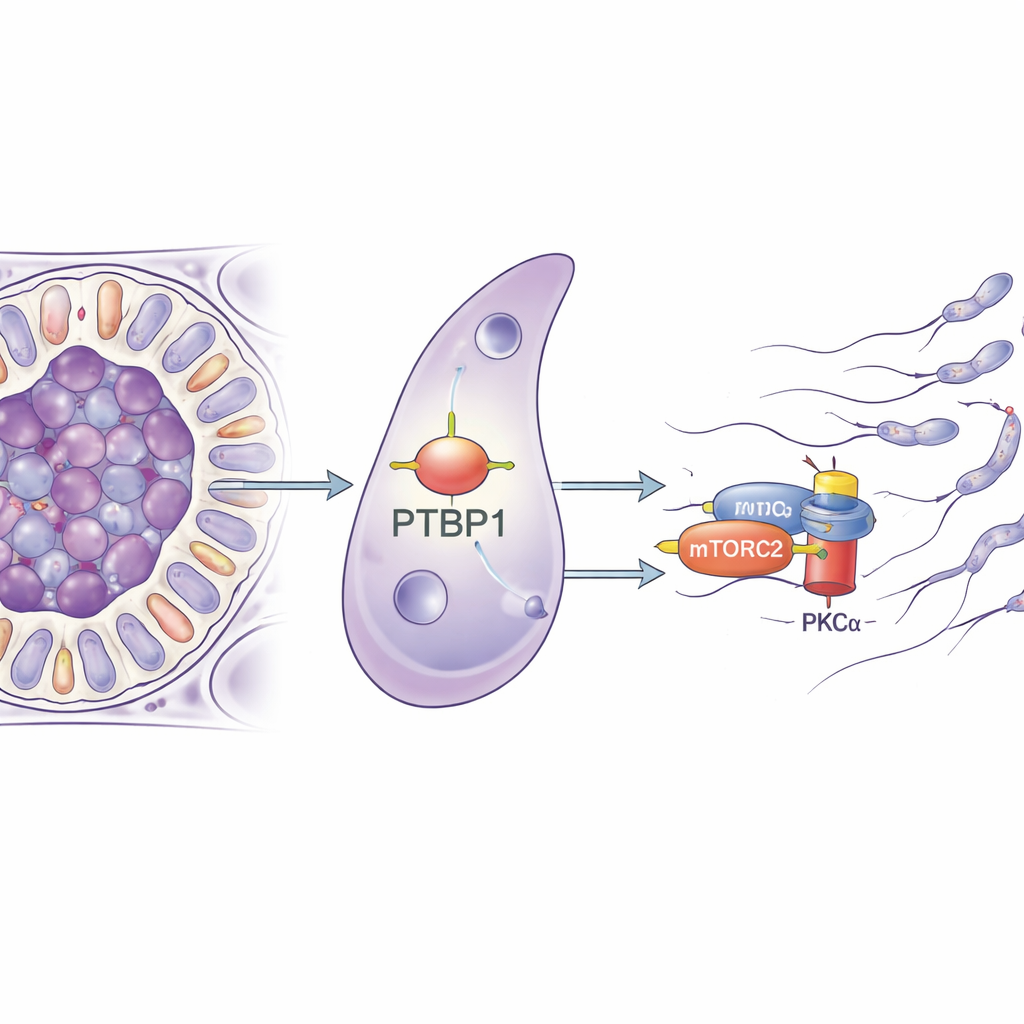
Os pesquisadores concentraram-se em uma proteína chamada PTBP1, mais conhecida por seu papel em gerenciar moléculas de RNA dentro das células — decidindo como os genes são spliceados, a estabilidade de suas mensagens e com que eficiência são traduzidos em proteína. PTBP1 é abundante tanto em células germinativas quanto em células de Sertoli, e trabalhos anteriores mostraram que removê‑la das células germinativas prejudica a produção de esperma. Neste estudo, a equipe deletou especificamente o PTBP1 apenas nas células de Sertoli em camundongos. À primeira vista, os animais jovens pareciam normais, mas ao atingirem a maturidade sexual os testículos encolheram, o número de espermatozoides no epidídimo despencou e nenhum dos machos conseguiu gerar descendência, revelando uma perda completa da fertilidade.
Quando o andaime celular desaba
Exames microscópicos dos testículos desses camundongos mostraram que a espermatogênese parou pela metade. Muitos túbulos continham espaços vazios, aglomerados anormais de núcleos de células germinativas fundidos e escassez de espermatozoides totalmente alongados. Os núcleos das células de Sertoli, que normalmente ficam junto à parede externa dos túbulos, frequentemente estavam deslocados em direção ao centro, sugerindo que essas células de suporte estavam perdendo a adesão à estrutura ao redor. Colorações para componentes-chave das junções e proteínas estruturais confirmaram que a barreira sangue–testículo estava enfraquecida e que os habituais feixes compactos de filamentos de actina foram substituídos por fios desorganizados e excessivamente intensos estendendo‑se da base ao centro do túbulo. Uma molécula traçadora que normalmente permanece no “lado sanguíneo” da barreira vazou para o interior dos túbulos, demonstrando diretamente a ruptura da barreira.
Rastreando a falha até um centro de sinalização
Para entender como uma proteína de ligação ao RNA poderia levar a problemas mecânicos tão severos, a equipe purificou células de Sertoli e analisou quais genes mudaram sua atividade quando PTBP1 estava ausente. Muitos dos genes afetados estavam envolvidos no controle do esqueleto celular e em como as células aderem umas às outras, apontando para um defeito de remodelamento amplo. Em seguida, os pesquisadores puxaram as moléculas de RNA que se ligam fisicamente ao PTBP1 e descobriram que ele se prende à mensagem para Rictor, um componente central de um complexo de sinalização chamado mTORC2. Esse complexo, por sua vez, ativa uma enzima chamada PKCα que modela os filamentos de actina. Em células de Sertoli sem PTBP1, a quantidade da proteína RICTOR caiu, e a PKCα estava muito menos ativa, embora o nível do RNA de Rictor praticamente não tenha mudado. Isso sugere fortemente que PTBP1 ajuda as células de Sertoli a produzir proteína RICTOR suficiente a partir de sua mensagem de RNA, mantendo assim a via mTORC2–PKCα em funcionamento.
Resgatando o andaime ao restaurar o sinal
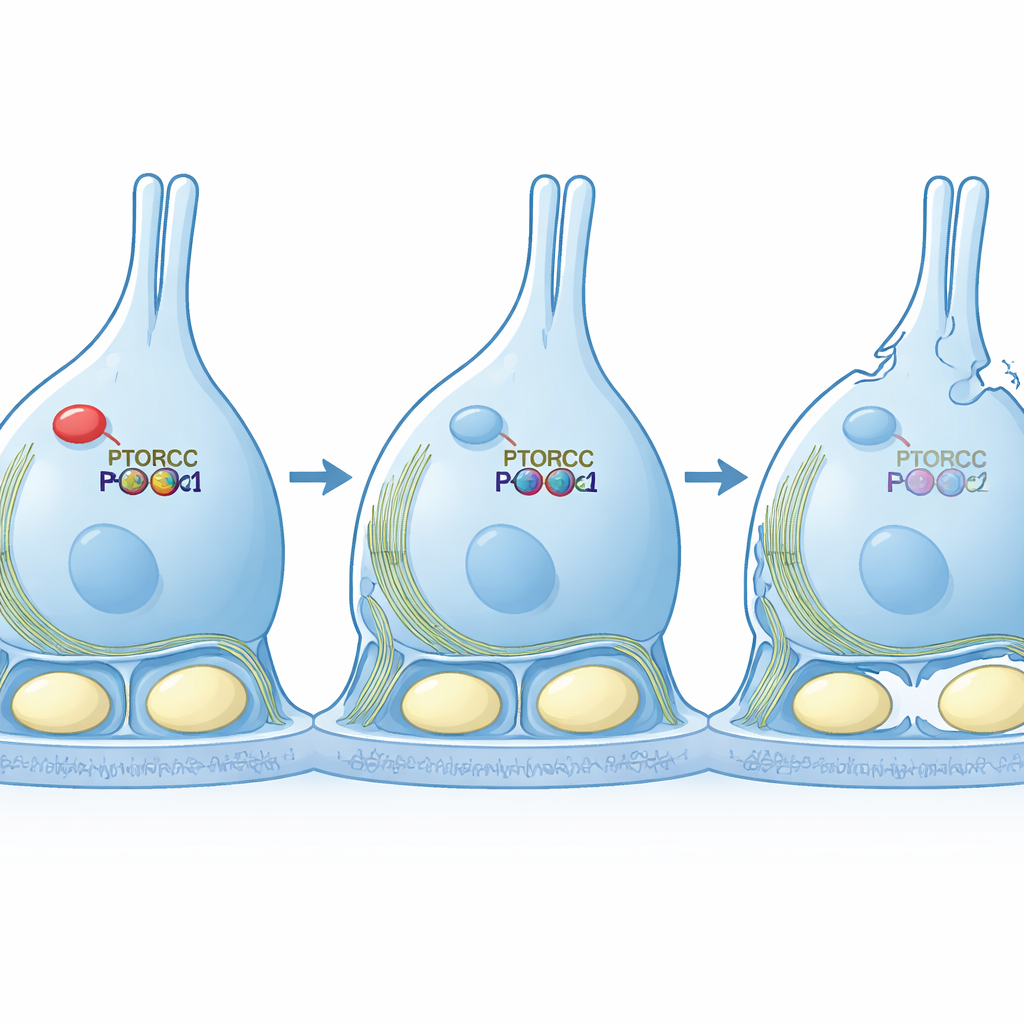
A equipe então passou para modelos em cultura celular para testar a causalidade. Quando reduziram o PTBP1 em uma linhagem celular semelhante a Sertoli, as células esticaram-se em formas longas e finas e exibiram uma rede de actina embaralhada — marcas de sinalização mTORC2 enfraquecida. Importante, quando forçaram essas células a produzir uma versão permanentemente ativa da PKCα, as células recuperaram sua forma normal e compacta e estruturas de actina mais ordenadas, mesmo com níveis baixos de RICTOR. Esse experimento de resgate mostra que o papel principal do PTBP1 neste contexto é manter a via mTORC2–PKCα forte o suficiente para organizar o andaime interno da célula.
O que isso significa para entender a infertilidade
Em termos simples, este trabalho revela uma cadeia de dependência dentro do testículo: PTBP1 ajuda as células de Sertoli a montar um centro de sinalização chave; esse centro organiza seu citoesqueleto; e um citoesqueleto intacto permite que elas prendam e protejam os espermatozoides em desenvolvimento. Rompa a cadeia no PTBP1, e as células de Sertoli perdem sua estrutura, a barreira protetora falha e o desenvolvimento dos espermatozoides desaba, resultando em infertilidade masculina. Embora esta pesquisa tenha sido feita em camundongos, as mesmas moléculas estão presentes em humanos, o que levanta a possibilidade de que defeitos sutis no controle de RNA dentro das células de Sertoli possam explicar alguns casos inexplicados de infertilidade masculina e oferece um novo conjunto de alvos moleculares para estudos futuros.
Citação: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Palavras-chave: fertilidade masculina, Células de Sertoli, espermatogênese, citoesqueleto, proteínas de ligação ao RNA