Clear Sky Science · pt
Regulação negativa da via NF-κB pela ligase de ubiquitina Nedd4-1(NE)
Por que é importante desligar a inflamação
Nosso sistema imunológico depende de explosões rápidas de inflamação para combater infecções e curar ferimentos, mas essas mesmas respostas podem danificar tecidos e alimentar o câncer se permanecerem ativadas por tempo demais. Este artigo explora como células humanas e de outros primatas evitam esse perigo usando um “freio” embutido recém-caracterizado que silencia um dos principais sistemas de alarme do corpo quando seu trabalho termina.
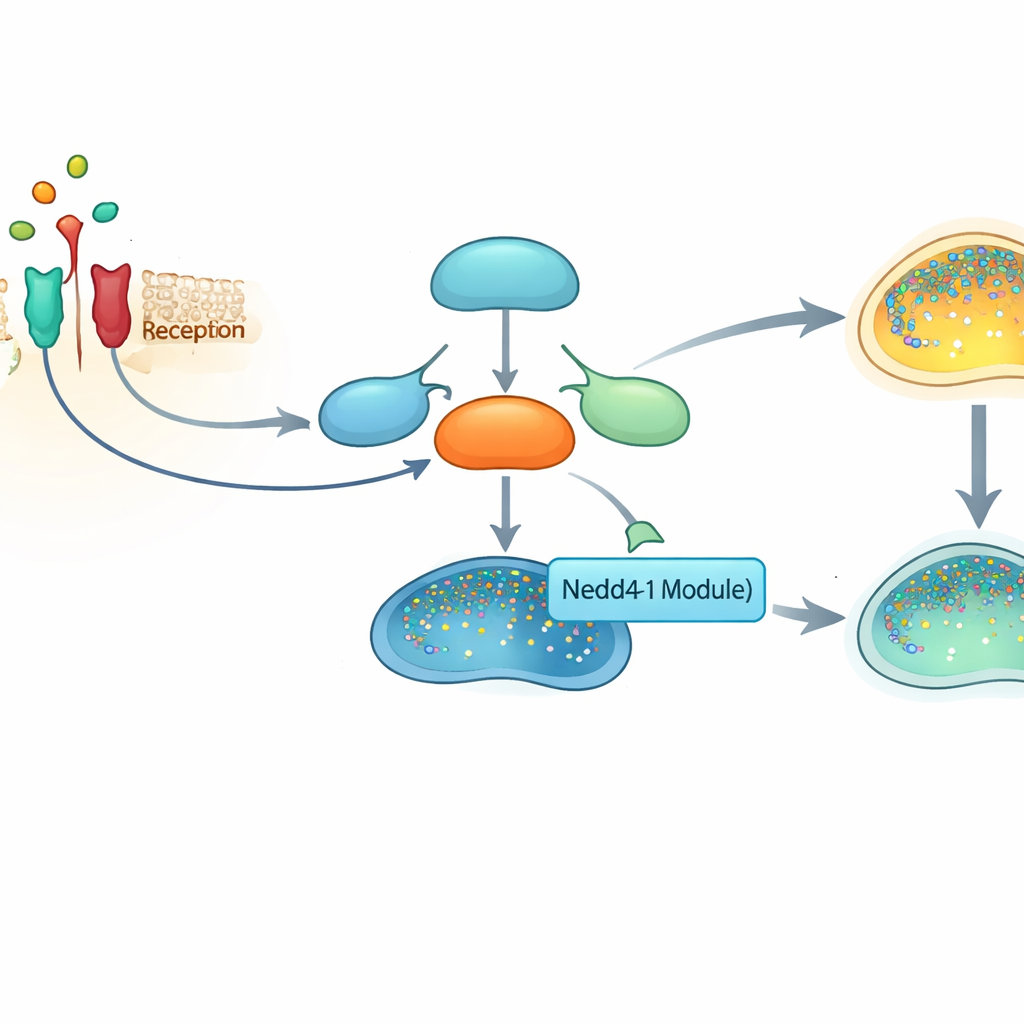
Um interruptor de alarme central em nossas células
No centro desta história está o NF-κB, uma família de proteínas que atua como um interruptor mestre para centenas de genes envolvidos em inflamação, sobrevivência celular e imunidade. Quando as células detectam sinais de estresse, como a molécula inflamatória TNFα, uma cascata de eventos libera o NF-κB de suas “chaperonas” proteicas no interior fluido da célula e permite que ele entre no núcleo, onde ativa genes pró-inflamatórios e pró-sobrevivência. Como essa via é tão poderosa, as células devem ajustar com precisão tanto sua ativação quanto seu desligamento. A falha em desligá-la tem sido associada a doenças inflamatórias crônicas e a muitos cânceres.
Um freio exclusivo de primatas no alarme
Os pesquisadores concentraram-se em Nedd4-1, membro de uma grande família de enzimas que marcam outras proteínas com uma pequena molécula chamada ubiquitina. Essa marca frequentemente sinaliza proteínas para destruição ou realocação dentro da célula, remodelando redes de sinalização. Uma variante de splicing previamente descoberta de Nedd4-1, denominada Nedd4-1(NE), é encontrada apenas em primatas e carrega um longo segmento extra em sua extremidade dianteira que altera sua localização na célula e o que ela reconhece. Em contraste com a forma padrão de Nedd4-1, que pode na verdade aumentar a atividade do NF‑κB por meio de outros parceiros, a equipe descobriu que Nedd4-1(NE) tem o efeito oposto: ele atenua a sinalização do NF‑κB, especialmente após exposição prolongada ao TNFα.
Dupla via para conter o NF-κB
Para descobrir como esse freio funciona, os autores usaram marcação por proximidade e métodos de pull‑down de proteínas para ver quais moléculas se associam fisicamente a Nedd4-1(NE). Eles identificaram componentes-chave da via NF‑κB, incluindo a quinase IKKβ e a proteína precursora NF‑κB1 (também chamada p105). Experimentos de seguimento mostraram que Nedd4-1(NE) adiciona marcas de ubiquitina à IKKβ, levando à sua degradação. Com menos IKKβ disponível, seu alvo habitual IκBα deixa de ser fosforilado e degradado com a mesma eficiência. Como resultado, IκBα permanece mais estável e mantém a subunidade ativa do NF‑κB, p50, sequestrada no citosol, impedindo sua entrada no núcleo para ativar genes inflamatórios.
Uma transferência guiada por adaptador para o freio
Nedd4-1(NE) também atua mais a jusante limitando os níveis do próprio NF‑κB1. Nesse caso, a enzima não age sozinha: ela colabora com outra proteína ligada à ubiquitinação chamada KPC1. KPC1 ajuda a processar o precursor NF‑κB1 p105 na forma ativa p50 e reside em compartimentos celulares conhecidos como endossomos tardios, onde Nedd4-1(NE) também é encontrado. A equipe demonstrou que Nedd4-1(NE) pode ubiquitinar KPC1 e que esse KPC1 modificado funciona como um adaptador, recrutando NF‑κB1 para Nedd4-1(NE) nos endossomos tardios. Esse complexo triplo promove a desestabilização tanto de p105 quanto de p50, novamente reduzindo o conjunto de NF‑κB que pode alcançar o núcleo.
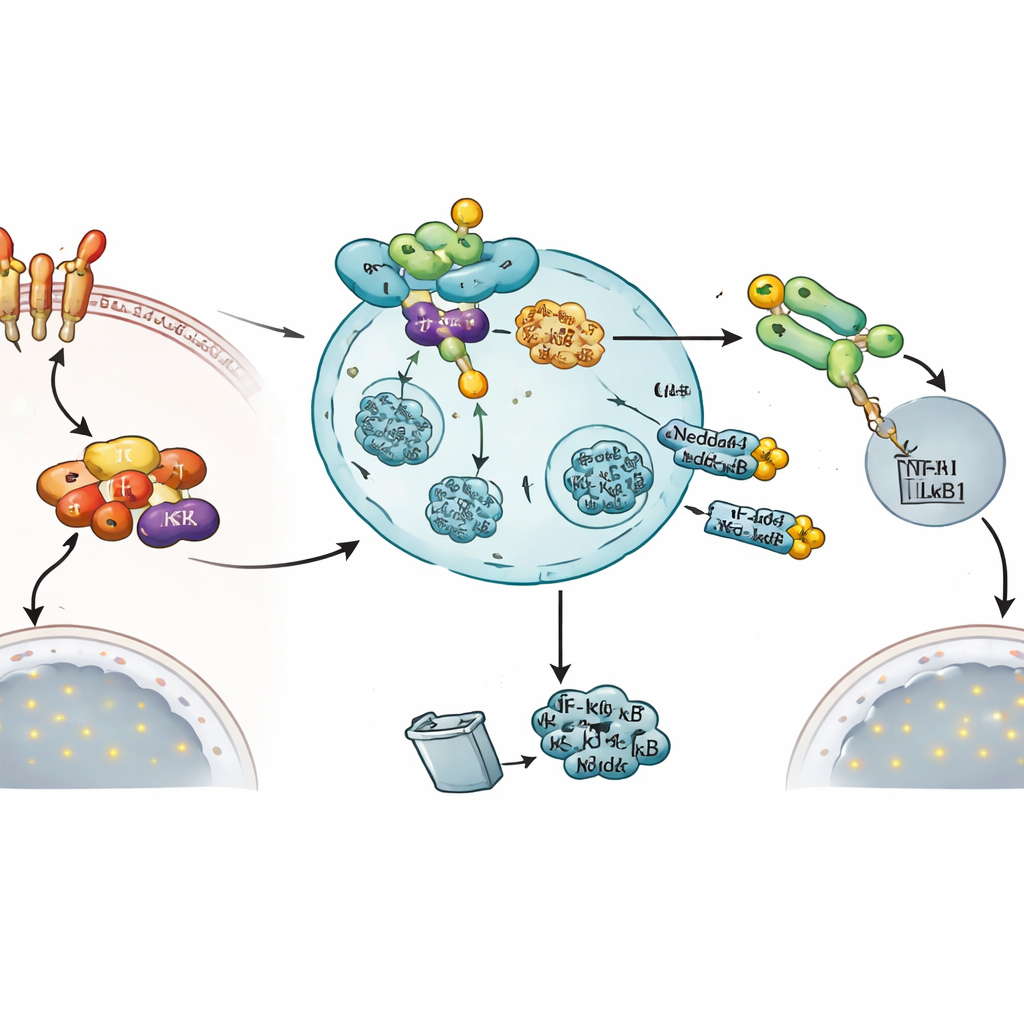
Um circuito de feedback embutido para encerrar o sinal
De maneira marcante, o próprio sinal que ativa o NF‑κB também parece induzir esse freio. Quando células foram tratadas com TNFα, os níveis do RNA mensageiro de Nedd4-1(NE) aumentaram dramaticamente, enquanto a forma padrão de Nedd4-1 não se alterou. Medidas funcionais sustentaram a ideia de que Nedd4-1(NE) é uma válvula de desligamento: aumentar Nedd4-1(NE) ativo reduziu o movimento de NF‑κB1 para o núcleo, diminuiu a atividade de um gene repórter responsivo ao NF‑κB e reduziu a expressão de um gene inflamatório regulado por NF‑κB, TNFAIP3. Em conjunto, esses achados delineiam um loop de feedback negativo no qual a ativação da via NF‑κB acaba elevando Nedd4-1(NE), que então mira dois nós críticos — IKKβ e NF‑κB1 — para trazer a resposta inflamatória de volta ao equilíbrio.
O que isso significa para saúde e doença
Para um público geral, a mensagem principal é que nossas células incorporam um mecanismo de segurança adicional, específico de primatas, para impedir que a sinalização inflamatória escape ao controle. Ao marcar seletivamente e aparar componentes centrais do sistema NF‑κB, Nedd4-1(NE) ajuda a encerrar a resposta ao TNFα e pode contribuir para o equilíbrio imunológico a longo prazo. Compreender esse freio embutido pode abrir novas vias para tratar doenças em que o NF‑κB está cronicamente hiperativo, como distúrbios autoimunes e certos cânceres, ao sugerir maneiras de imitar ou potencializar esse processo natural de desligamento.
Citação: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Palavras-chave: Sinalização NF-kB, inflamação, ligase de ubiquitina, Nedd4-1(NE), TNF alfa