Clear Sky Science · pt
Notch3 regula a plasticidade fenotípica de pericitos no câncer colorretal
Por que os vasos sanguíneos ao redor dos tumores importam
O câncer colorretal está entre os tumores mais comuns e letais no mundo, e ainda assim a maioria das terapias mira diretamente as células tumorais, muitas vezes negligenciando o sistema de suporte ao redor que ajuda o tumor a crescer. Este artigo foca em um grupo menos conhecido de células de suporte chamadas pericitos, que envolvem pequenos vasos sanguíneos. Ao revelar como um interruptor de sinalização chamado Notch3 altera o comportamento dos pericitos, os autores mostram como o suprimento sanguíneo do tumor pode ser direcionado para vasos mais permeáveis e caóticos que favorecem o câncer, ou para vasos mais normais que podem retardar a doença e melhorar o tratamento. 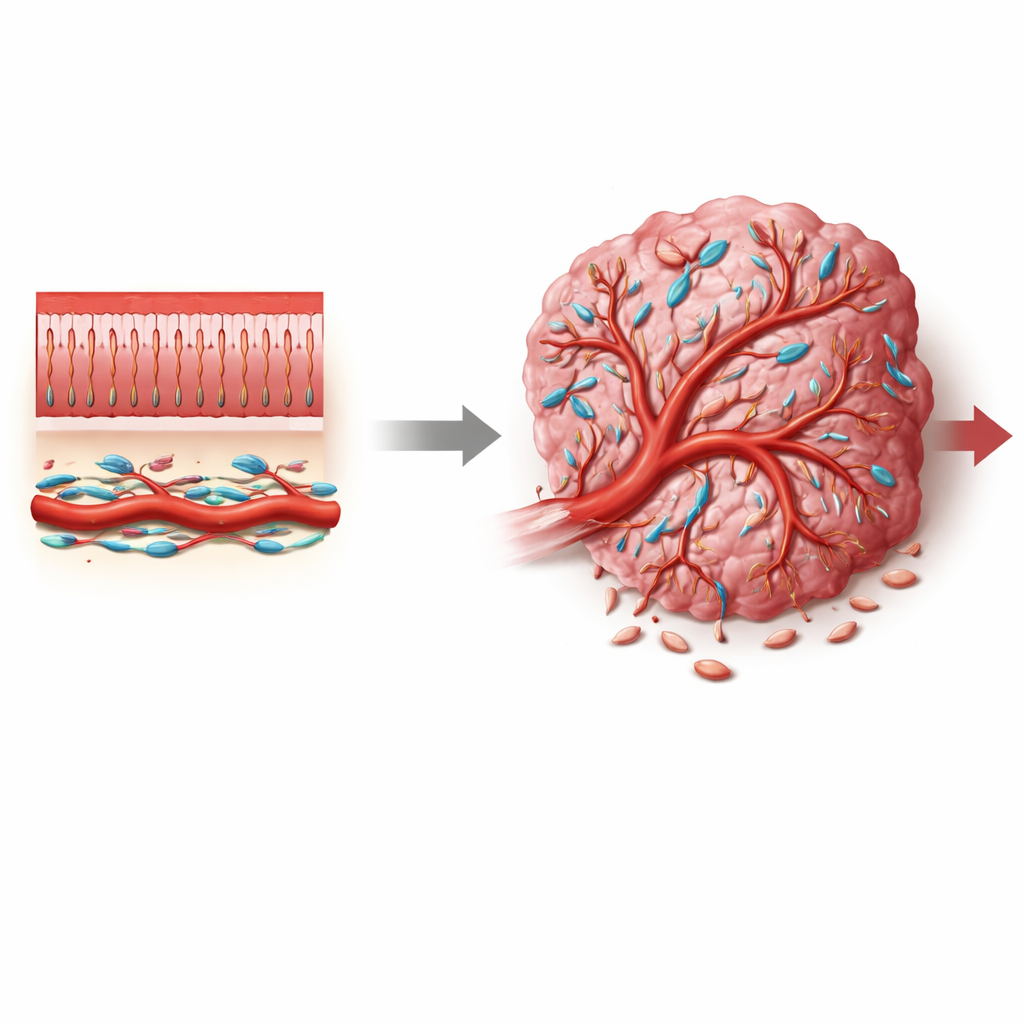
Os ajudantes ocultos ao redor dos vasos tumorais
Vasos sanguíneos são mais do que tubos vazios. Em tecidos saudáveis, pequenos vasos são firmemente envoltos por pericitos — células especializadas que estabilizam as paredes vasculares, controlam o fluxo sanguíneo e impedem vazamentos. Em tumores, no entanto, esses pericitos frequentemente apresentam aparência e comportamento diferentes: podem se desprender, proliferar ou mudar de identidade, contribuindo para a vasculatura anômala e permeável típica dos cânceres. Em tumores colorretais, onde o microambiente está repleto de fibroblastos, células imunes e células vasculares, não estava claro de onde vêm os pericitos associados ao tumor, quais estados eles adotam e quais sinais moleculares os empurram para funções que promovem o tumor.
Rastreando pericitos durante a formação do tumor
Para acompanhar os pericitos ao longo do tempo, os pesquisadores usaram modelos murinos de câncer colorretal associado à colite, nos quais puderam “marcar” geneticamente tipos celulares específicos e observar seu destino. Eles mostraram que os pericitos encontrados nos tumores se originam em grande parte de pericitos residentes do tecido que se expandem e proliferam durante o desenvolvimento do câncer, em vez de virem de fontes distantes como a medula óssea. Usando sequenciamento de RNA de célula única avançado, catalogaram dezenas de milhares de células do estroma de tumores de camundongos e cólon normal e descobriram que os pericitos estão significativamente enriquecidos no microambiente tumoral. Eles também identificaram expansão semelhante de pericitos em vários conjuntos de dados de câncer colorretal humano, ressaltando que isso não é apenas um fenômeno específico de camundongos.
Um interruptor molecular que altera o comportamento dos pericitos
Em seguida, a equipe investigou quais sinais moldam o comportamento dos pericitos dentro dos tumores e encontrou que o Notch3 — um receptor que permite a comunicação entre células vizinhas — está especialmente ativo nos pericitos tumorais. Análises computacionais de comunicação célula–célula sugeriram que os pericitos tanto enviam quanto recebem sinais relacionados ao Notch, especialmente por meio de parceiros em células dos vasos sanguíneos. Ao ativar artificialmente o Notch3 em pericitos, os pesquisadores observaram que essas células proliferavam mais, mas expressavam menos proteínas contráteis normalmente associadas ao papel de estabilizar vasos. Os vasos tumorais nesses camundongos tornaram-se maiores, mais permeáveis e revestidos por mais células endoteliais proliferativas, indicando uma vasculatura menos estável. Inversamente, a deleção de Notch3 reduziu a proliferação endotelial, diminuiu o tamanho dos vasos e reduziu o vazamento, sugerindo um deslocamento em direção a vasos mais normalizados sem alterar dramaticamente o número ou o tamanho inicial dos tumores. 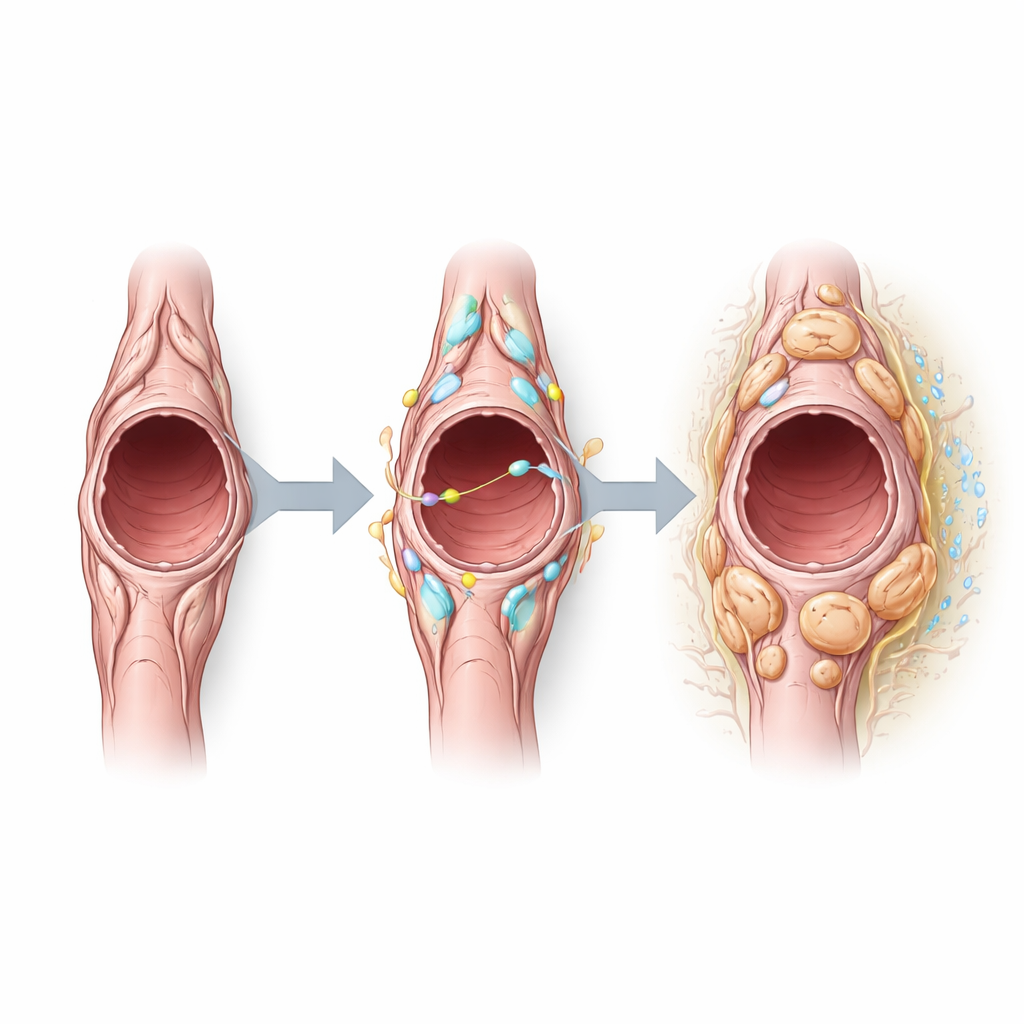
Muitas faces dos pericitos dentro dos tumores
Além de mudanças simples de liga/desliga, o estudo revelou que os pericitos tumorais existem em vários estados distintos. Alguns subgrupos exibiam características de células altamente contráteis, outros produziam grande quantidade de matriz extracelular, alguns mostravam traços inflamatórios, e um subconjunto até carregava assinaturas normalmente vistas em células endoteliais. A atividade de Notch3 não era distribuída de forma uniforme: estava enriquecida em uma população “sintética” ou produtora de matriz e baixa no subconjunto mais contrátil. Análises de trajetórias sugeriram que os pericitos podem migrar de um estado contrátil para um estado sintético e proliferativo conforme a atividade de Notch3 aumenta. Quando os autores examinaram dados de câncer colorretal humano, encontraram um espectro comparável de estados de pericitos e novamente observaram maior atividade de um gene alvo de Notch3 em pericitos associados ao tumor e proliferativos, espelhando os resultados em camundongos.
Transformando o caos vascular em uma oportunidade terapêutica
No conjunto, o trabalho pinta o Notch3 como um botão-chave que ajusta a identidade dos pericitos e, por meio deles, a estrutura e a função dos vasos sanguíneos tumorais. Alta atividade de Notch3 empurra os pericitos para um estado proliferativo e menos contrátil ligado a vasos ampliados e permeáveis que favorecem a progressão tumoral. Baixa atividade de Notch3 associa-se a pericitos mais contráteis, endotélio mais calmo e vasculatura mais normalizada que pode restringir o crescimento tumoral e melhorar a entrega de fármacos. Ao direcionar o Notch3 especificamente em pericitos, terapias futuras poderiam desviar os vasos tumorais do caos para a estabilidade, oferecendo um novo ângulo para tratar câncer colorretal avançado em combinação com medicamentos existentes.
Citação: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Palavras-chave: câncer colorretal, microambiente tumoral, pericitos, sinalização Notch3, vasos sanguíneos tumorais