Clear Sky Science · pt
TRIM47 endotelial regula a integridade da barreira hematoencefálica e a cognição via a via de sinalização KEAP1/NRF2 em camundongos
Por que proteger os pequenos vasos do cérebro importa
A doença cerebral de pequenos vasos é um problema discreto, porém persistente, no cérebro. Ela danifica os menores vasos sanguíneos, aumenta o risco de AVC e corrói gradualmente memória e raciocínio, mas os médicos ainda não dispõem de tratamentos que atinjam suas causas biológicas fundamentais. Este estudo investiga uma proteína específica, TRIM47, encontrada nas células que revestem os vasos cerebrais, para responder a uma pergunta simples porém crucial: ela ajuda a manter a barreira hematoencefálica intacta, e isso importa para a cognição?
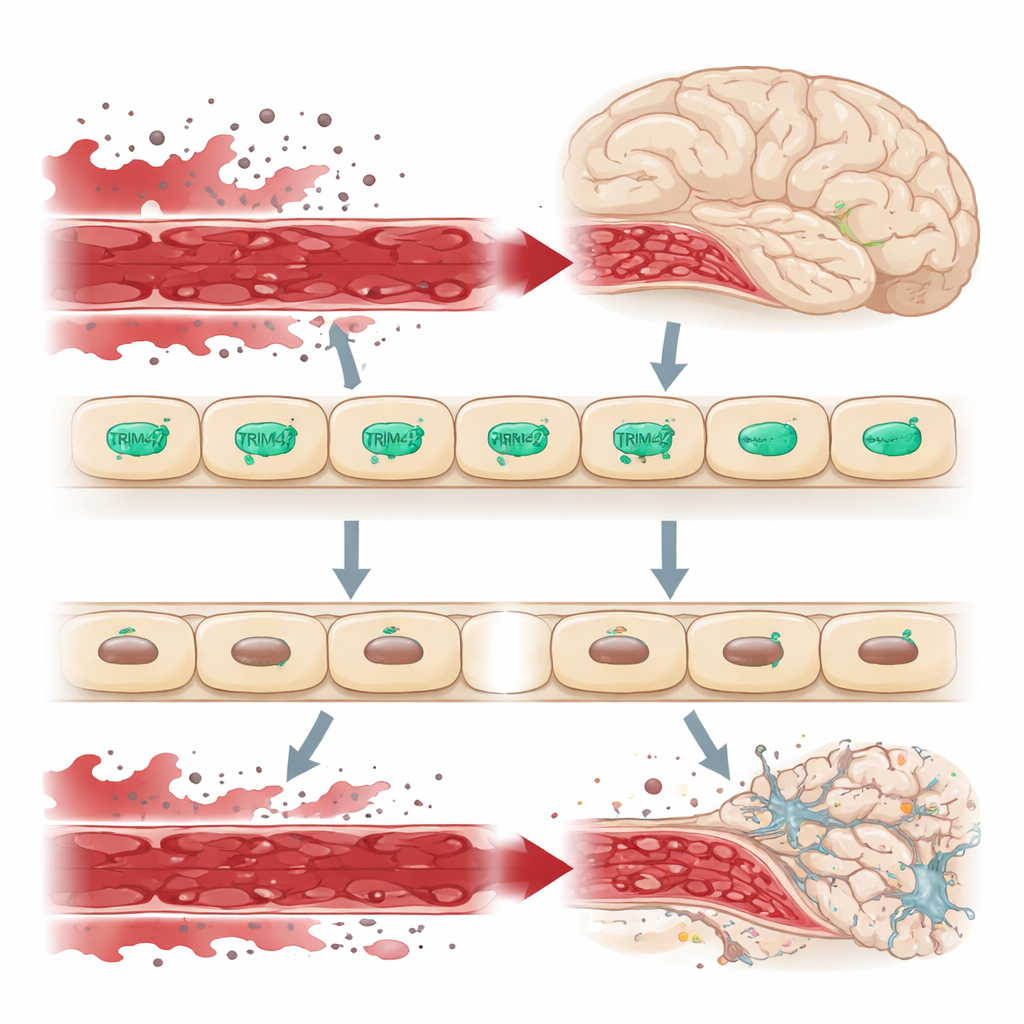
Um guardião na fronteira do cérebro
O cérebro é protegido da circulação sistêmica pela barreira hematoencefálica, um revestimento de células endoteliais muito selado que controla estritamente o que pode entrar no tecido cerebral. Quando essa barreira vaza, moléculas nocivas do sangue penetram no cérebro, estressando neurônios e células de suporte e contribuindo para condições como a demência. Estudos genéticos em grandes populações humanas apontaram um trecho de DNA que contém o gene TRIM47 como uma região de risco para a doença cerebral de pequenos vasos. O TRIM47 é especialmente ativo em células endoteliais cerebrais, sugerindo que pode ser um guardião importante dessa barreira.
Como o TRIM47 protege as células do estresse oxidativo
Os autores primeiro estudaram células endoteliais humanas do cérebro cultivadas em laboratório e reduziram os níveis de TRIM47 usando interferência por RNA. Isso desencadeou amplas mudanças na atividade gênica, com a rede mais fortemente afetada centrada em NRF2, um regulador mestre das defesas antioxidantes celulares. Em condições normais, o NRF2 é mantido sob controle por outra proteína, KEAP1, que o direciona para degradação. A equipe mostrou que o TRIM47 se liga ao KEAP1 e ajuda a impedir a degradação do NRF2. Com TRIM47 presente, o NRF2 pode se acumular, mover-se para o núcleo e ativar genes que desintoxicam espécies reativas de oxigênio. Quando o TRIM47 é perdido, os níveis de NRF2 caem, os genes antioxidantes ficam menos ativos e as células endoteliais tornam-se mais vulneráveis ao estresse oxidativo.
De vasos vazando a problemas de memória em camundongos
Para ver como esse mecanismo se manifesta em um cérebro vivo, os pesquisadores criaram camundongos sem o gene Trim47 em todo o organismo, e outra linhagem em que o Trim47 podia ser deletado apenas em células endoteliais. Animais adultos de ambos os modelos desenvolveram problemas claros de aprendizagem espacial e memória, falhando em tarefas como o labirinto em Y e o teste da água de Morris, apesar de movimentação normal. O exame de seus cérebros revelou que a barreira hematoencefálica havia se tornado permeável: pequenos traçadores fluorescentes e proteínas sanguíneas escaparam dos vasos para o tecido circundante. Proteínas-chave de “selagem” que formam junções apertadas e de adesão entre as células endoteliais, especialmente Claudin-5 e Occludina, foram reduzidas. Astrócitos próximos, as células de suporte em forma de estrela que reagem rapidamente a lesões, tornaram-se ativados, embora houvesse poucos sinais de inflamação ampla ou perda neuronal nessa fase.
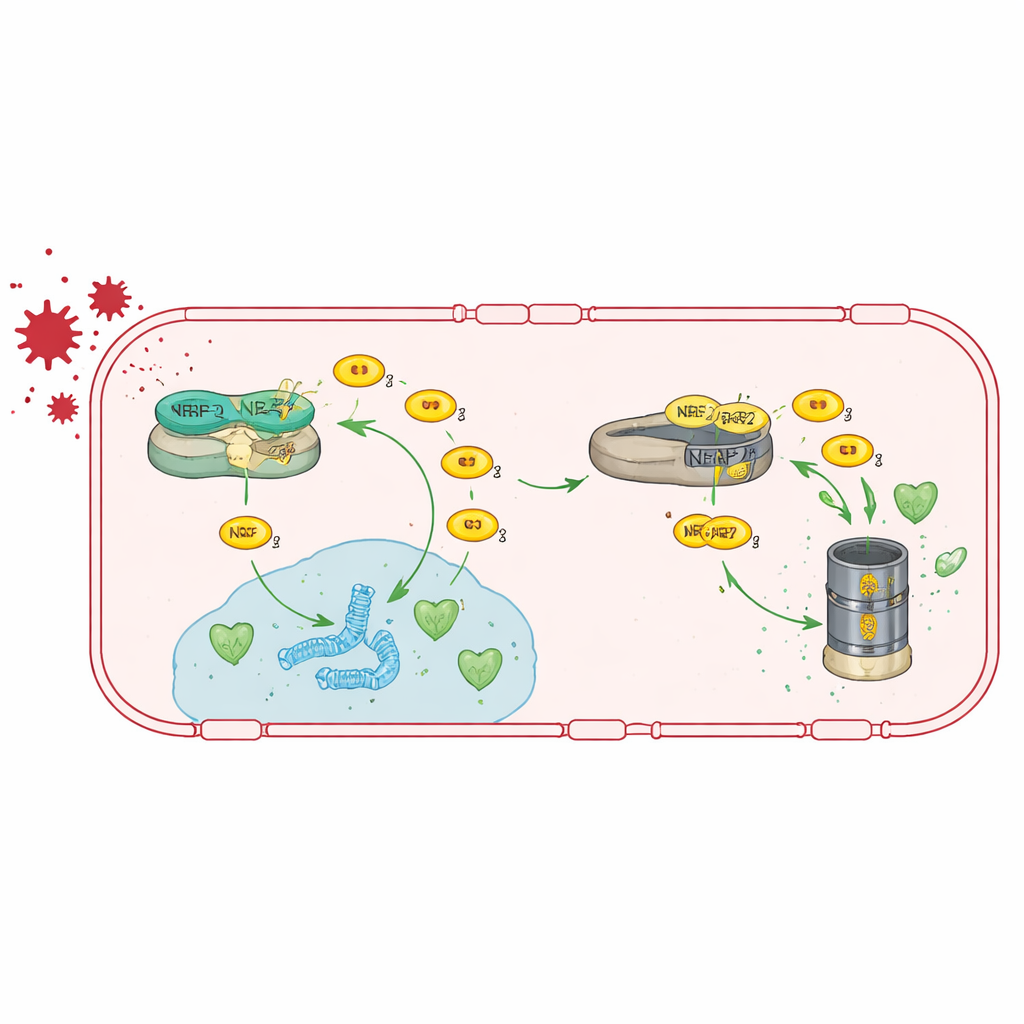
Reativando a via antioxidante
Como o TRIM47 atua principalmente ao reforçar a atividade do NRF2, a equipe testou se poderia contornar sua perda estimulando diretamente o NRF2. Alimentaram camundongos deficientes em Trim47 com uma dieta contendo tert-butil-hidroquinona (tBHQ), um composto conhecido por estabilizar o NRF2 e ativar seus genes-alvo. Esse tratamento restaurou a atividade dos genes antioxidantes nas células endoteliais cerebrais, trouxe a expressão dos genes de junção apertada de volta próximos ao normal e reduziu o vazamento da barreira hematoencefálica. De forma impressionante, também normalizou a ativação dos astrócitos e resgatou o desempenho dos animais nos testes de memória, sugerindo que reforçar essa via antioxidante pode reverter tanto problemas vasculares quanto cognitivos, pelo menos em camundongos.
Pistas a partir do sangue humano e próximos passos
Para conectar seus experimentos em camundongos à doença humana, os pesquisadores analisaram proteínas relacionadas à via NRF2 em amostras de sangue de milhares de pessoas que haviam feito exames de ressonância magnética cerebral. Níveis de várias proteínas reguladas por NRF2 foram associados a marcadores de imagem da doença de pequenos vasos, como espaços perivasculares aumentados e alterações na substância branca. Isso sustenta a ideia de que a sinalização TRIM47–NRF2 alterada é relevante em pessoas, não apenas em animais experimentais, e que essas proteínas podem servir como biomarcadores da gravidade ou progressão da doença.
O que isso significa para a saúde cerebral
Em conjunto, o trabalho retrata o TRIM47 como um guarda-costas molecular que ajuda os vasos sanguíneos cerebrais a resistir aos danos oxidativos ao estabilizar o sistema antioxidante NRF2. Quando o TRIM47 falta ou está comprometido, a barreira hematoencefálica enfraquece, lesões cerebrais sutis se acumulam e a memória começa a falhar. Reativar a via NRF2 pode remendar a barreira e restaurar a cognição em camundongos, destacando esse eixo de sinalização como um alvo terapêutico promissor para formas vasculares de demência. Embora o tBHQ em si não seja adequado como fármaco para humanos, compostos mais seguros que aumentem o NRF2 ou estratégias que imitem o papel protetor do TRIM47 podem, um dia, ajudar a preservar a saúde cerebral ao fortalecer seus menores e mais frágeis vasos.
Citação: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Palavras-chave: doença cerebral de pequenos vasos, barreira hematoencefálica, TRIM47, via NRF2, demência vascular