Clear Sky Science · pt
Um caminho entre subunidades é necessário para a ligação entropicamente dirigida e negativamente cooperativa de nucleotídeos cíclicos no canal HCN2
Como o minúsculo marca‑passos do coração percebe sinais químicos
Cada batimento cardíaco e muitos ritmos cerebrais dependem de canais microscópicos que se abrem e fecham nas membranas das nossas células. Esses canais, chamados canais pacemaker HCN, são controlados não apenas pela voltagem elétrica, mas também por pequenas moléculas mensageiras conhecidas como nucleotídeos cíclicos. Este estudo investiga uma pergunta aparentemente simples, com implicações amplas: como essas pequenas moléculas se ligam ao canal HCN2 de forma coordenada, e como falhas sutis nesse processo podem contribuir para transtornos como a epilepsia?
Um regulador molecular para os ritmos do corpo
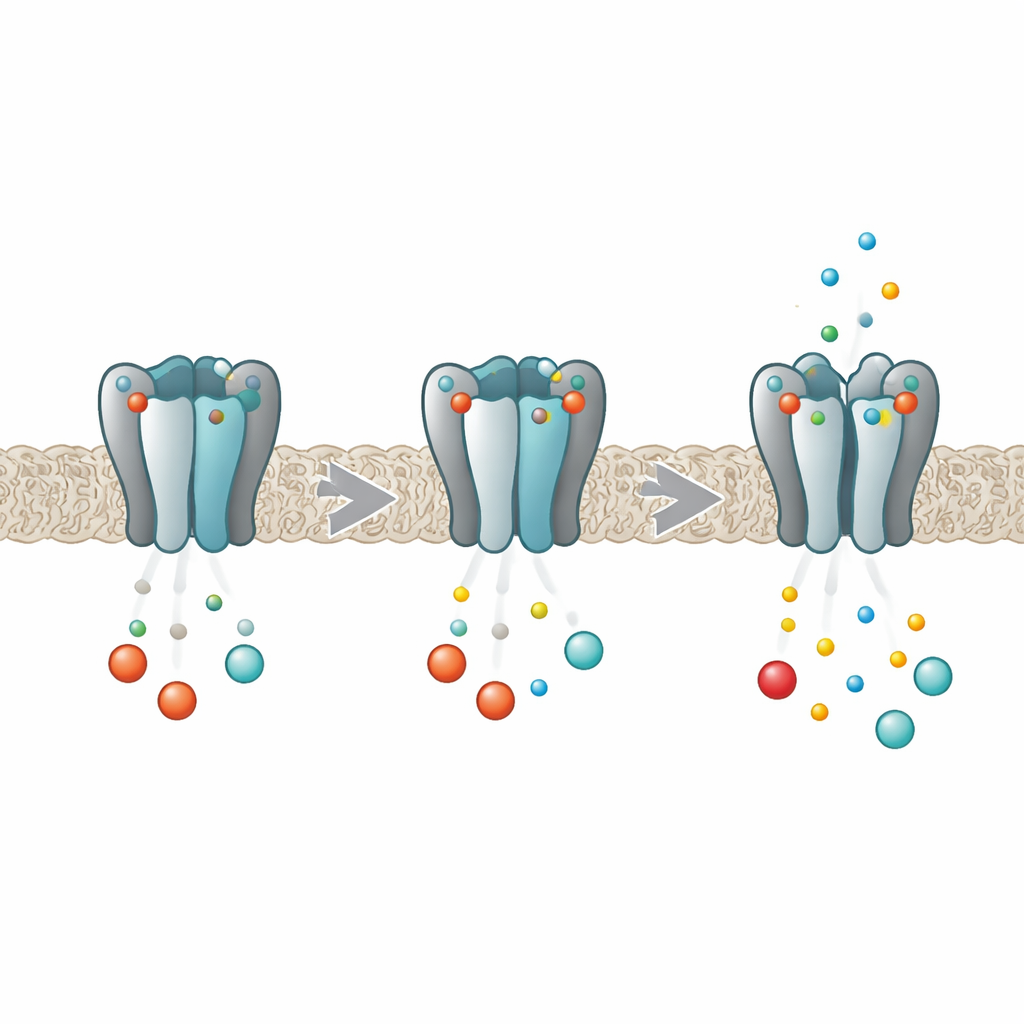
Os canais HCN funcionam como dimmers para a atividade elétrica nas células do coração e do cérebro. Cada canal é formado por quatro subunidades proteicas idênticas que, juntas, formam um poro central por onde os íons fluem. No interior de cada subunidade há uma cavidade que pode captura r nucleotídeos cíclicos como cAMP e cGMP. Quando esses mensageiros se ligam, eles facilitam a abertura do poro, aumentando a corrente do marca‑passos. Trabalhos anteriores mostraram que na variante HCN2 a ligação não ocorre de forma independente em cada cavidade; em vez disso, os quatro sítios influenciam‑se mutuamente de modo que a primeira molécula se liga com mais facilidade do que as subsequentes — um comportamento conhecido como cooperatividade negativa. O novo trabalho buscou descobrir exatamente como as quatro subunidades “conversam” entre si durante esse processo.
Subunidades que sentem suas vizinhas
Os pesquisadores combinaram simulações computacionais com medições laboratoriais em pedaços isolados da cauda do canal HCN2. Usando longas simulações de dinâmica molecular, observaram como a região terminal do canal — a parte que contém as cavidades para nucleotídeos cíclicos e o chamado C‑linker que conecta ao poro — se flexiona e oscila quando números diferentes de moléculas de cAMP ou cGMP estão ligadas. Eles descobriram que, quando um mensageiro se prende a uma subunidade, isso não estabiliza apenas essa subunidade isoladamente. Em vez disso, altera sutilmente a estabilidade das vizinhas, às vezes tornando‑as mais rígidas, às vezes mais flexíveis, mesmo que a forma global da proteína mal se altere. Essas influências vizinha‑a‑vizinha dependiam de quantos sítios estavam ocupados e de onde esses sítios se situavam ao redor do anel, correspondendo ao esperado para cooperatividade negativa.
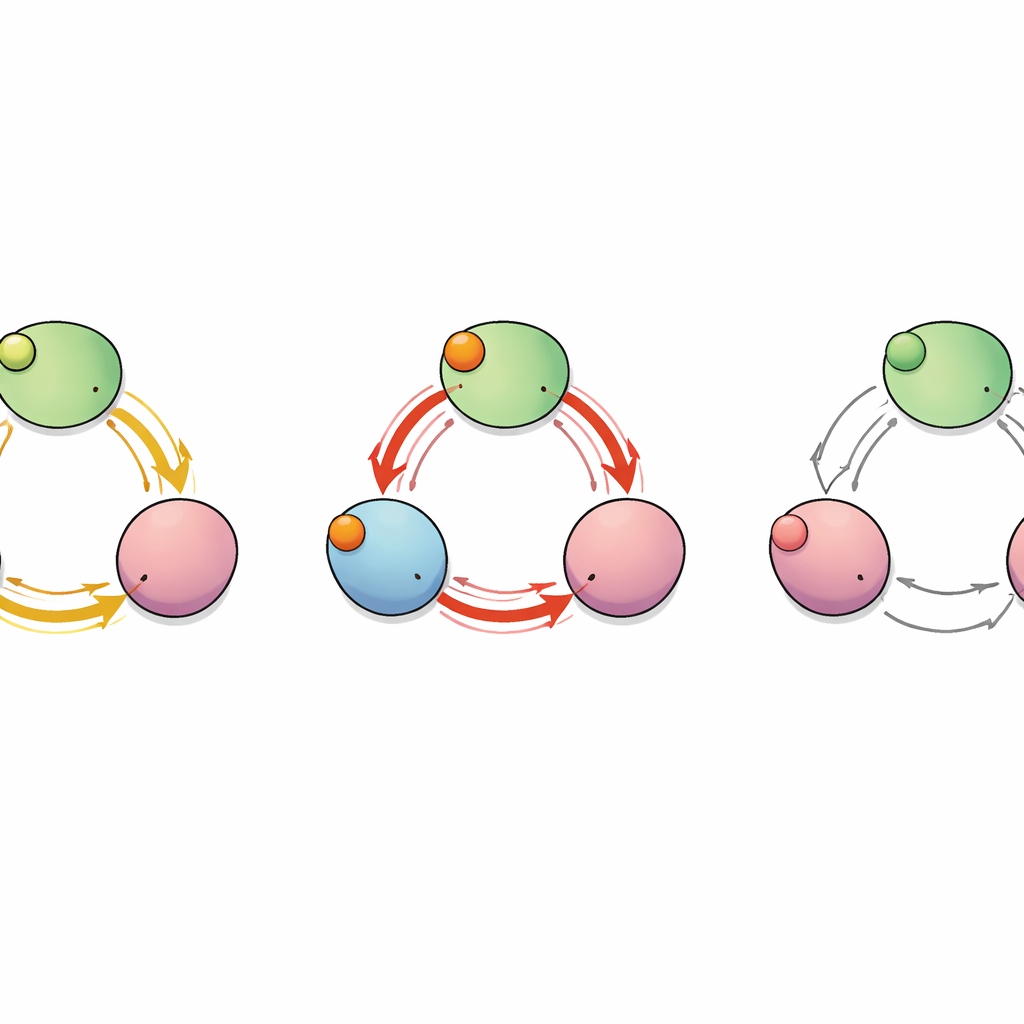
Um caminho oculto entre subunidades
Para mapear como o “sinal” da ligação viaja através da proteína, a equipe tratou o canal como uma rede de aminoácidos interagentes. Eles calcularam quais resíduos se moviam de forma correlacionada durante as simulações e usaram ferramentas da teoria dos grafos para identificar os caminhos de comunicação mais curtos e eficientes das cavidades de ligação até os segmentos do C‑linker que controlam o poro. Essa análise revelou várias rotas possíveis, mas duas se destacaram: uma que permanece dentro de uma única subunidade e outra que salta de uma subunidade para a vizinha. Ao longo dessa via intersubunitária, um único resíduo — um glutamato na posição 488 (E488) — atuou como um hub crítico por onde passaram muitos dos caminhos mais curtos, sugerindo que ele poderia ser um ponto de retransmissão chave para a ligação cooperativa.
Mutações que interrompem a conversa
Os autores então partiram para experimentos com as caudas purificadas do canal para testar a importância dessa via. Eles alteraram E488 e a tirosina 459 (Y459) nas proximidades, que se encontra na subunidade vizinha onde o caminho chega. Usando espalhamento dinâmico de luz, confirmaram que as proteínas mutantes ainda se montavam em complexos de quatro subunidades, mas deixaram de mostrar o apertamento intersubunitário fortemente induzido pelo ligante observado na proteína normal. A titulação isotérmica por calorimetria, que registra os pequenos calores de ligação, revelou uma mudança ainda maior: o HCN2 tipo selvagem exibiu dois eventos de ligação distintos, um primeiro passo de alta afinidade impulsionado principalmente por um aumento de entropia (maior movimento interno), seguido por três passos de afinidade mais baixa. Em contraste, os mutantes em E488 ou Y459 exibiram apenas um único modo de ligação de afinidade modesta, sem esse impulso entrópico favorável e sem a característica cooperatividade negativa.
Por que mudanças sutis na entropia importam
Ao juntar essas peças, o estudo desenha um retrato do canal HCN2 como um anel dinâmico de quatro subunidades conectadas por “caminhos de conversa” específicos. Quando o primeiro nucleotídeo cíclico se liga, ele ajusta os movimentos de partes distantes do anel por meio de E488 e Y459, tornando os eventos de ligação subsequentes menos favoráveis e afinando a resposta do poro. Esse efeito é conduzido não por grandes rearranjos estruturais, mas por alterações na flexibilidade interna — mudanças na entropia que são invisíveis em instantâneos estáticos, porém cruciais para a função. Mutações que rompem os resíduos-chave ao longo desse caminho intersubunitário silenciam a conversa, abolindo a cooperatividade negativa, e estão ligadas a doenças como epilepsia generalizada idiopática. Para o leitor leigo, a conclusão é que os interruptores vitais do coração e do cérebro dependem de “sussurros” moleculares finamente coreografados entre subunidades protéicas, e entender esses sussurros ajuda a explicar tanto os ritmos normais quanto o que acontece quando eles se alteram.
Citação: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Palavras-chave: canal iônico HCN2, ligação de nucleotídeos cíclicos, cooperatividade negativa, comunicação alostérica, mutação associada à epilepsia