Clear Sky Science · pt
Uma pequena molécula ativa alostericamente a secreção dependente de SecA
Transformando o porto de envio bacteriano em modo turbo
As bactérias sobrevivem exportando constantemente proteínas por pequenas portas em suas membranas. Essas exportações ajudam-nas a construir paredes celulares, secretar toxinas e adaptar-se ao estresse — processos centrais em muitas infecções. Este estudo descreve uma pequena molécula, chamada HSI#6, que faz algo incomum: em vez de bloquear essa maquinaria de exportação, ela a transforma em um modo hiperativo e menos seletivo. Entender como esse interruptor funciona pode tanto revelar novas estratégias antibacterianas quanto oferecer à biotecnologia uma forma de aumentar a secreção de proteínas sob demanda.
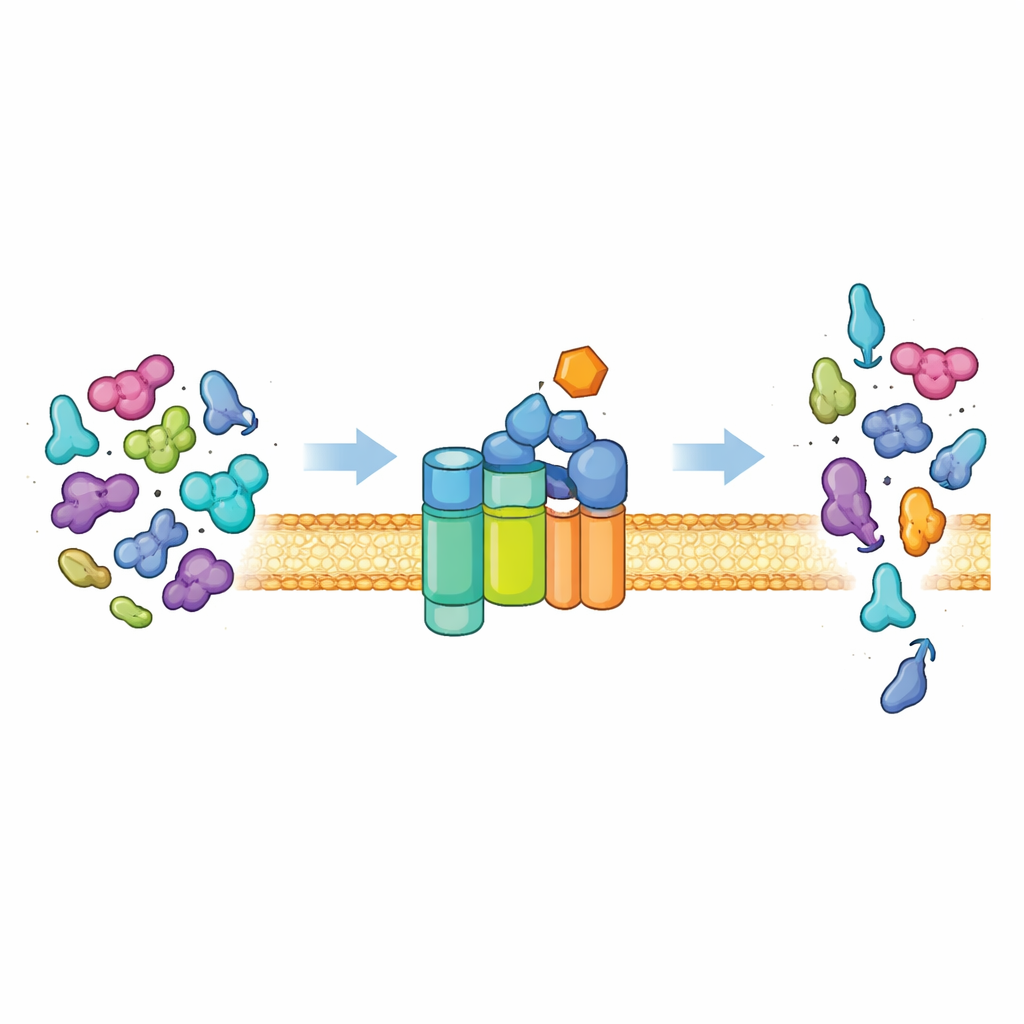
A saída de proteínas da célula
A maioria das bactérias exporta proteínas para fora da célula usando uma via universal conhecida como sistema Sec. No seu núcleo está um canal de membrana (SecYEG) e uma proteína motora (SecA) que queima combustível celular (ATP) para empurrar cadeias de proteínas desdobradas através do canal. Em condições normais, esse sistema é exigente. Ele exporta principalmente “pré-proteínas” que carregam etiquetas de endereço especiais, conhecidas como peptídeos sinal, além de características adicionais em seu corpo principal. Essas características são necessárias para transformar o SecA de um estado silencioso e de baixa atividade em um motor potente. Apenas proteínas que apresentam a combinação correta de sinais conseguem destravar a atividade total, garantindo que a célula exporte a carga certa e mantenha as proteínas citoplasmáticas comuns em segurança dentro dela.
Uma pequena molécula que desperta o motor
Os pesquisadores descobriram HSI#6 em uma triagem de compostos que interferiam com a secreção de proteínas bacterianas e o crescimento. Testes bioquímicos mostraram que HSI#6 se liga diretamente ao SecA com afinidade micromolar e altera a eficiência com que ele usa ATP. Em solução, faz com que o SecA retenha ATP com mais afinco; quando o SecA está ligado ao canal, HSI#6 tanto melhora a ligação do ATP quanto acelera o turnover do ATP. Esse padrão é a marca de um ativador alostérico: uma molécula que se liga a um sítio numa proteína, mas altera a atividade em outro sítio distante. Ao contrário dos clientes proteicos naturais, HSI#6 não precisa atuar como carga para estimular o motor — ele simplesmente ajusta a dinâmica interna do SecA de modo que toda a translocase fique cataliticamente preparada.
De filtro seletivo a nanomáquina promíscua
Uma vez que HSI#6 está ligado, o sistema Sec deixa de insistir nas etiquetas de exportação usuais. Em experimentos in vitro, o composto aproximadamente dobrou a secreção de uma pré-proteína padrão e tornou o complexo mais resistente ao azida de sódio, um inibidor conhecido do SecA. Mais impressionante, HSI#6 permitiu que a maquinaria normal, de tipo selvagem, transportasse proteínas que não possuem peptídeos sinal, bem como proteínas que normalmente residem no citoplasma. Em células bacterianas vivas, o mesmo efeito foi observado usando repórteres baseados em fosfatase alcalina: quando proteínas citoplasmáticas foram fundidas a uma enzima secretada, a presença de HSI#6 causou um aumento acentuado na atividade secretada sem alterar a quantidade de proteína produzida. Em outras palavras, HSI#6 efetivamente desacopla a exportação das verificações usuais de identidade do cliente, transformando o sistema Sec em uma bomba de exportação de amplo espectro para qualquer proteína suficientemente desdobrada.
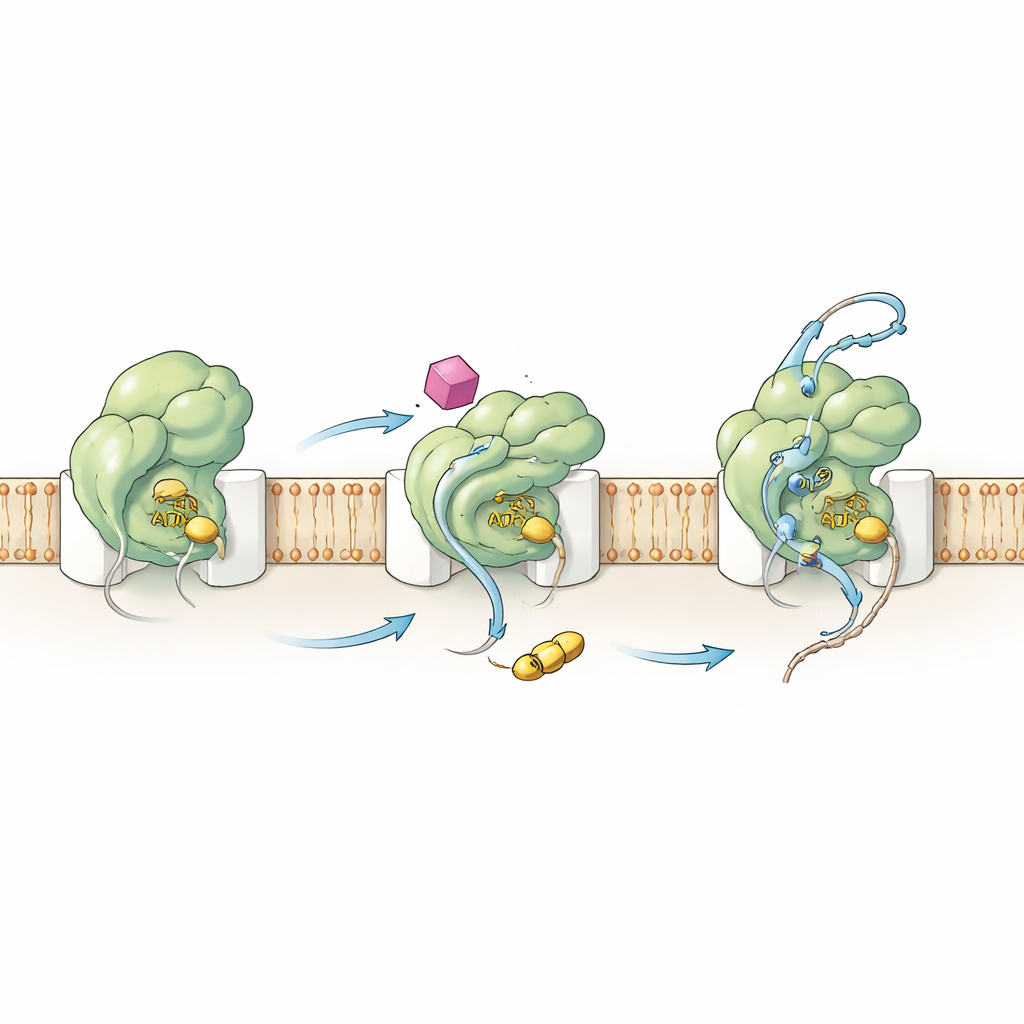
Reconfigurando o motor de dentro
Para entender como HSI#6 desencadeia esse comportamento, a equipe examinou tanto a química quanto os movimentos do SecA. Medições cinéticas mostraram que o composto desloca a etapa chave de ativação para upstream: o complexo SecA–canal torna-se cataliticamente ativo mesmo antes de um cliente proteico se ligar. HSI#6 também ajuda o SecA a liberar o combustível gasto (ADP), uma etapa normalmente lenta e limitante, apoiando assim um ciclo de ATP mais rápido. Usando espectrometria de massa com troca hidrogênio–deutério, os autores mapearam como HSI#6 remodela a flexibilidade de diferentes regiões do SecA. O composto afrouxa seletivamente partes da proteína que detectam clientes e se conectam ao canal, enquanto torna mais rígida uma região de suporte que provavelmente abriga seu sítio de ligação. O padrão de movimentos resultante assemelha-se a um estado já engajado, “ligado”, da translocase, sugerindo que HSI#6 estabiliza uma forma ativada — possivelmente até favorecendo um SecA monomérico ligado ao canal — sem qualquer cliente presente.
Por que isso importa para a medicina e a biotecnologia
Ao demonstrar que uma pequena molécula pode ativar alostericamente o SecA e eliminar sua seletividade de cliente habitual, este trabalho revela uma nova maneira de controlar uma máquina bacteriana central. Para doenças infecciosas, essa secreção forçada e descontrolada poderia enfraquecer patógenos ao drenar energia e perturbar seus programas de exportação finamente ajustados, tornando ativadores do tipo HSI#6 pontos de partida atraentes para o desenho de antibióticos — ou como guias para a criação de futuros inibidores que bloqueiem as mesmas características regulatórias. Para a biotecnologia, o mesmo princípio poderia ser reaproveitado para aumentar a secreção de proteínas recombinantes úteis, sem a necessidade de peptídeos sinal projetados ou ajustes genéticos complexos. Em essência, o estudo demonstra que o “porto de envio” proteico bacteriano pode ser reprogramado quimicamente, abrindo novas vias tanto para combater micróbios quanto para aproveitá-los como fábricas microscópicas.
Citação: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Palavras-chave: secreção de proteínas bacterianas, translocase SecA, ativação alostérica, reguladores de pequena molécula, descoberta de antibacterianos