Clear Sky Science · pt
LncRNA P4HA2-AS1 promove fibrose intersticial renal via ubiquitinação K63 mediada por TRIM32 de ULK1 e desregulação da autofagia
Por que a cicatrização renal importa
A doença renal crônica afeta centenas de milhões de pessoas no mundo e frequentemente avança silenciosamente até que a diálise ou um transplante sejam a única forma de sobrevivência. No centro desse declínio está um processo chamado cicatrização, em que o tecido renal normal é gradualmente substituído por material rígido e não funcional. Este estudo faz uma pergunta simples, mas crucial: quais interruptores moleculares dentro das células renais as empurram para essa cicatrização prejudicial, e é possível reverter esses interruptores?
Um interruptor de RNA oculto nas células renais
Os rins filtram o sangue usando redes elaboradas de pequenos túbulos. Quando esses túbulos são lesionados por obstrução do fluxo urinário, glicemia alta ou perda súbita do suprimento sanguíneo, eles podem responder depositando tecido cicatricial entre as células. Os pesquisadores examinaram os rins de camundongos com vários tipos de lesão e os compararam a rins saudáveis usando sequenciamento de RNA, uma técnica que lê quais genes estão ativados. Eles descobriram que uma molécula pouco conhecida chamada P4HA2-AS1, um RNA longo não codificante que não produz proteína, estava consistentemente elevada em rins danificados e formadores de cicatriz e em células renais humanas estressadas em laboratório. Esse RNA foi encontrado principalmente na região citoplasmática das células, sugerindo que pode regular outras proteínas ali. 
Reduzindo o RNA para proteger o rim
Para testar se P4HA2-AS1 é apenas um espectador ou um motor ativo do dano, a equipe diminuiu seus níveis em camundongos e em células renais humanas cultivadas. Em um modelo murino bem estabelecido, no qual um ureter é ligado para causar obstrução de longo prazo, reduzir esse RNA por entrega viral direcionada aliviou muitos sinais de fibrose: os túbulos permaneceram mais intactos, houve menos colágeno e outras proteínas de cicatriz entre as células, e marcadores de função renal no sangue melhoraram. Em culturas de células renais humanas, a redução de P4HA2-AS1 também atenuou a resposta a um potente sinal pró-fibrótico, TGF-β, levando a menor produção de fibronectina, colágeno e outros fatores pró-fibróticos. Esses experimentos mostraram que esse RNA não é meramente um marcador de dano, mas alimenta ativamente o processo de cicatrização.
Autofagia: da manutenção ao dano
Os pesquisadores então investigaram como esse RNA causa dano. Seus dados de expressão gênica e de imagem apontaram para a autofagia, o sistema interno de reciclagem da célula que degrada proteínas e organelas desgastadas. Em condições normais, a autofagia é um processo de manutenção saudável, mas quando é ativada demais e por muito tempo pode levar rins lesionados a um reparo maladaptativo e à fibrose. Em células renais sob estresse, P4HA2-AS1 aumentou o fluxo de material pela via autofágica, levando ao acúmulo de vesículas de reciclagem. Quando o RNA foi bloqueado, essa atividade excessiva retornou a níveis mais próximos do normal, tanto em células quanto em rins de camundongos obstruídos. Camundongos sem ULK1, uma enzima iniciadora central da autofagia, também foram protegidos da fibrose, e nesses animais a superexpressão de P4HA2-AS1 não pôde mais agravar o dano, ligando de forma firme os efeitos do RNA a essa via.
Uma cadeia molecular em três elos
Aprofundando-se, a equipe usou técnicas bioquímicas de "pesca" para identificar proteínas que se ligam fisicamente a P4HA2-AS1. Uma delas se destacou: TRIM32, uma enzima que marca outras proteínas com pequenas "bandeiras" moleculares chamadas ubiquitinas. O RNA se liga a TRIM32 e o protege da degradação, elevando seus níveis dentro das células renais. O TRIM32 estabilizado, por sua vez, anexa um tipo específico de cadeia de ubiquitina a ULK1. Em vez de direcionar ULK1 para destruição, essa cadeia age como um potenciador, aumentando a capacidade de ULK1 de iniciar a autofagia. Quando os cientistas removeram TRIM32 em camundongos ou o silenciaram em células renais, tanto a fibrose quanto a autofagia excessiva foram reduzidas. Reintroduzir TRIM32 em células onde P4HA2-AS1 havia sido bloqueado restaurou parcialmente a resposta fibrótica, mostrando que essa enzima é um elo intermediário chave na cadeia. 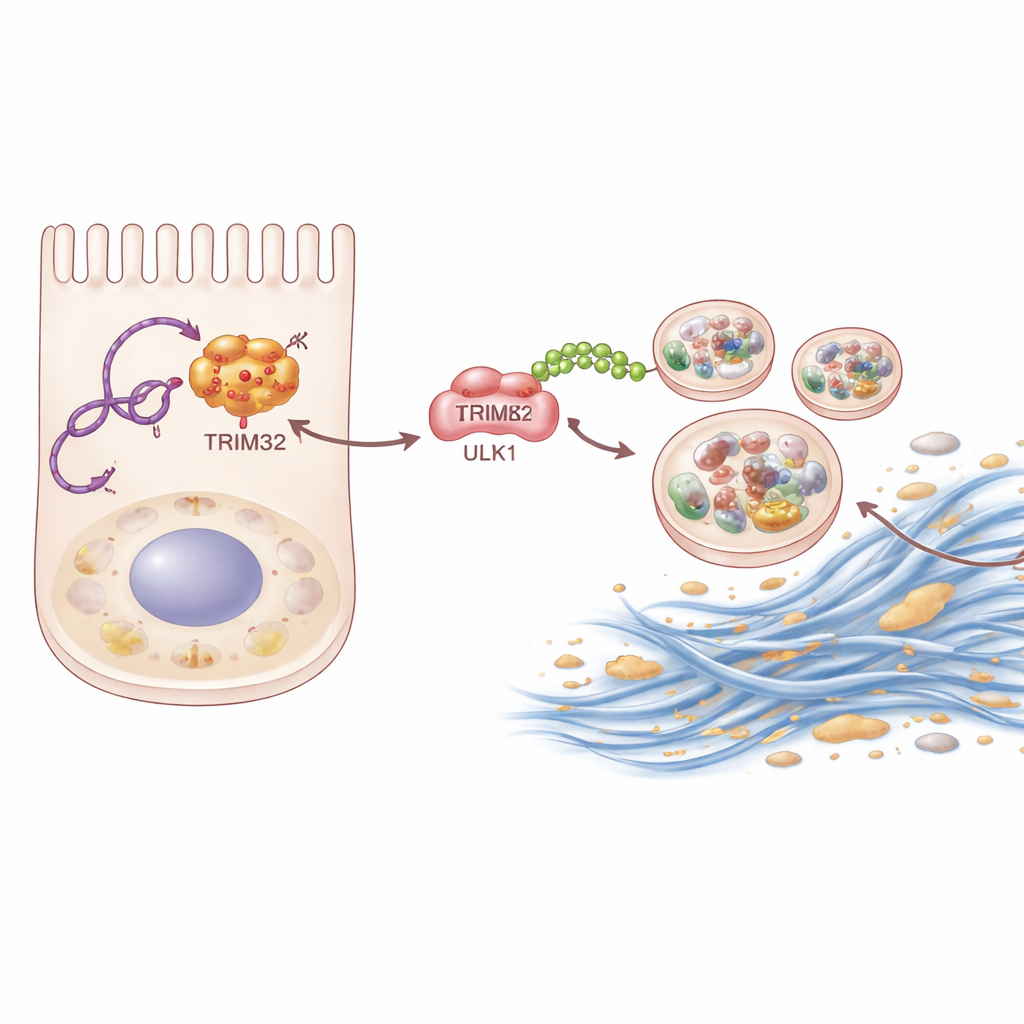
Novos caminhos para rins mais saudáveis
Tomado em conjunto, o trabalho revela uma via molecular até então desconhecida que conecta RNA longo não codificante, marcação proteica e reciclagem celular ao acúmulo de tecido cicatricial renal. Em rins lesionados, P4HA2-AS1 aumenta, estabiliza TRIM32, superativa ULK1 e impulsiona a autofagia além de sua faixa benéfica, encorajando, em última instância, o acúmulo de proteínas fibróticas e a perda de função. Para o público não especializado, a mensagem principal é que a cicatrização renal não é uma caixa-preta inevitável: ela é movida por interruptores identificáveis que podem ser alvo de fármacos. Alvejar o eixo P4HA2-AS1–TRIM32–ULK1 — reduzindo o RNA disfuncional, modulando TRIM32 ou ajustando a atividade de ULK1 — pode um dia oferecer novos tratamentos para retardar ou prevenir a progressão da doença renal crônica.
Citação: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Palavras-chave: doença renal crônica, fibrose renal, autofagia, RNA longo não codificante, túbulos renais