Clear Sky Science · pt
Obesidade prejudica a espermatogênese por meio de ferroptose de células de Leydig induzida pelo miR-122-5p exossomal de origem hepática
Por que peso e fertilidade estão ligados
A obesidade costuma ser discutida em termos de doenças cardíacas e diabetes, mas também pode minar silenciosamente a fertilidade masculina. Este estudo em camundongos revela um modo surpreendente pelo qual uma dieta rica em gordura pode reduzir a testosterona e prejudicar a produção de espermatozoides: o fígado envia pequenas “bolhas mensageiras” pela corrente sanguínea que desencadeiam um tipo especial de morte celular nas células produtoras de hormônio dos testículos. Compreender essa comunicação oculta do fígado ao testículo pode ajudar a explicar por que homens com sobrepeso frequentemente enfrentam baixo nível de testosterona e infertilidade, além de apontar novos alvos terapêuticos.
Mensagens escondidas entre órgãos
Nossos órgãos conversam constantemente entre si por hormônios e outros mensageiros químicos. Uma forma dessa comunicação usa exossomos — bolhas de nanômetros liberadas pelas células que transportam lipídios, proteínas e material genético. Os pesquisadores partiram de camundongos alimentados com dieta normal ou com dieta rica em gordura que induziu obesidade, resistência à insulina e controle glicêmico prejudicado. Os camundongos obesos apresentaram testículos menores e menos ativos: contagem de espermatozoides, níveis de testosterona e o tamanho e número de túbulos produtores de espermatozoides foram todos reduzidos. Ao examinar marcadores celulares chave nos testículos, encontraram menos células de Leydig produtoras de testosterona e menos células espermatogênicas em estágios iniciais e tardios, confirmando que toda a linha de produção de espermatozoides estava comprometida. 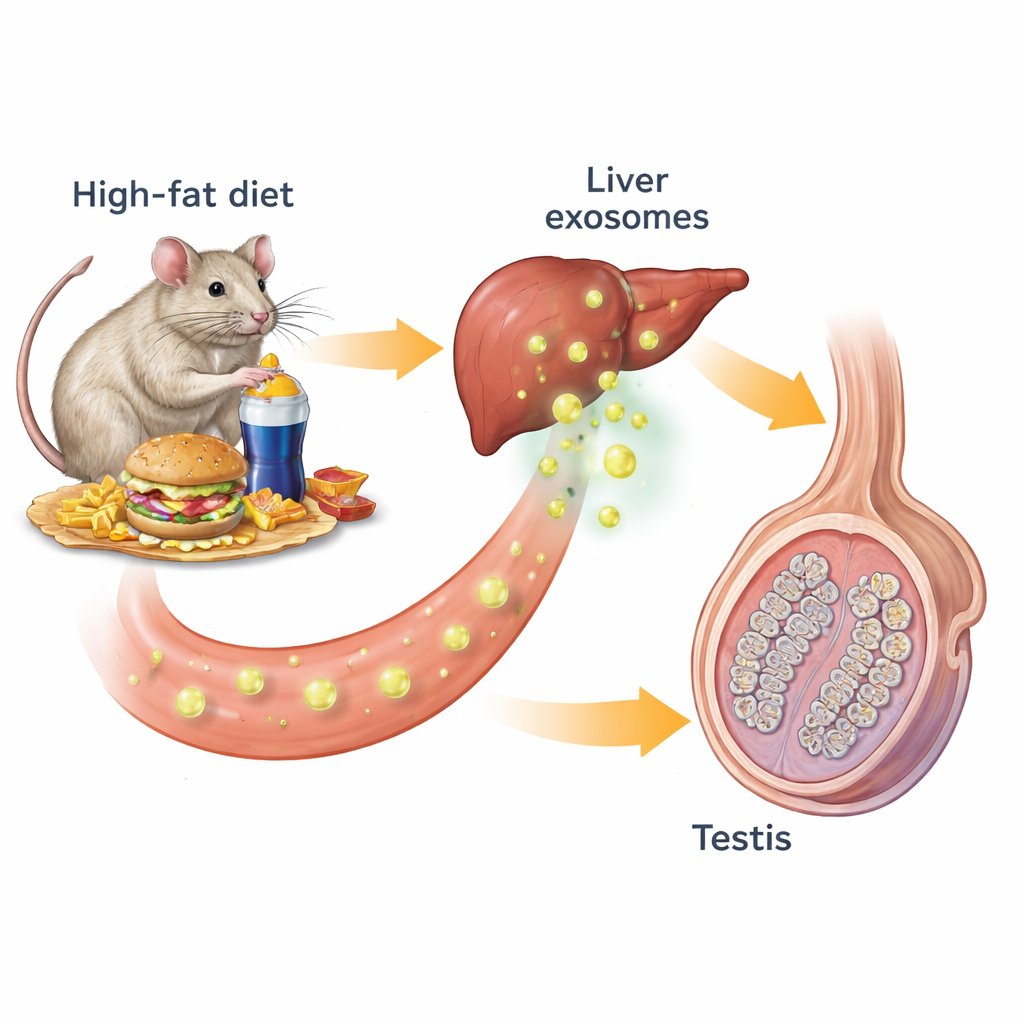
Exossomos espalham o dano
Para testar se exossomos circulantes ajudam a promover esse dano, os cientistas purificaram exossomos do sangue de camundongos obesos e magros. Injetar exossomos de camundongos obesos em animais saudáveis e magros foi suficiente para reproduzir muitos dos problemas: os receptores desenvolveram sinais de disfunção metabólica, seus níveis de testosterona caíram e a contagem de espermatozoides e a estrutura testicular se deterioraram. Bloquear a liberação de exossomos em camundongos obesos com um fármaco chamado GW4869 reverteu em grande parte essas alterações, restaurando contagens de espermatozoides, testosterona e arquitetura testicular normal. Esses resultados mostram que exossomos na corrente sanguínea não são meros espectadores; eles carregam ativamente sinais nocivos da obesidade para o sistema reprodutor.
Uma forma tóxica de morte celular
A equipe então investigou exatamente o que os exossomos estavam fazendo às células de Leydig. Eles se concentraram na ferroptose, uma forma de morte celular impulsionada por ferro, marcada pelo acúmulo de ferro, dano oxidativo aos lipídios e lesão mitocondrial — as usinas de energia da célula. Em camundongos obesos e em camundongos saudáveis tratados com exossomos de origem obesa, os testículos apresentaram níveis mais altos de ferro e malondialdeído, um subproduto do dano lipídico, além de dano mitocondrial evidente ao microscópio eletrônico. Tratar camundongos obesos com um composto bloqueador de ferroptose, o Ferrostatina‑1, preservou as células de Leydig, aumentou testosterona e contagens de espermatozoides e melhorou a saúde mitocondrial. Em cultura celular, a mesma droga protegeu células de Leydig isoladas da morte e do estresse oxidativo induzidos por exossomos de animais obesos. Em conjunto, esses experimentos revelam a ferroptose como elo chave entre obesidade e falha na produção de testosterona.
A mensagem do fígado e o interruptor SCD2
Para localizar a mensagem dentro dos exossomos, os pesquisadores sequenciaram seu conteúdo de pequenos RNAs e descobriram que um microRNA particular, miR‑122‑5p, estava fortemente aumentado nos exossomos de camundongos obesos. Esse microRNA era especialmente abundante no fígado e em exossomos de origem hepática, e esses exossomos hepáticos puderam ser rastreados viajando até os testículos. Quando os níveis de miR‑122‑5p foram experimentalmente reduzidos nos exossomos, as células de Leydig ficaram menos propensas à ferroptose e a produção de testosterona melhorou, embora os animais permanecessem metabolicamente enfermos. Testes adicionais mostraram que miR‑122‑5p reprime diretamente um gene chamado Scd2, que ajuda a converter certos lipídios em formas que protegem as células do dano oxidativo. Reduzir Scd2 em células de Leydig as tornou mais vulneráveis à ferroptose e diminuiu a testosterona, enquanto aumentar Scd2 em camundongos obesos restaurou parcialmente níveis hormonais, produção de espermatozoides e estrutura mitocondrial. 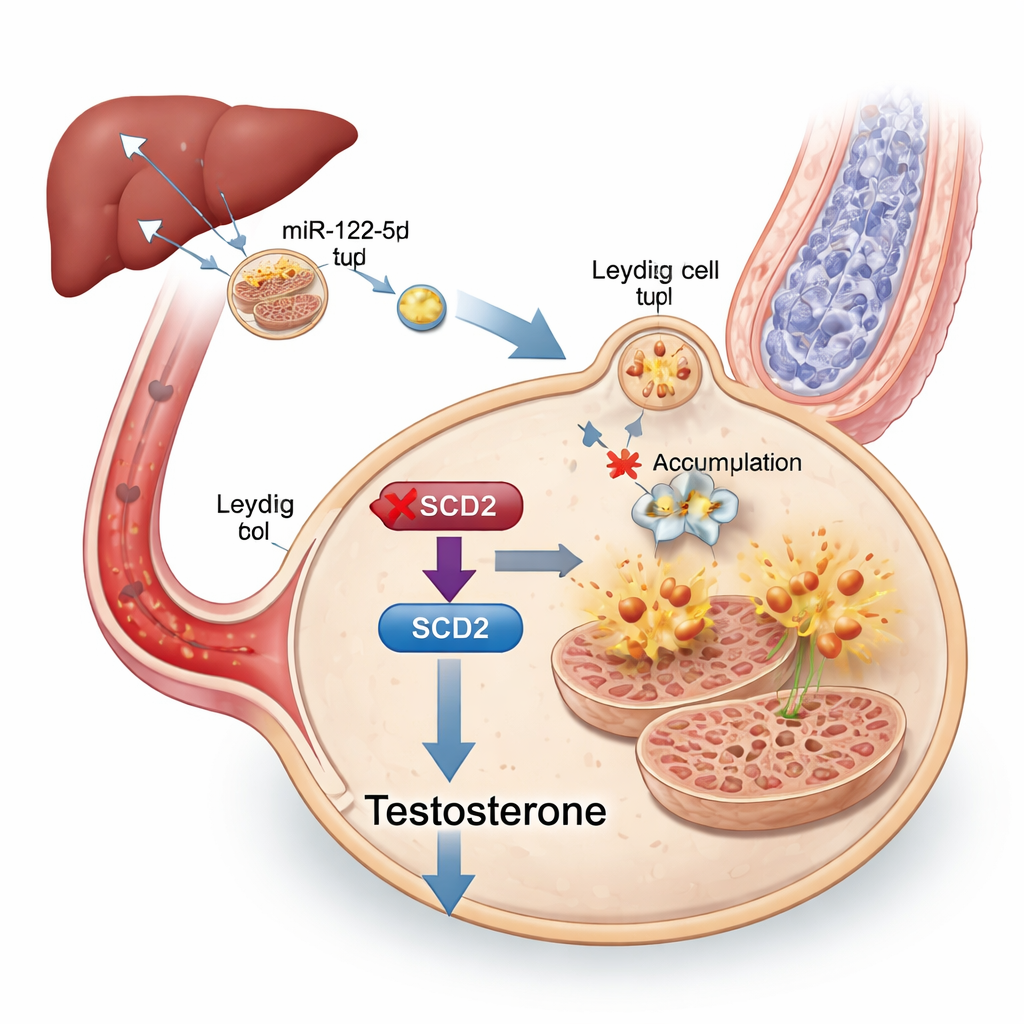
O que isso significa para a saúde humana
Em termos simples, este trabalho mostra que uma dieta rica em gordura pode fazer com que o fígado carregue exossomos com uma abundância excessiva de miR‑122‑5p. Esses exossomos viajam pelo sangue até os testículos, onde o microRNA desliga a chave Scd2 de “manuseio de gordura” nas células de Leydig. Sem Scd2, essas células acumulam dano oxidativo impulsionado por ferro, passam por ferroptose, produzem menos testosterona e, em última instância, sustentam menos espermatozoides saudáveis. Embora essa pesquisa tenha sido realizada em camundongos e ainda precise ser confirmada em humanos, ela identifica exossomos de origem hepática, miR‑122‑5p, ferroptose e Scd2 como biomarcadores promissores e potenciais alvos medicamentosos para tratar a infertilidade masculina relacionada à obesidade — e ressalta mais um motivo pelo qual dietas ricas em gordura a longo prazo podem corroer silenciosamente a saúde reprodutiva.
Citação: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Palavras-chave: obesidade e fertilidade masculina, testosterona, exossomos, células de Leydig, ferroptose