Clear Sky Science · pt
Reconhecimento e ligação de glicolipídeos pela Siglec-6 dependem de interações com a membrana celular
Como Nossas Células Diferenciam Amigo de Invasor
O sistema imunológico varre constantemente nossas próprias células, decidindo quando manter a calma e quando atacar. Uma parte chave dessa vigilância envolve o reconhecimento de estruturas açucaradas na superfície celular. Este estudo revela que um receptor imune humano, chamado Siglec-6, usa não apenas esses açúcares, mas também a própria membrana celular ao redor para tomar decisões especialmente precisas sobre o que ligar. Essa estratégia incomum pode ajudar a explicar como nossos corpos ajustam finamente os sinais imunes e pode abrir novas vias para terapias direcionadas.
Um Guardião Sensível a Açúcares nas Células Imunes
As Siglecs são uma família de receptores presentes em células imunes que reconhecem açúcares contendo ácido siálico, ajudando o sistema imunológico a distinguir “self” de “non-self”. A maioria das Siglecs depende de um único bloco construtivo altamente conservado — um resíduo de arginina — para se ligar a esses açúcares. Se essa arginina for removida, a ligação geralmente falha. A Siglec-6, no entanto, é uma exceção: trabalhos anteriores mostraram que ela ainda pode se ligar a alguns lipídios portadores de açúcar mesmo quando essa arginina chave é mutada. O novo estudo procurou descobrir como a Siglec-6 consegue violar essa regra aparente e o que isso significa para seu papel em mastócitos, células B de memória e células placentárias humanas.
Os Lipídios Especiais que a Siglec-6 Procura
Na superfície das células, os açúcares relevantes podem ser exibidos tanto em proteínas quanto em lipídios. Este trabalho foca em um grupo de lipídios portadores de açúcar chamados gangliosídeos, especialmente três estreitamente relacionados denominados GM1, GM2 e GM3. Todos os três projetam uma única “cabeça” terminada em ácido siálico para fora da membrana. Experimentos anteriores mostraram que a Siglec-6 se liga fortemente ao GM1 quando ele faz parte de uma membrana, mas quase nada ao GM2 ou GM3, embora suas cabeças açucaradas sejam muito semelhantes. Usando simulações computacionais detalhadas de membranas realistas, os autores confirmaram que o ácido siálico no GM1 e no GM3 está igualmente exposto e acessível. Em outras palavras, o simples acesso físico não é o que confere ao GM1 seu status especial. Em vez disso, um açúcar adicional na ponta do GM1 — a galactose terminal — emergiu como uma peça crítica que ajuda a posicionar corretamente a Siglec-6 contra a membrana.
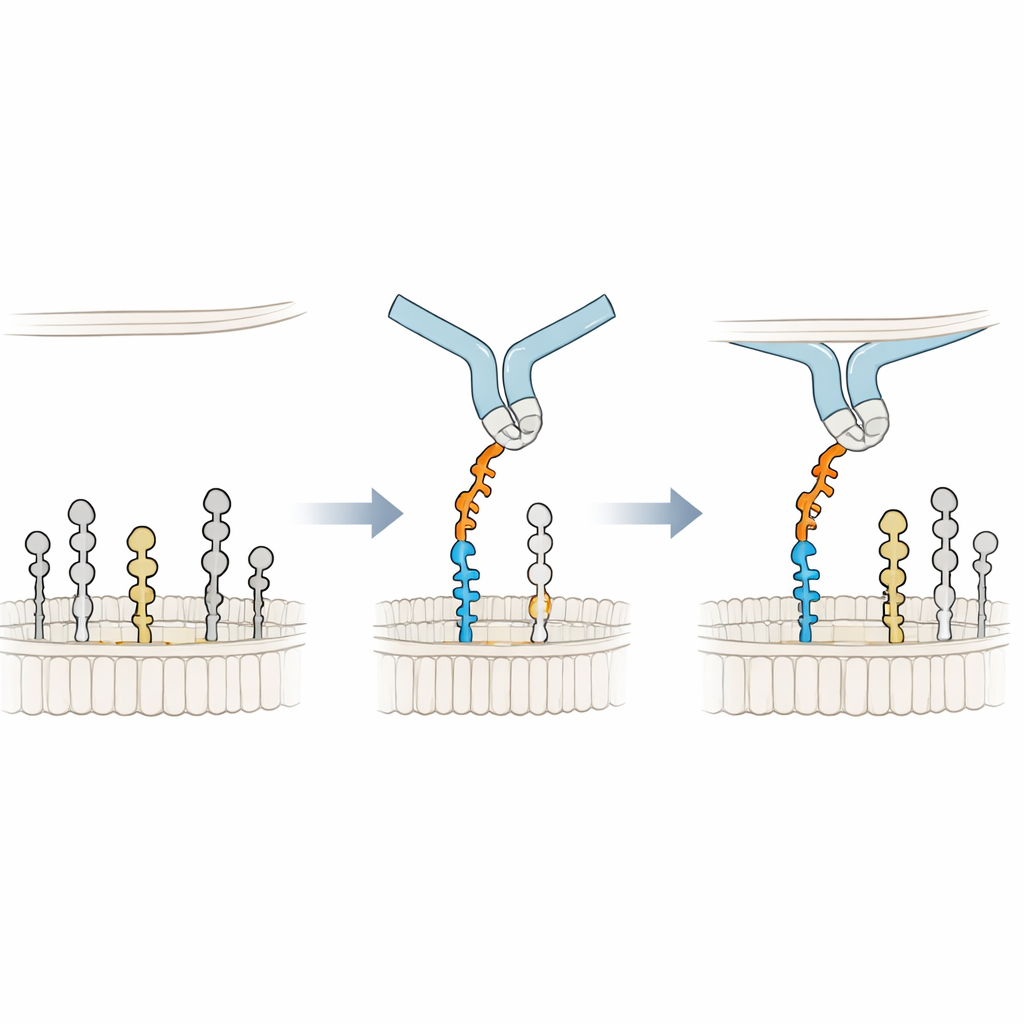
Apóia-se na Membrana para um Aperto Melhor
Para entender o mecanismo de ligação em detalhe atômico, os pesquisadores construíram modelos 3D da Siglec-6 interagindo com o GM1 em uma membrana e executaram longas simulações de dinâmica molecular. Eles descobriram que a Siglec-6 ainda usa sua arginina canônica (Arg122) para contatar o ácido siálico, mas esse contato pisca ao longo do tempo. O que mantém o complexo estável é algo novo: um triptofano próximo (Trp127) se insere na parte gordurosa da membrana, enquanto uma lisina adjacente (Lys126) interage com os grupos cabeças carregados dos lipídios circundantes. Essa “cunha” na membrana suplementa a interação habitual açúcar–arginina, efetivamente tomando emprestada energia de ligação do ambiente lipídico. Quando a galactose terminal do GM1 é removida para mimetizar o GM2, um loop flexível na Siglec-6 se move para o espaço vago, puxa o receptor para longe da membrana e interrompe esse aperto assistido pela membrana, explicando a perda de ligação estável.
Experimentos que Testaram o Mecanismo
A equipe então testou essas percepções computacionais em ensaios celulares vivos e bioquímicos. Eles modificaram geneticamente células para expressarem Siglec-6 normal ou mutante e mediram o quanto essas células se ligavam a lipossomos fluorescentes e pequenos discos lipídicos carregando GM1. Mutar a arginina canônica reduziu apenas modestamente a ligação quando o GM1 estava em uma membrana, confirmando que a Siglec-6 não depende apenas desse resíduo nesse contexto. Em contraste, mutar Trp127 praticamente aboliu a ligação a lipossomos contendo GM1, e mutar tanto Trp127 quanto Lys126 praticamente eliminou a ligação por completo. Os mesmos mutantes, entretanto, ligaram-se normalmente a açúcares semelhantes ao GM1 apresentados fora de uma membrana, mostrando que a estrutura básica da Siglec-6 estava intacta. Experimentos de espectrometria de massa nativa revelaram ainda que a Siglec-6 pode ligar-se não apenas ao GM1, mas também a fosfolipídios ordinários, e que essa interação lipídica desaparece quando Trp127 é removido. Notavelmente, a Siglec-6 até se liga a lipossomos “nus” sem GM1, novamente de modo dependente de Trp127, sugerindo que ela pode primeiro sondar a membrana e então travar quando encontra GM1.
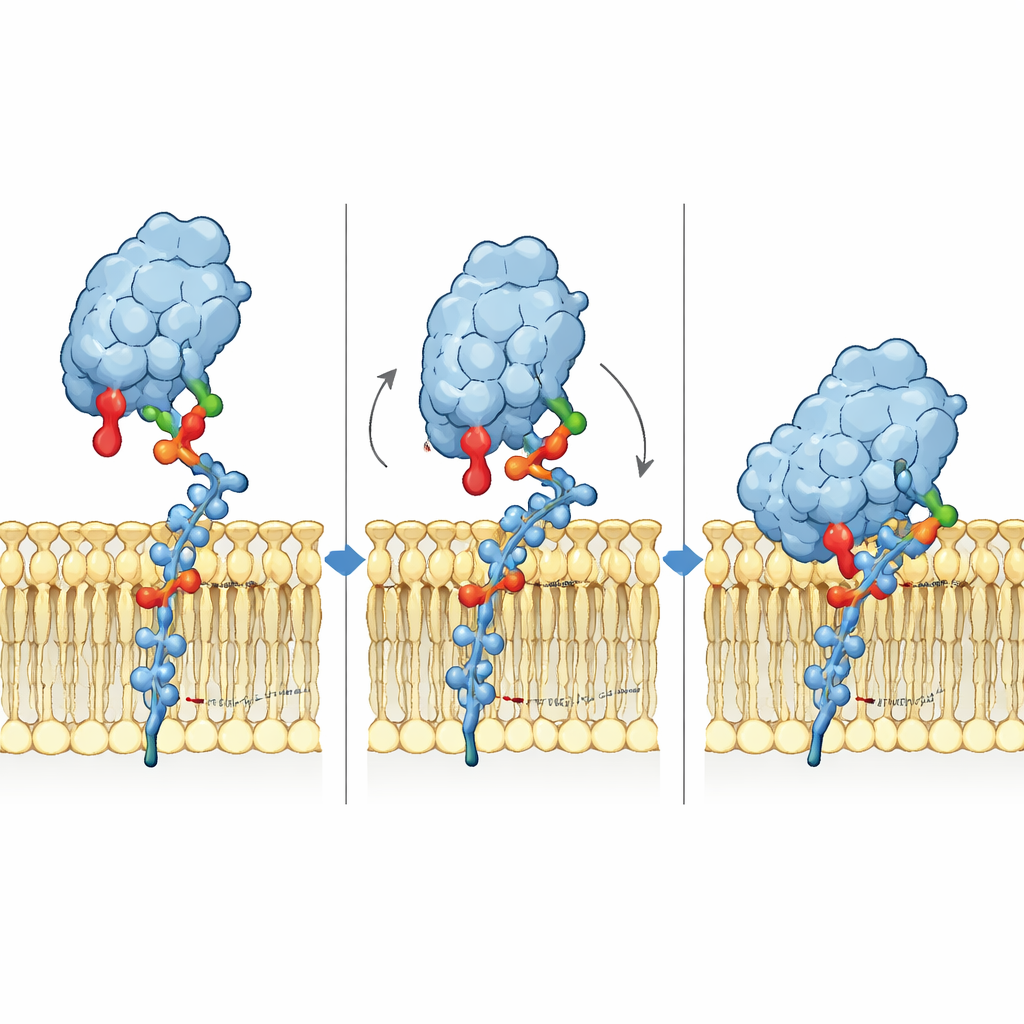
Açúcares Livres Contam Outra História
Quando os mesmos três gangliosídeos foram testados como fragmentos de açúcar livres em vez de parte de uma membrana, a Siglec-6 comportou-se mais como suas parentes. Em solução, ela se ligou ao GM1, GM2 e GM3 com afinidade igualmente fraca, e agora a arginina canônica foi essencial: mutar Arg122 reduziu drasticamente a ligação, enquanto mutar Trp127 teve pouco efeito. Esse contraste mostra que a Siglec-6 efetivamente alterna de mecanismo dependendo de ela encontrar açúcares em uma membrana ou em forma livre. Em membranas, ela depende de uma parceria cooperativa entre a cabeça açucarada, a galactose terminal do GM1 e o contato direto com a membrana; em solução, ela retorna ao clássico motivo de reconhecimento centrado na arginina.
Por Que Isso Importa para o Controle Imune
Tomado em conjunto, o estudo revela a Siglec-6 como um sensor afinado que usa o contexto físico da membrana para aguçar sua especificidade. Ao se ancorar parcialmente nos lipídios circundantes, ela pode reconhecer seletivamente o GM1 entre gangliosídeos muito semelhantes, transformando efetivamente um “leitor de ácido siálico” geral em um detector de alta precisão de um padrão superficial particular. Essa estratégia assistida pela membrana parece única entre as Siglecs estudadas até agora e pode ajudar a Siglec-6 a vasculhar superfícies celulares em busca de assinaturas glicolipídicas específicas que regulam respostas imunes ou marcam tecidos particulares, como a placenta humana. Compreender esse modo duplo de reconhecimento pode auxiliar no desenho de terapias e ferramentas diagnósticas que explorem a incomum combinação de detecção de açúcar e membrana pela Siglec-6.
Citação: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Palavras-chave: Siglec-6, gangliosídeos, membrana celular, reconhecimento de glicolipídeos, regulação imunológica