Clear Sky Science · pt
Análise integrada de GWAS e molQTLs revela variantes genéticas específicas de células no sistema imune suíno
Por que a imunidade dos porcos importa para todos nós
Porcos ajudam a alimentar grande parte do mundo e também servem como modelos importantes para estudos médicos em humanos. Ainda assim, doenças infecciosas em suínos custam bilhões de dólares aos produtores a cada ano e incentivam o uso intensivo de antibióticos. Este estudo faz uma pergunta simples, porém poderosa: como pequenas diferenças no DNA moldam o funcionamento das células imunes dos porcos, e é possível rastrear esses efeitos até o comportamento de tipos celulares individuais no sangue? Entender essa cadeia de causa e efeito pode orientar programas de melhoramento para rebanhos mais saudáveis e oferecer pistas sobre o funcionamento do nosso próprio sistema imune.
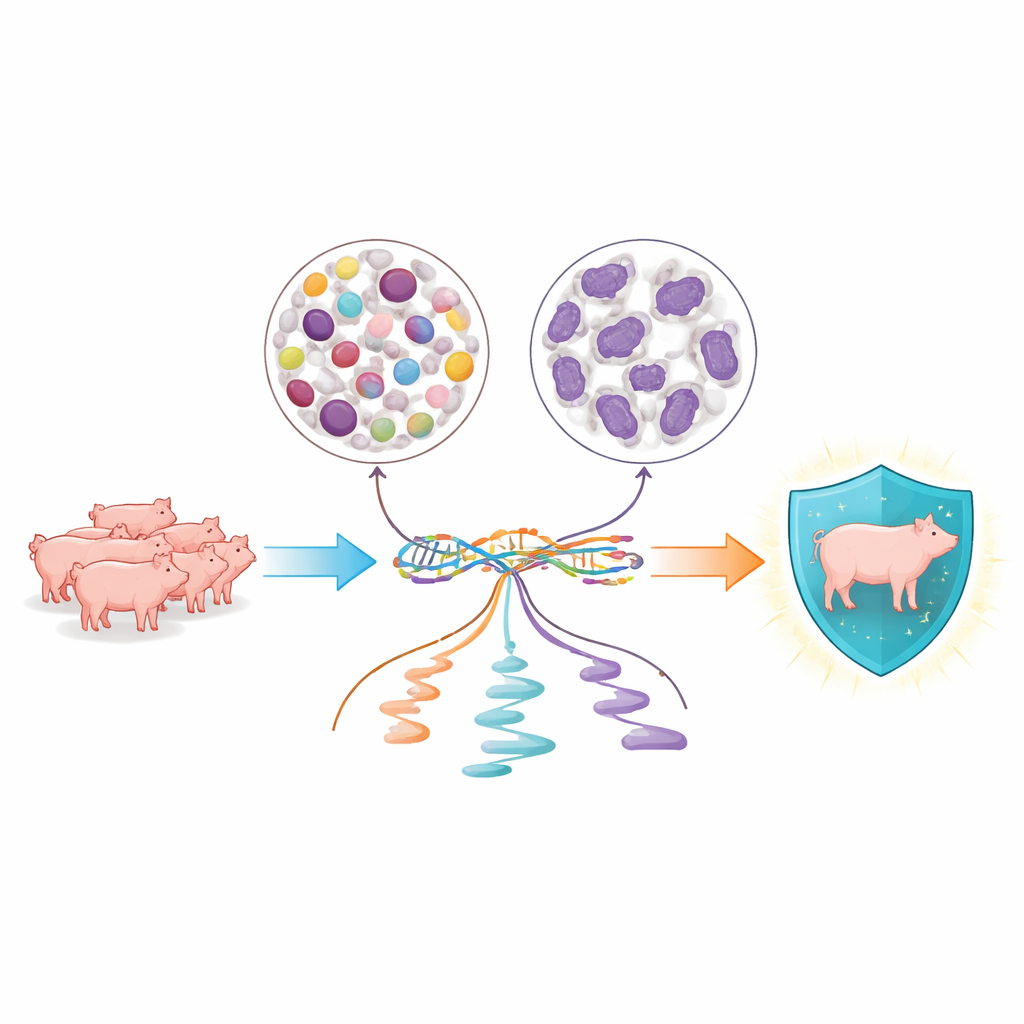
Observando de perto duas famílias celulares sanguíneas-chave
Os pesquisadores concentraram-se em dois grandes grupos de glóbulos brancos que patrulham constantemente o sangue suíno: células mononucleares do sangue periférico, que incluem linfócitos e monócitos envolvidos em defesas mais lentas e específicas, e neutrófilos, que promovem ataques rápidos e de primeira linha contra microrganismos. A partir de 134 leitões Yorkshire, eles purificaram cada tipo celular separadamente e obtiveram dados de genoma completo além de instantâneos detalhados do RNA, as moléculas que transportam instruções genéticas dentro das células. Isso permitiu ver não apenas quais genes estavam ativados, mas também como a célula recortava e finalizava essas mensagens antes de usá-las.
Conectando variantes de DNA a interruptores moleculares
Em vez de olhar apenas para quais variantes de DNA se associam ao risco de doença, a equipe mapeou como variantes influenciam três tipos de características moleculares em cada tipo celular. Algumas variantes alteraram quanto RNA um gene produzia. Outras mudaram como o RNA era emendado, aparando ou reordenando trechos. Uma terceira classe deslocou como o RNA era finalizado em sua extremidade, um processo chamado poliadenilação que pode afetar a estabilidade da mensagem. Esses pares variante–efeito são chamados de loci quantitativos moleculares, ou molQTLs. Os mapas revelaram milhares desses sítios em cada tipo celular e, de forma marcante, mais de quatro em cada cinco foram específicos ou das células mononucleares mistas ou dos neutrófilos, ressaltando o quão diferentemente o mesmo genoma pode ser lido em diferentes células imunes.
Encontrando redes que ligam genes a características imunes no animal inteiro
Para ver como esses interruptores moleculares se relacionam com a imunidade do animal inteiro, os cientistas combinaram os mapas de molQTLs com exames de sangue padrão e medidas de proteínas de sinalização imune. Eles construíram redes de co-expressão—grupos de genes que tendem a subir e cair juntos—e investigaram quais se correlacionavam com características como a proporção de neutrófilos ou linfócitos, contagem de leucócitos ou níveis de interferons e fator de necrose tumoral. Módulos ligados a características de linfócitos foram enriquecidos em vias da imunidade adaptativa, enquanto os associados a traços de neutrófilos destacaram defesas inatas rápidas e sinalização inflamatória. Muitos genes-chave nesses módulos foram diretamente regulados por molQTLs específicos de tipo celular, sugerindo rotas claras do variante de DNA até a alteração na composição ou função celular.
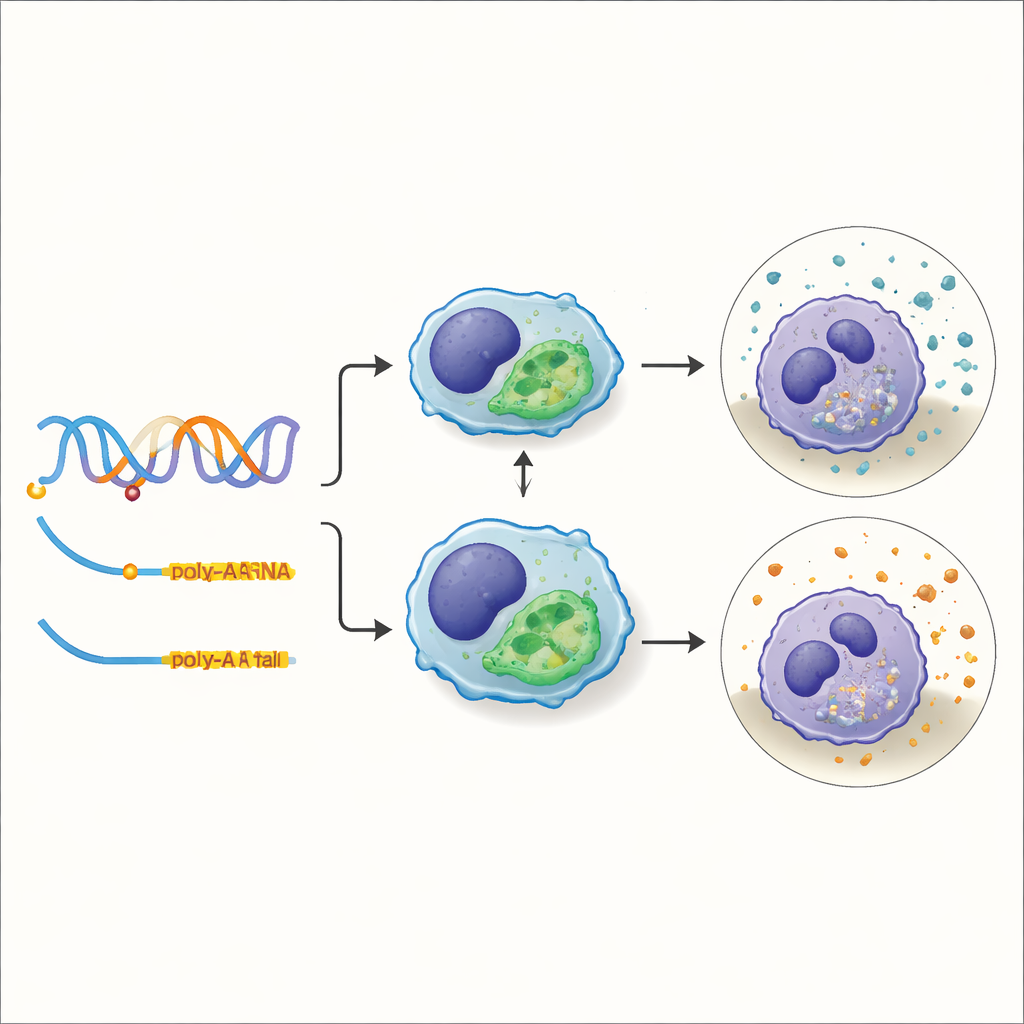
Focando em uma variante que ajusta a capacidade de “limpeza” celular
Uma das características mais práticas examinadas pela equipe foi a capacidade fagocitária—a habilidade das células imunes de englobar e eliminar detritos ou patógenos. Sobrepondo seus molQTLs com resultados de estudos de associação genômica ampla para fagocitose, eles identificaram 588 regiões onde a mesma mudança no DNA provavelmente impulsiona tanto uma alteração molecular quanto uma mudança no desempenho de limpeza celular. Um exemplo de destaque foi uma variante dentro de um gene chamado TXNDC15. Essa mudança não simplesmente ligava ou desligava o gene; em vez disso, alterou qual sítio de poliadenilação a célula escolhia para o RNA desse gene. Porcos portadores de uma versão da variante favoreciam uma cauda mais curta no RNA, que se mostrou mais estável e se acumulou em níveis mais altos, e esses animais exibiram maior atividade fagocitária em suas células imunes.
O que isso significa para porcos mais saudáveis e além
Em termos práticos, este trabalho mostra como pequenas diferenças no DNA podem reconfigurar as “instruções” dentro de tipos celulares imunes específicos e, por meio disso, influenciar quantas dessas células existem e quão bem desempenham suas funções. Ao separar cuidadosamente os tipos celulares e acompanhar não apenas a atividade gênica, mas também como as mensagens são recortadas e finalizadas, o estudo revela pontos de controle ocultos que estudos em tecido misto deixam passar. O mapa genético resultante fornece uma base para selecionar porcos naturalmente mais resistentes a doenças, potencialmente reduzindo a necessidade de antibióticos. Ao mesmo tempo, porque a imunidade suína se assemelha bastante à nossa, esses insights também podem ajudar cientistas a entender como mecanismos semelhantes operam na saúde e na doença humanas.
Citação: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Palavras-chave: imunidade suína, variantes genéticas, células imunes, fagocitose, QTLs moleculares