Clear Sky Science · pt
Inibição de ATM Melhora a Eficiência de Knock-in ao Suprimir a Ativação de Vias Apoptóticas Induzidas por AAV
Tornando a Edição Genética Mais Eficaz
A edição gênica com CRISPR promete tratamentos para doenças genéticas, culturas mais resistentes e ferramentas de pesquisa poderosas. Mas um dos seus truques mais valiosos — inserir com precisão novo DNA em um local escolhido do genoma, conhecido como “knock-in” — ainda funciona com pouca eficiência. Este estudo investiga por que algumas células aceitam novo DNA mais facilmente do que outras e revela uma forma de induzir as células a realizarem edições precisas com maior frequência, especialmente ao usar o vírus adeno-associado (AAV), um veículo de ponta para terapia gênica.
Observando o Reparo do DNA em Tempo Real
Para entender o que ajuda ou atrapalha a inserção genética precisa, os pesquisadores construíram um “painel de controle” intricado dentro de células-tronco embrionárias de camundongo. Esse sistema triplo de repórteres usa três marcadores fluorescentes para acompanhar, nas mesmas células, se o CRISPR cortou o DNA, se ocorreu um knock-in preciso e se a célula, em vez disso, integrou o DNA doador por um método de reparo mais grosseiro. Ao ler combinações de cores diferentes por citometria de fluxo, eles puderam separar edições limpas baseadas em molde de inserções propensas a erros e células não editadas. Esse acompanhamento lado a lado permitiu mapear como diferentes vias de reparo do DNA contribuem para cada resultado com muito mais resolução do que testes antigos baseados em PCR.
Dois Doadores de DNA, Duas Respostas Muito Diferentes
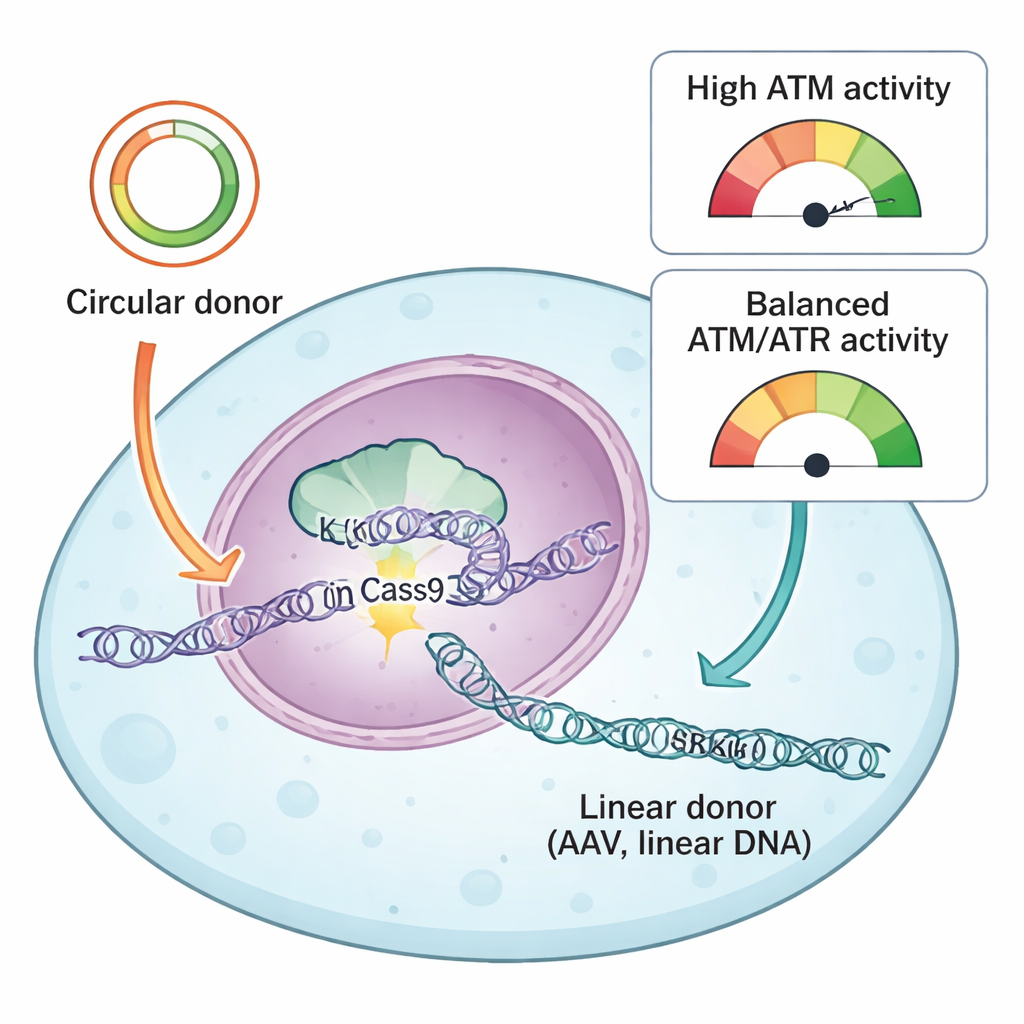
A equipe comparou dois tipos comuns de DNA doador usados para guiar os reparos do CRISPR: plasmídeos circulares e DNA linear derivado de AAV. Ambos carregam “braços de homologia” correspondentes que dizem à célula onde inserir a nova sequência, mas entram na célula em formas físicas diferentes. Plasmídeos circulares são laços fechados de DNA de fita dupla, enquanto doadores de AAV tipicamente chegam como moléculas lineares simples. Usando seu sistema de repórteres e uma biblioteca de fármacos que alvos proteínas da resposta ao dano de DNA, os autores descobriram que uma proteína chave, ATR, era uniformemente essencial para knock-ins bem-sucedidos com ambos os tipos de doador. Inibir ATR reduziu fortemente a inserção precisa, enquanto a ativação moderada de ATR via a via KEAP1–NRF2 aumentou a eficiência dos knock-ins, especialmente com doadores AAV.
Quando a Proteção do DNA Volta-se Contra
Um sensor diferente do dano ao DNA, ATM, mostrou-se notavelmente dependente do tipo de doador. Com doadores plasmidiais circulares, bloquear ATM reduziu tanto o knock-in preciso quanto as inserções mediadas por end-joining, condizendo com seu papel clássico em ajudar as células a reparar quebras de fita dupla. Mas com DNA linear — seja de AAV, AAV auto-complementar ou plasmídeos cortados em fragmentos retos — a inibição de ATM teve o efeito oposto: aumentou a eficiência de knock-in. Os pesquisadores rastrearam esse efeito à forma como as células interpretam surtos de DNA linear. Doses altas de AAV ativaram fortemente ATM, que por sua vez ligou p53 e caspase 3, atores centrais da morte programada. Células que haviam absorvido muitas cópias do DNA doador, e portanto tinham maior chance de um knock-in bem-sucedido, também eram as mais suscetíveis a serem eliminadas por esse sistema de alarme.
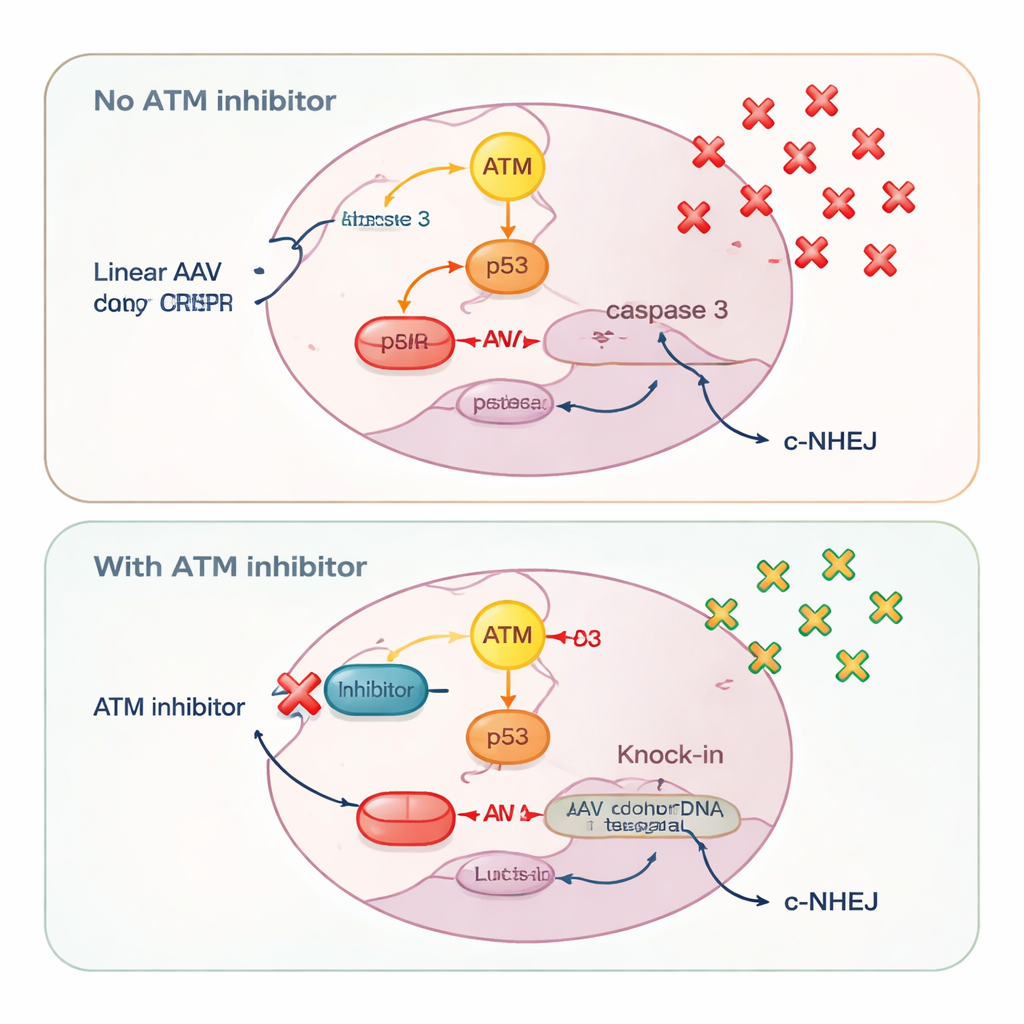
Salvando as Células Melhor Preparadas
Ao adicionar inibidores de ATM, os cientistas silenciaram a via de morte ATM–p53–caspase 3. Isso poupou células que carregavam grandes quantidades de DNA doador, permitindo que mais delas sobrevivessem tempo suficiente para completar um knock-in preciso. Medições de cópias do genoma viral confirmaram que a inibição de ATM aumentou o número de moléculas de AAV retidas dentro das células. Ao mesmo tempo, o bloqueio de ATM atenuou ligeiramente uma via de reparo rápida e brusca chamada junção de extremidades não homóloga clássica, como mostrado pela redução da ativação de DNA-PK, uma enzima central nessa via. Enfraquecer essa opção de reparo concorrente direcionou mais cortes do CRISPR para knock-in baseado em homologia em vez de consertos rápidos que ignoram o molde doador.
O Que Isso Significa para Futuras Terapias Gênicas
Para não especialistas, a mensagem é que as mesmas salvaguardas celulares que nos protegem do dano ao DNA podem sabotar involuntariamente a edição genética precisa, especialmente quando grandes quantidades de DNA doador viral são usadas. Este trabalho mostra que ajustar suavemente essas salvaguardas — mantendo ATR ativo, mas restringindo temporariamente ATM quando doadores lineares como AAV estão presentes — pode tornar os knock-ins por CRISPR mais confiáveis e eficientes. Essa estratégia poderia melhorar terapias gênicas, engenharia celular e modelos de doença ao ajudar mais células a aceitar a alteração pretendida enquanto evita perda celular desnecessária.
Citação: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Palavras-chave: Knock-in com CRISPR, edição gênica com AAV, resposta ao dano de DNA, inibição de ATM, engenharia do genoma