Clear Sky Science · pt
STING controla a glicólise e a lactilação de histonas para impulsionar o reprogramamento metabólico de macrófagos na íleo pós-operatório
Quando a cirurgia coloca o intestino em pausa
Após cirurgia abdominal, muitos pacientes descobrem que seus intestinos simplesmente se recusam a despertar. Essa desaceleração, chamada íleo pós-operatório, pode significar dias de náusea, inchaço e recuperação atrasada. O estudo resumido aqui faz uma pergunta aparentemente simples: por que certas células imunes no intestino mantêm o intestino paralisado, e reduzir um único interruptor molecular poderia ajudar o intestino a voltar a funcionar?
Como uma operação rotineira desencadeia inflamação intestinal
A cirurgia abdominal inevitavelmente perturba os intestinos. Em camundongos, uma manipulação suave do intestino foi suficiente para causar inchaço, acúmulo de líquido e obstrução do conteúdo no intestino delgado. Quando os pesquisadores rastrearam até onde um corante fluorescente inofensivo viajava pelo trato gastrointestinal, viram que a cirurgia retardou fortemente seu progresso, sinal de motilidade prejudicada. O exame microscópico da parede intestinal mostrou que a camada muscular — o tecido que realmente se contrai para empurrar o alimento — tornou‑se inflamada e repleta de células imunes recrutadas, especialmente macrófagos e neutrófilos. Essas descobertas sugerem que a própria camada muscular do intestino torna‑se um campo de batalha inflamado após a cirurgia, e essa inflamação local está intimamente ligada à paralisia intestinal.
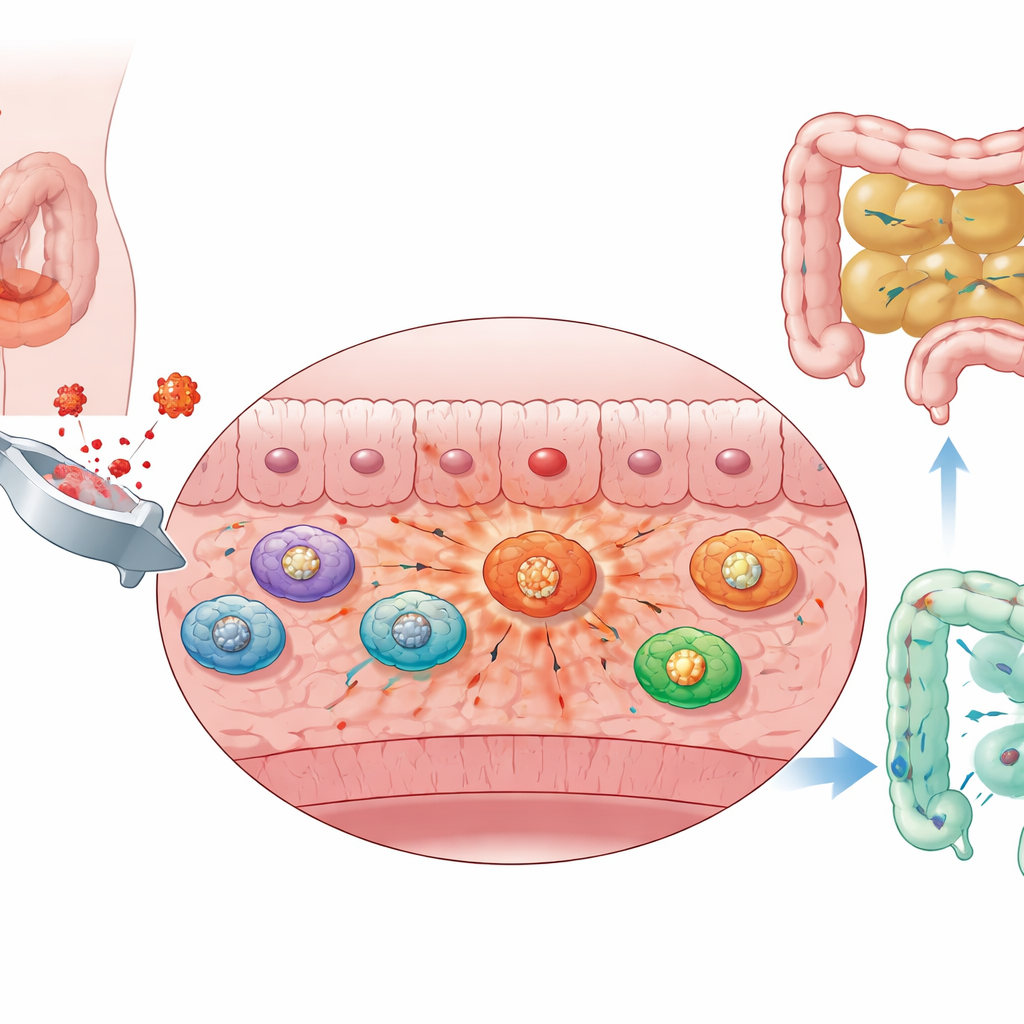
Macrófagos trocam o combustível e atiçam as chamas
Para entender o que esses macrófagos infiltrantes estavam fazendo, a equipe analisou dados de RNA em larga escala e de sequenciamento unicelular da camada muscular intestinal. Eles descobriram que os macrófagos em animais operados aumentaram fortemente uma via rápida de queima de açúcar conhecida como glicólise. Em comparação com outras células imunes no mesmo tecido, os macrófagos infiltrantes mostraram as maiores pontuações de glicólise e expressaram níveis elevados de enzimas glicolíticas-chave. Um subconjunto distinto dessas células dependia fortemente da glicólise, apresentava assinaturas inflamatórias pronunciadas e respondia vigorosamente a componentes bacterianos como o lipopolissacarídeo. Em essência, os macrófagos haviam mudado para um modo de alta queima de açúcar e alta inflamação que parece agravar a inflamação da camada muscular que mantém o intestino imóvel.
Um interruptor molecular que liga a detecção de perigo à queima de açúcar
Os pesquisadores então se concentraram em STING, uma proteína mais conhecida como sistema de alarme para DNA estranho, mas cada vez mais reconhecida como reguladora metabólica. Na musculatura intestinal inflamada, o subconjunto de macrófagos altamente glicolíticos mostrou níveis marcadamente mais altos de STING, um padrão confirmado por coloração tecidual. Em cultura celular, expor macrófagos ao lipopolissacarídeo bacteriano aumentou tanto a atividade de STING quanto as enzimas glicolíticas que ajudam a converter glicose em energia e lactato. Quando os cientistas nocauteavam o gene STING, esse estouro de queima de açúcar colapsou: intermediários glicolíticos caíram, a acidificação do meio de cultura diminuiu e menos espécies reativas de oxigênio foram produzidas. Essas células deficientes em STING também geraram menos lactato, o que implica que a via de alarme e o motor metabólico estão fortemente acoplados.
Do resíduo de açúcar à memória epigenética
O lactato costuma ser visto como um resíduo metabólico, mas aqui ele desempenha um papel mais sutil. A equipe mostrou que em macrófagos normais o dilúvio de lactato é usado para modificar quimicamente histonas — as proteínas que empacotam o DNA — por meio de um processo chamado lactilação. Essa modificação foi especialmente proeminente em um sítio chamado H4K8 em histonas próximas ao gene da HK2, uma enzima glicolítica guardiã. Em células deficientes em STING, a lactilação de histonas e a acessibilidade da cromatina no promotor de HK2 foram ambas reduzidas, e métodos especializados de sequenciamento confirmaram que essas alterações limitaram a ativação de HK2. Ao mesmo tempo, um fator de transcrição a jusante, IRF3, mostrou‑se capaz de se ligar diretamente ao promotor de HK2 com mais facilidade quando essa marca de lactilação de histona estava presente. Juntos, esses passos criam um circuito auto‑reforçador: STING estabiliza fatores que impulsionam a glicólise, a glicólise produz lactato, o lactato decora histonas para abrir o gene HK2, e IRF3 aumenta a expressão de HK2, alimentando ainda mais a glicólise e a inflamação.
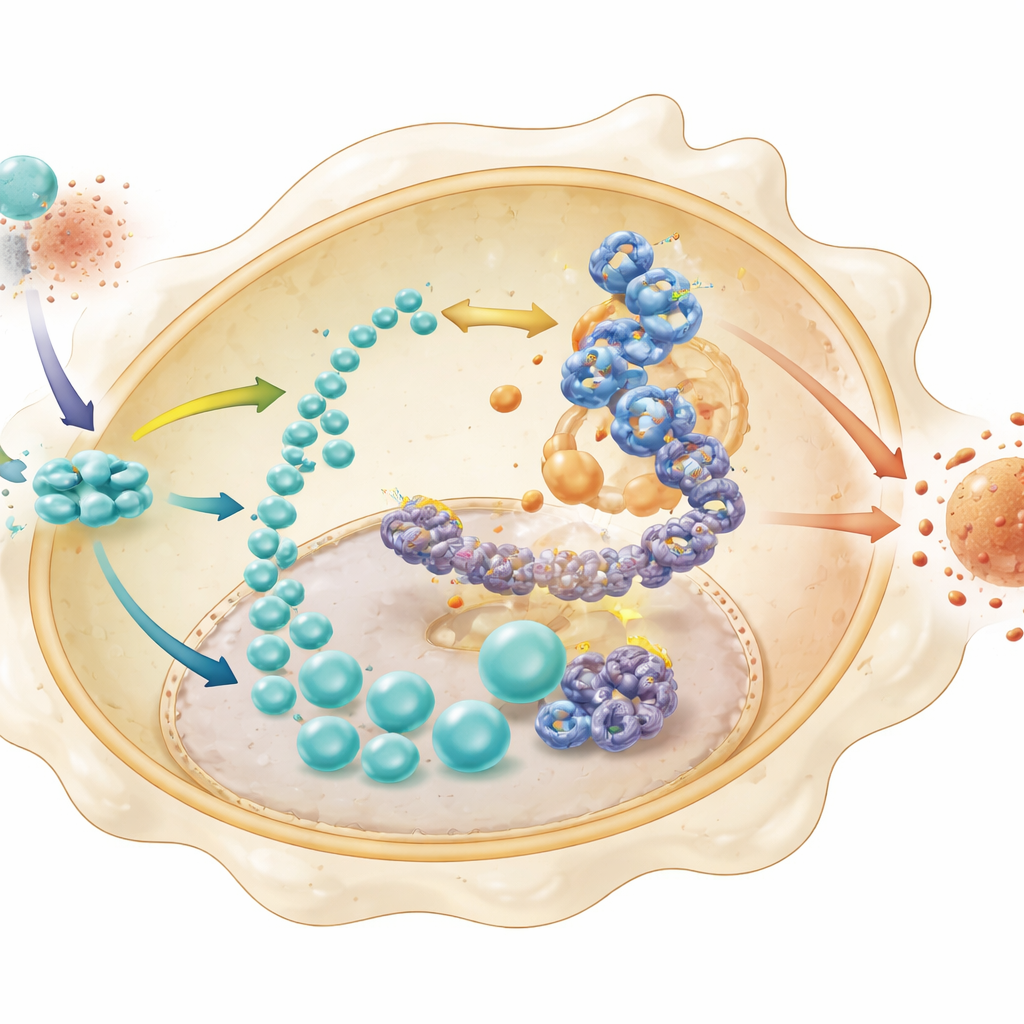
Quebrando o ciclo para permitir a recuperação intestinal
Por fim, a equipe perguntou se romper esse circuito poderia realmente ajudar os animais a se recuperarem do íleo pós‑operatório. Em camundongos sem STING, o tecido muscular intestinal expressou menos enzimas glicolíticas, continha menos macrófagos inflamatórios e mostrou um deslocamento de um estado macrófago agressivo e pró‑inflamatório para um perfil mais resolutivo. A infiltração de neutrófilos foi menor e o trânsito intestinal melhorou. Bloquear farmacologicamente STING em camundongos normais trouxe benefícios semelhantes, enquanto reativar a enzima HK2 em animais deficientes em STING restaurou parcialmente a inflamação e os problemas de motilidade. Para um leitor leigo, a mensagem é clara: um único interruptor sensor de perigo em macrófagos intestinais pode reprogramar seu metabolismo de modo a prender o intestino numa pausa prolongada após a cirurgia. Mirar no STING — ou no ciclo de retroalimentação queima‑de‑açúcar/lactato que ele controla — oferece um caminho promissor para acelerar a recuperação e aliviar uma das complicações mais persistentes das operações abdominais.
Citação: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Palavras-chave: íleo pós-operatório, metabolismo de macrófagos, via STING, glicólise, inflamação intestinal