Clear Sky Science · pt
Caracterizando a desenvolvibilidade de nanocorpos para melhorar o desenho terapêutico usando o Therapeutic Nanobody Profiler
Por que os primos diminutos dos anticorpos importam para os medicamentos do futuro
Muitos dos medicamentos de maior sucesso hoje são anticorpos — proteínas que se ligam aos alvos da doença com grande precisão. Uma classe mais recente de ligantes ainda menores, chamados nanocorpos, pode infiltrar‑se em bolsões de difícil acesso em vírus, tumores e outras moléculas. Mas ser capaz de se ligar a um alvo não basta: um candidato a medicamento também precisa ser fácil de produzir, estável no frasco e seguro no organismo. Este artigo apresenta o Therapeutic Nanobody Profiler, uma ferramenta computacional projetada para ajudar cientistas a avaliar, de forma precoce e apenas a partir da sequência, quais nanocorpos têm maior probabilidade de se tornar medicamentos práticos.
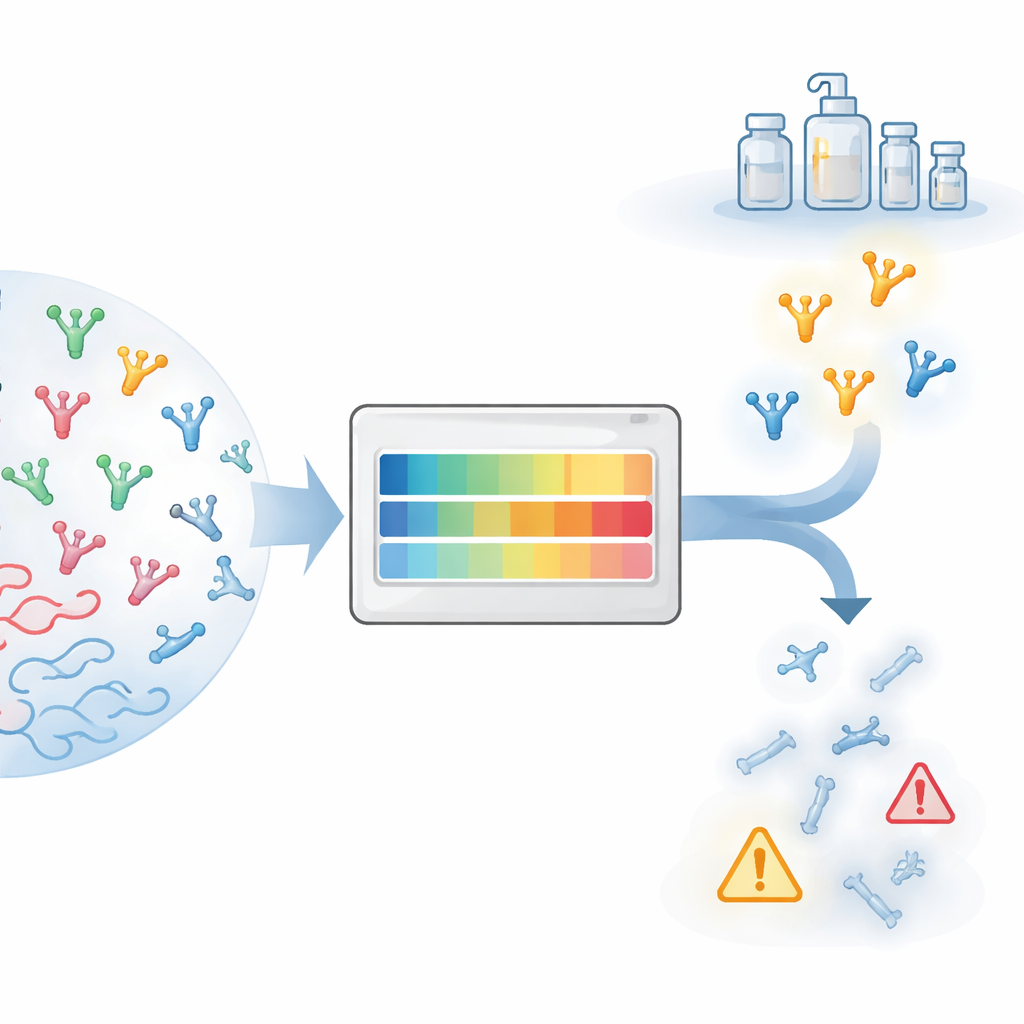
Da ideia promissora ao fármaco prático
Transformar uma proteína em uma terapia real envolve uma série de dificuldades práticas agrupadas sob o termo “desenvolvibilidade”. As proteínas precisam ser produzidas em grandes quantidades, permanecer solúveis, evitar aglomeração e manter‑se estáveis durante transporte e armazenamento. Na última década, os pesquisadores aprenderam a prever muitas dessas características para anticorpos monoclonais de tamanho integral, apoiados por abundantes dados clínicos e testes laboratoriais especializados. No entanto, os nanocorpos são estruturalmente diferentes: consistem de um único domínio em vez de um par de cadeias, frequentemente têm laços de ligação mais longos e expõem regiões de superfície que ficam enterradas em anticorpos convencionais. Como resultado, métodos ajustados para anticorpos regulares podem fornecer respostas enganosas quando aplicados a nanocorpos.
Um profiler construído para as peculiaridades dos nanocorpos
Para enfrentar esse desencontro, os autores projetaram o Therapeutic Nanobody Profiler (TNP), inspirado por uma ferramenta anterior para anticorpos padrão, mas reengenheirado em torno da biologia dos nanocorpos. Eles compilaram sequências de nanocorpos de muitas fontes: ensaios clínicos, repertórios imunes naturais, patentes, artigos científicos e estruturas cristalinas conhecidas. Usando preditores estruturais baseados em deep learning adaptados a anticorpos de domínio único, geraram modelos 3D para essas sequências. A partir de cada modelo, mediram o comprimento dos laços de ligação, o quanto um laço-chave se projeta a partir do corpo da proteína e como grupos de resíduos hidrofóbicos e carregados se organizam na superfície — características que influenciam fortemente solubilidade, agregação e adesão não específica.
Dois estilos estruturais, ambos viáveis
Uma das descobertas mais marcantes diz respeito ao principal laço de ligação, conhecido como CDR3. Quando a equipe quantificou quão “compacto” esse laço é — comparando seu comprimento com a distância que ele se estende a partir da proteína — encontraram uma divisão clara em dois estilos estruturais. Em um subtipo, o laço é mais longo e dobra‑se sobre o lado da proteína, formando muitos contatos estabilizadores com um conjunto de resíduos característicos. No outro, o laço projeta‑se mais, como em um fragmento de anticorpo convencional. Nanocorpos em estágio clínico ocupam ambos os subtipos e, quando os pesquisadores compararam diversas medidas experimentais práticas — como agregação, auto‑associação e estabilidade térmica — não observaram penalidade sistemática para nenhum dos estilos. Isso significa que os projetistas de fármacos não precisam favorecer um formato geral de laço em detrimento do outro, contanto que as demais propriedades pareçam aceitáveis.
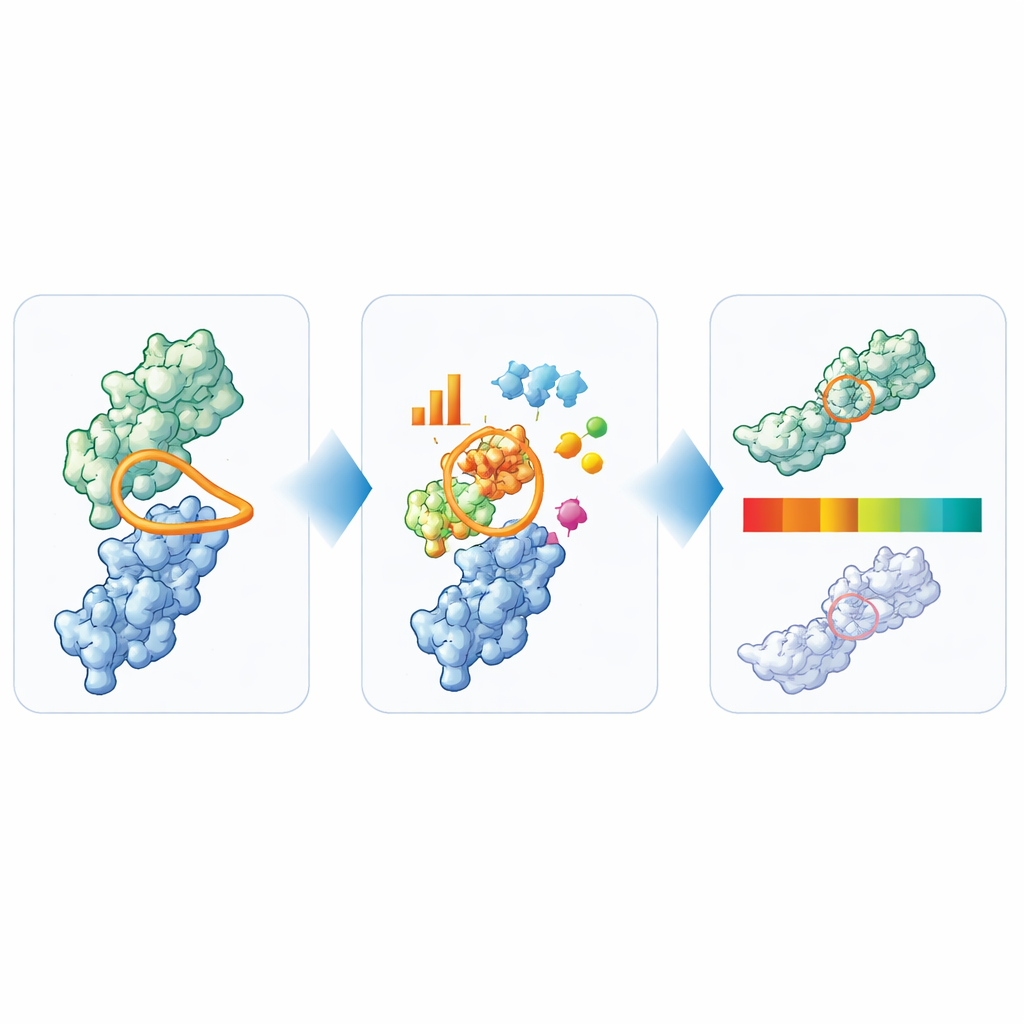
Transformando estrutura em sinais simples de semáforo
A partir de sua análise ampla, os autores destilaram seis características-chave que, em conjunto, capturam as principais preocupações de desenvolvibilidade para nanocorpos: comprimento total dos laços, o comprimento específico e a compacidade do CDR3, e os tamanhos das manchas de superfície hidrofóbicas, positivamente carregadas e negativamente carregadas ao redor do sítio de ligação. Eles então usaram os 36 nanocorpos que chegaram a testes clínicos para definir limites práticos para cada medida. Valores na região central, bem frequentada, são rotulados como “verde”, valores na fronteira como “âmbar” e outliers claros como “vermelho”. Para testar o quão informativos esses sinais são, aplicaram o TNP a 72 nanocorpos proprietários adicionais e compararam os alertas com um painel extensivo de ensaios laboratoriais. Nanocorpos que o TNP marcou como outliers claros geralmente também mostraram múltiplos sinais de advertência experimentais, enquanto aqueles que pareciam limpos computacionalmente foram com mais frequência bem comportados no laboratório.
O que isso significa para os tratamentos de amanhã
Para não especialistas, a mensagem central é que a forma e o padrão de superfície de um nanocorpo agora podem ser convertidos em um perfil de desenvolvibilidade direto antes que trabalhos laboratoriais caros comecem. O Therapeutic Nanobody Profiler não substitui experimentos, e ainda ocorrem discrepâncias entre previsões e ensaios, especialmente porque os testes de laboratório foram realizados em nanocorpos fundidos a fragmentos maiores de anticorpos. Mas ao sinalizar rapidamente candidatos com laços incomumente longos ou muito compactos ou com manchas de superfície problemáticas, o TNP ajuda a direcionar a atenção para nanocorpos que têm mais probabilidade de se tornar fármacos confiáveis. À medida que mais nanocorpos entrarem em ensaios clínicos e ampliarem o conjunto de referência, essa ferramenta deve se tornar ainda mais precisa, acelerando o desenho de medicamentos pequenos e robustos, semelhantes a anticorpos, para uma ampla gama de doenças.
Citação: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Palavras-chave: nanocorpos, desenvolvibilidade de fármacos biológicos, perfilamento computacional, engenharia de anticorpos, estabilidade de proteínas