Clear Sky Science · pt
Esparsificação e decorrelação da atividade das células granulares no giro denteado pela noradrenalina
Por que um pico de alerta pode afiar as memórias
Momentos que nos despertam — uma quase batida no trânsito, um comentário inesperado, uma reviravolta surpreendente em um filme — costumam ficar na memória bem mais do que um dia comum. Este estudo investiga uma razão central: um químico cerebral ligado ao estado de alerta, a noradrenalina, remodela silenciosamente como uma passagem crítica de memória no hipocampo filtra e separa experiências, ajudando eventos semelhantes a se tornarem mais fáceis de distinguir depois.
O guardião do cérebro para experiências semelhantes
Dentro do hipocampo está o giro denteado, uma região que atua como guardião das novas memórias. Ele recebe informações ricas do córtex entorrinal — sinais sobre onde estamos e o que está acontecendo ao nosso redor — e as converte em padrões de atividade nas células granulares, seus neurônios principais. Teoria e experimentos sugerem que esses padrões devem ser “esparsos” (apenas algumas células ativas ao mesmo tempo) e “descorrelacionados” (experiências diferentes ativam conjuntos distintos de células) para que as memórias não se confundam. Ainda assim, como essa transformação ocorre ao nível de células e circuitos específicos tem permanecido pouco claro.
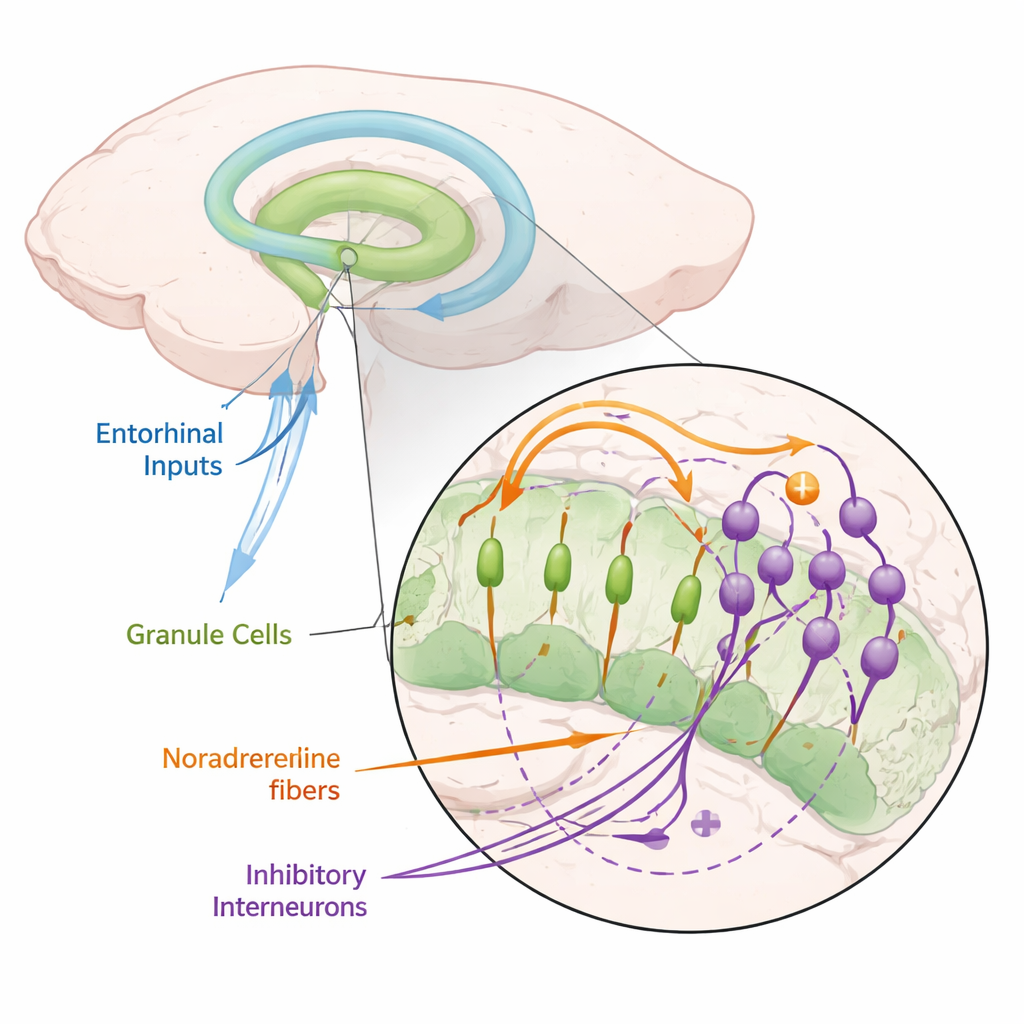
Químico do alerta que silencia células-chave da memória
Os autores focaram na noradrenalina, um neuromodulador liberado por neurônios em uma pequena região do tronco encefálico chamada locus coeruleus, que se ativa durante atenção, novidade e estresse. Em camundongos, expressaram proteínas sensíveis à luz nesses neurônios noradrenérgicos, permitindo a liberação de noradrenalina sob demanda com flashes de luz. Quando estimularam a via de entrada principal para o giro denteado e gravaram de células granulares, descobriram que liberar noradrenalina reduzia fortemente a tendência dessas células de disparar. Essa supressão apareceu tanto no nível de neurônios individuais quanto em sinais populacionais, e foi reproduzida simplesmente banhando fatias em noradrenalina. Bloquear receptores de noradrenalina eliminou o efeito, mostrando que ele realmente dependia desse mensageiro químico.
Não é excitação mais fraca, mas freios mais fortes
Para entender como a noradrenalina silenciou as células granulares, a equipe verificou as possibilidades óbvias. Ela não alterou de forma significativa a voltagem de repouso ou a resistência de entrada das células granulares, o que significa que sua excitabilidade básica permaneceu aproximadamente a mesma. Também não enfraqueceu as correntes excitatórias que essas células recebem do córtex entorrinal. Em vez disso, quando bloquearam receptores GABAA, que mediam a inibição, a noradrenalina deixou de suprimir o disparo das células granulares. Medidas detalhadas de corrente mostraram que a noradrenalina aumentou seletivamente uma forma rápida de inibição feedforward: sinais excitatórios de entrada primeiro acionavam um conjunto de interneurônios, que então inibiam rapidamente as células granulares antes que estas pudessem disparar. Análises de tempo revelaram que essa corrente inibitória sensível à noradrenalina chegava logo após a excitação direta, mas antes da população principal de células granulares disparar, uma característica de freios feedforward.
Células inibitórias especializadas que impõem o tempo
Quais interneurônios forneceram essa inibição crucial? Surpreendentemente, células que expressam parvalbumina, consideradas por muito tempo dominantes no controle rápido feedforward, não foram as responsáveis — a noradrenalina na verdade as tornava menos ativas. Em vez disso, os protagonistas foram interneurônios que expressam colecistoquinina (células CCK). Essas células recebem entrada direta das mesmas fibras corticais que excitam as células granulares e disparam pouco antes das células granulares, indicando um papel feedforward. A noradrenalina despolarizou as células CCK, tornando-as mais fáceis de recrutar, e aumentou com que frequência sinais de entrada as ativavam, sem mudar a força de cada conexão inibitória individual. Quando os pesquisadores bloquearam farmacologicamente a saída das células CCK, a noradrenalina deixou de suprimir a atividade das células granulares. Na prática, a noradrenalina aumenta um circuito de interneurônios CCK que impõe uma janela de tempo muito estreita durante a qual picos excitatórios de entrada podem efetivamente ativar as células granulares.
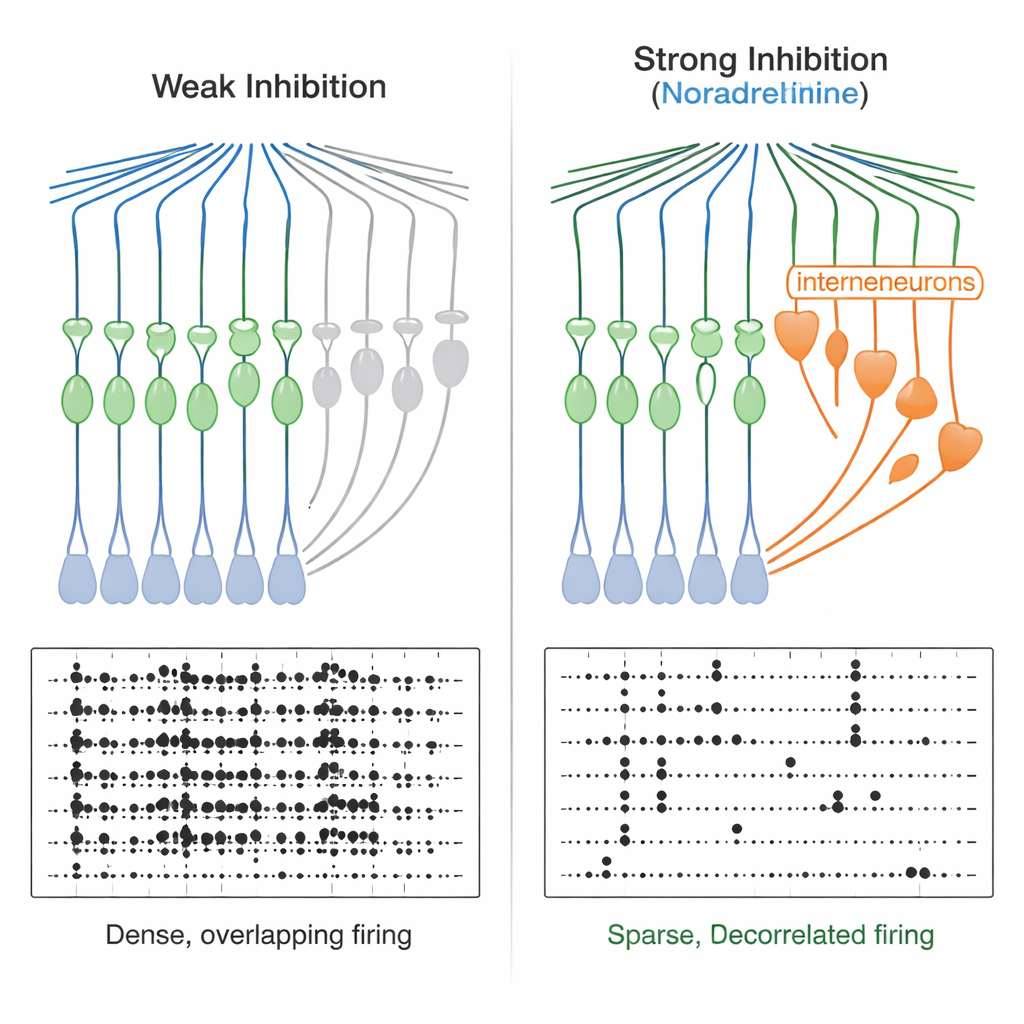
De janelas estreitas a códigos de memória mais limpos
Esse afunilamento do tempo tem consequências poderosas. Quando a equipe entregou pares de entradas excitatórias breves, acharam que em condições normais as células granulares podiam integrar entradas separadas por dezenas de milissegundos em um único pico. Com noradrenalina presente, a janela encolheu para apenas alguns milissegundos — as células granulares passaram a responder quase exclusivamente a entradas altamente sincronizadas. Modelos computacionais de rede confirmaram que tornar a inibição feedforward mais forte e mais rápida produziu saída mais esparsa e reduziu as sobreposições entre padrões de atividade, melhorando a “descorrelação”. Experimentalmente, quando os pesquisadores aplicaram dois padrões de entrada semelhantes, mas não idênticos, ao giro denteado, as células granulares responderam com padrões de disparo mais distintos na presença de noradrenalina, tanto em gravações de célula única quanto em imagens de cálcio em muitas células. Ao mesmo tempo, a atividade global das células granulares tornou-se mais esparsa.
Como o alerta pode nos ajudar a separar memórias semelhantes
Para o leitor leigo, a conclusão é que a noradrenalina, liberada quando estamos alertas ou emocionalmente engajados, ajuda um filtro de memória chave no hipocampo a se tornar mais seletivo. Ao energizar uma classe específica de células inibitórias, ela estreita a janela temporal durante a qual entradas podem ativar as células granulares, de modo que só sinais fortemente sincronizados e relevantes passam. Isso reduz o disparo geral, torna os padrões de atividade menos sobrepostos e ajuda o cérebro a armazenar experiências semelhantes — como duas salas de aula ou duas conversas — como memórias separadas em vez de um borrão. O trabalho revela um mecanismo de circuito concreto que liga o alerta momentâneo a memórias mais precisas e menos confundíveis.
Citação: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Palavras-chave: noradrenalina, giro denteado, interneurônios inibitórios, separação de padrões, memória episódica