Clear Sky Science · pt
Percepções estruturais da helicase WRN revelam estados conformacionais e oportunidades para descoberta de fármacos contra câncer MSI‑H
Por que isso importa para o tratamento do câncer
Alguns cânceres têm uma fragilidade inerente: são incapazes de reparar corretamente erros no DNA. Uma proteína chamada helicase WRN funciona como uma ferramenta molecular de reparo que mantém esses tumores vulneráveis vivos. Este estudo revela, em detalhe atômico, como a WRN se move ao longo do DNA e como fármacos experimentais podem travar seu movimento — oferecendo um roteiro para novos tratamentos que matam seletivamente essas células cancerosas frágeis, preservando o tecido saudável.
O “faz‑tudo” do DNA sob o microscópio
A helicase WRN faz parte da equipe de manutenção da célula, ajudando a desenrolar o DNA para que danos possam ser detectados e reparados. Pessoas nascidas sem a WRN funcional desenvolvem a síndrome de Werner, um distúrbio raro marcado por envelhecimento prematuro, o que mostra o quão crucial essa proteína é para a manutenção do genoma. Tumores com “alta instabilidade de microssatélites” (MSI‑H) — um defeito comum no câncer colorretal e em alguns outros cânceres — mostram dependência especialmente grande da WRN. Quando a WRN é inativada nessas células, seu DNA já frágil rapidamente se desmorona e as células cancerosas morrem. Isso torna a WRN um alvo farmacológico atraente, mas até agora faltava aos cientistas uma visão clara de como a proteína muda de forma ao agarrar o DNA, queimar combustível químico e se deslocar ao longo do material genético.
Observando a WRN flexionar e respirar
Os autores usaram cristalografia de raios X para capturar várias “fotografias” de alta resolução do núcleo da helicase humana WRN. Eles resolveram estruturas da WRN isolada e da WRN ligada a DNA de fita simples e a uma molécula de combustível análoga ao ATP que não pode ser quebrada. Essas vistas revelaram que a proteína é construída a partir de dois lóbulos principais conectados por uma dobradiça flexível que se comporta como uma junta que respira. Em seu estado de repouso, sem combustível, a WRN adota uma forma compacta “fechada” em que os lóbulos ficam próximos. Quando o análogo do ATP e o DNA estão presentes, os lóbulos abrem‑se para uma configuração mais “aberta” que pode acomodar o DNA em uma ranhura carregada positivamente. Um pequeno laço aromático dentro da WRN remodela‑se em um curto hélice e se encaixa entre as bases do DNA, agindo como um catraca que ajuda a proteína a avançar sem deslizar para trás.
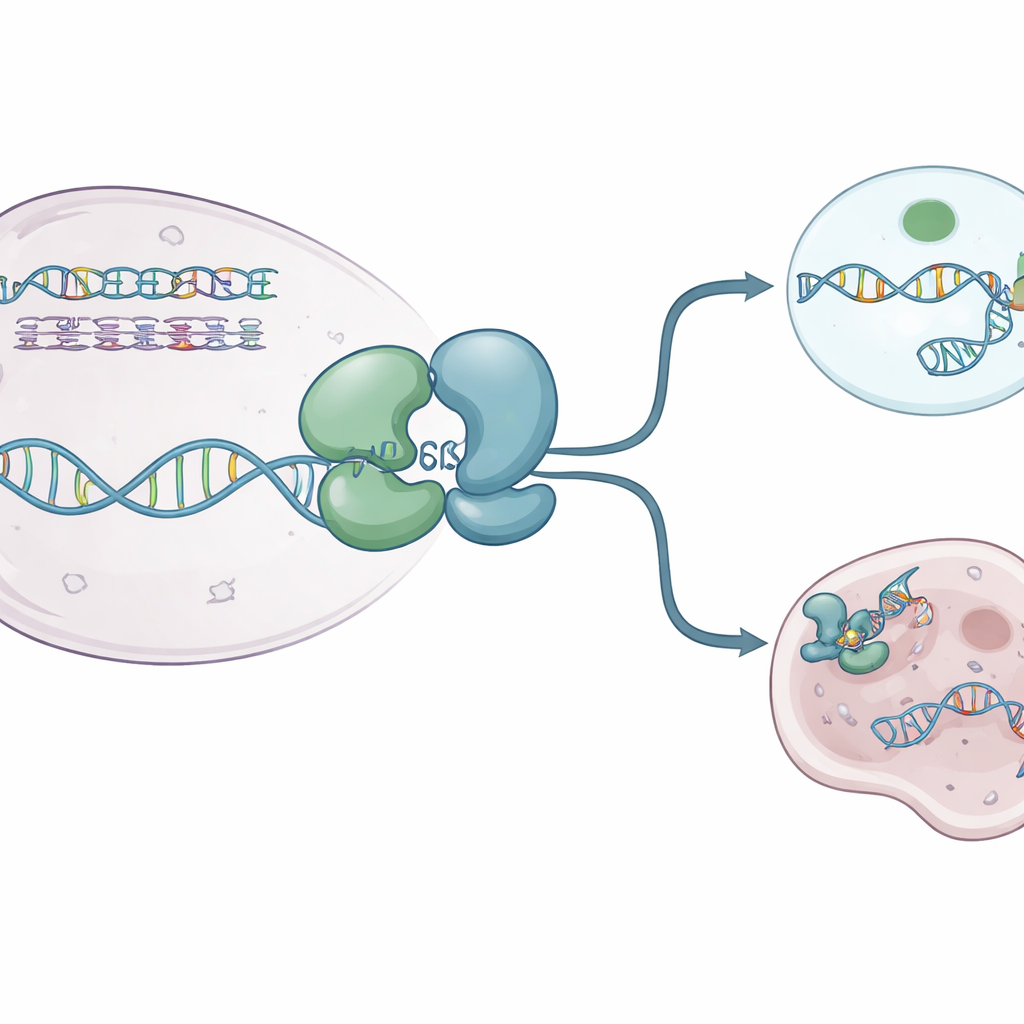
Como os medicamentos atuais desligam a WRN
Vários compostos bloqueadores da WRN entraram recentemente em testes clínicos. Eles não entopem diretamente a ranhura ativa da proteína. Em vez disso, atuam à distância, agarrando a região da dobradiça e travando a WRN em formas que não conseguem se envolver adequadamente com o DNA. Algumas moléculas, como HRO761 e um candidato clínico relacionado da GSK, giram um lóbulo em cerca de 180 graus em relação ao outro, criando uma forma “torcida” dramática que fica afastada do DNA. Outras, incluindo VVD‑133214 e um composto intimamente relacionado estudado aqui, prendem a WRN em um arranjo fortemente “fechado” que não expõe superfícies-chave de agarre do DNA. Experimentos biofísicos confirmaram que, quando esses medicamentos estão ligados, a WRN não consegue mais formar um complexo estável com DNA de fita simples, cortando de fato a ligação entre o uso de ATP e o desenrolamento do DNA.
Como as células cancerosas aprendem a escapar
Para ver como os tumores podem escapar desses medicamentos, a equipe cultivou células de câncer colorretal MSI‑H na presença de inibidores da WRN por semanas a meses. Populações resistentes surgiram rapidamente. A análise genética mostrou que, em cada caso, as células haviam adquirido uma única alteração precisa no gene WRN próxima à dobradiça onde os medicamentos se ligam. Uma mutação enfraqueceu o efeito do inibidor do “estado torcido” HRO761, enquanto outra mutação reduziu a sensibilidade ao VVD‑133214, que favorece o estado fechado. Além disso, muitas células resistentes aumentaram a produção de WRN, dando‑se mais cópias do alvo e diluindo parcialmente o impacto do medicamento. Essas descobertas ecoam padrões de resistência observados com outros fármacos anticâncer direcionados, nos quais pequenos ajustes estruturais na proteína alvo ou a superexpressão podem reduzir a eficácia do tratamento.
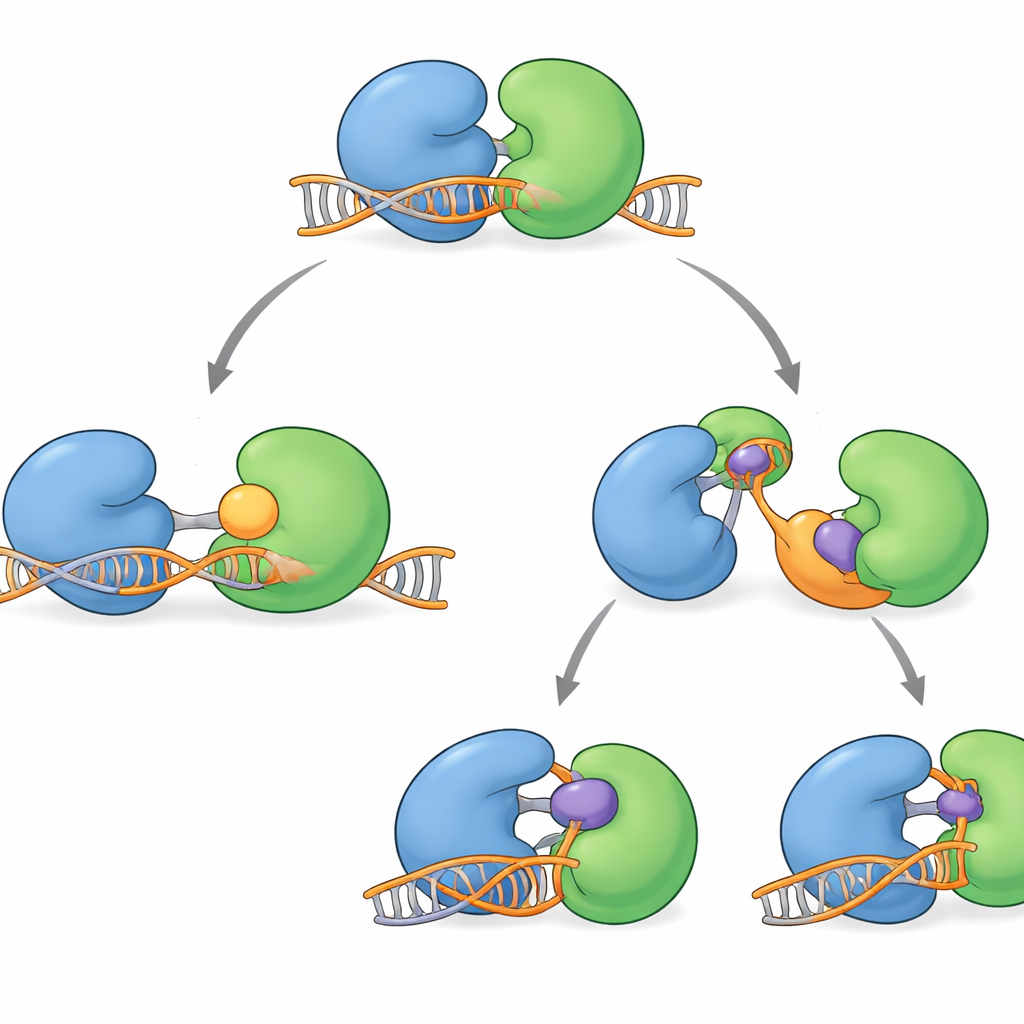
Olhando adiante para bloqueadores de WRN mais inteligentes
Em conjunto, as novas estruturas mapeiam um ciclo de trabalho completo da WRN enquanto ela se prende ao DNA, avança e depois se reinicia. Elas também mostram que os compostos clínicos atuais estabilizam principalmente formas da proteína “fora do DNA”. Para o leitor geral, o ponto-chave é que agora entendemos onde a WRN é vulnerável e como os tumores podem se adaptar. Isso sugere uma próxima geração de inibidores que se liguem à WRN quando ela está presa ao DNA, potencialmente aprisionando‑a em um estado tóxico — de modo semelhante aos medicamentos bem‑sucedidos que aprisionam outras enzimas de reparo do DNA. Esses bloqueadores de WRN “on‑DNA”, usados isoladamente ou em combinação com agentes existentes, poderiam oferecer maneiras mais duradouras de explorar a fraqueza oculta dos cânceres MSI‑H.
Citação: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Palavras-chave: helicase WRN, instabilidade de microssatélites, reparo de DNA, inibidores alostéricos, resistência a medicamentos