Clear Sky Science · pt
PiR48444 inibe a diferenciação osteogênica de CEM e a regeneração óssea ao visar a metilação m6A de BMP2 mediada por METTL7A/eIF4E
Por que moléculas minúsculas são importantes para ossos quebrados
Fraturas e perda óssea relacionada à idade são problemas comuns, e os médicos buscam usar células‑tronco para ajudar o corpo a reconstruir o esqueleto danificado. No entanto, essas células‑tronco nem sempre formam novo osso com a eficiência desejada, especialmente em pessoas mais velhas ou em tecidos inflamados. Este estudo revela uma pequena molécula de RNA, chamada piR48444, que age como um freio molecular nas células‑tronco formadoras de osso. Ao liberar esse freio, os pesquisadores mostram que pode ser possível impulsionar a reparação óssea e proteger contra a perda óssea.
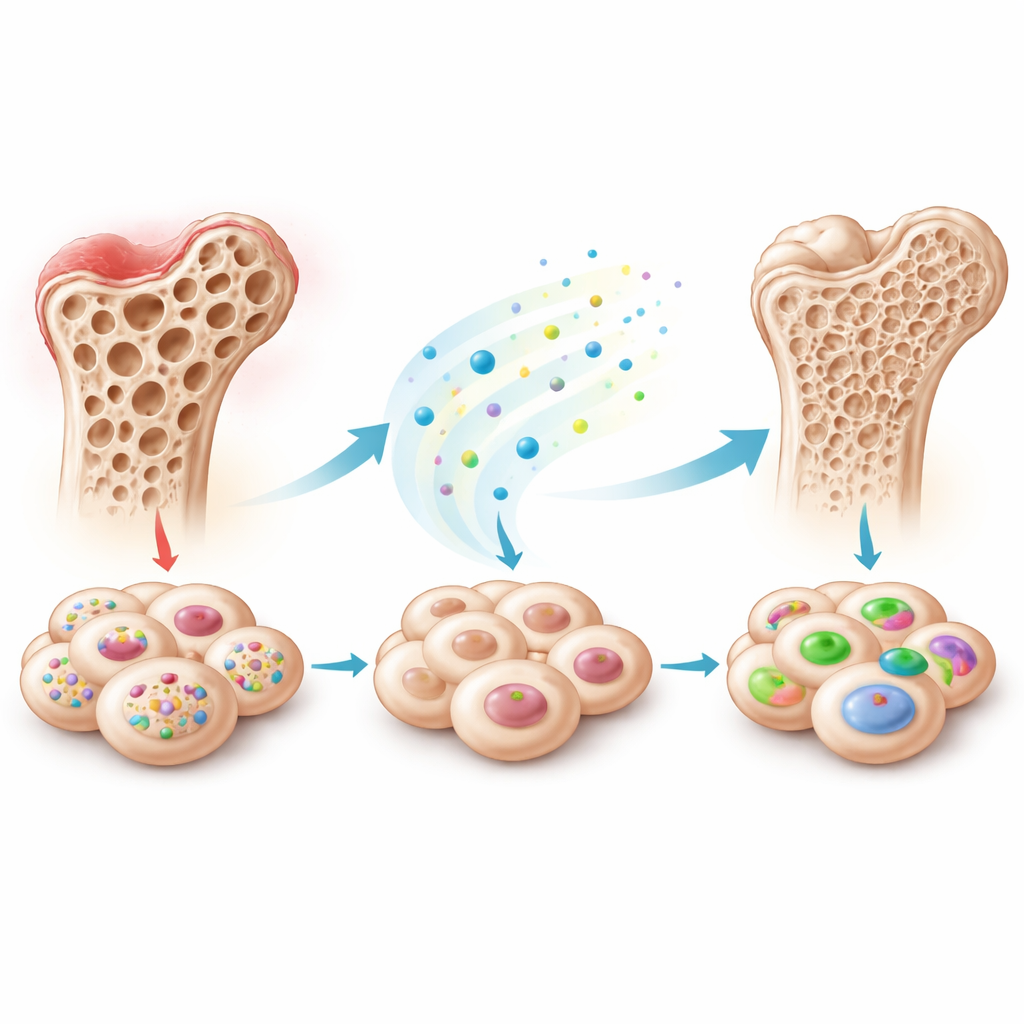
Um freio oculto dentro de muitos tipos de células‑tronco
A equipe concentrou‑se nas células‑tronco mesenquimais, células versáteis que podem se diferenciar em osso, cartilagem, tecido adiposo e outros, e que são isoladas de vários tecidos, como medula óssea, dentes de leite exfoliados e gordura. Quando essas células são induzidas a formar osso em laboratório, milhares de genes e pequenos RNAs alteram sua atividade. Ao sequenciar essas moléculas em células‑tronco de dentes de leite exfoliados, os pesquisadores descobriram que um pequeno RNA em particular, piR48444, diminuía constantemente à medida que as células se direcionavam para o osso. Eles então verificaram outros tipos de células‑tronco e observaram o mesmo padrão: células que formavam mais osso tinham menos piR48444, sugerindo que essa molécula normalmente restringe sua capacidade formadora de osso.
De placas de laboratório para ossos vivos
Para testar essa hipótese, os cientistas alteraram os níveis de piR48444 em vários tipos de células‑tronco. Quando reduziram piR48444, as células depositaram mais cálcio, ativaram genes associados ao osso e passaram a se assemelhar mais a tecido ósseo imaturo ao microscópio. Quando forçaram as células a produzir piR48444 em excesso, ocorreu o contrário: a atividade relacionada ao osso diminuiu. A equipe então avançou para modelos animais. Células‑tronco com piR48444 desativado foram usadas para preencher pequenos defeitos no crânio de camundongos. Essas células modificadas produziram muito mais osso novo do que as células controle, conforme demonstrado por tomografias 3D por raios‑X e colorações de tecido, sugerindo que bloquear piR48444 pode melhorar significativamente a reparação óssea em organismos vivos.
Protegendo ossos frágeis na doença e no envelhecimento
A perda óssea é impulsionada não apenas por lesões, mas também por inflamação e envelhecimento. Em células‑tronco da medula óssea expostas a toxinas bacterianas, e em células‑tronco de animais mais velhos, os níveis de piR48444 estavam anormalmente altos enquanto os marcadores de formação óssea eram baixos. Os pesquisadores criaram um “antagomir” — uma molécula curta projetada para neutralizar piR48444 na corrente sanguínea — e a injetaram em camundongos com perda óssea induzida por inflamação ou em camundongos naturalmente envelhecidos. Em ambos os modelos, os animais tratados preservaram muito mais do osso esponjoso interno, com traveículas ósseas mais densas e numerosas, enquanto a cortical externa permaneceu inalterada. Isso indica que bloquear piR48444 pode proteger seletivamente a parte frágil e metabolicamente ativa do esqueleto que é mais vulnerável durante o envelhecimento e a inflamação crônica.
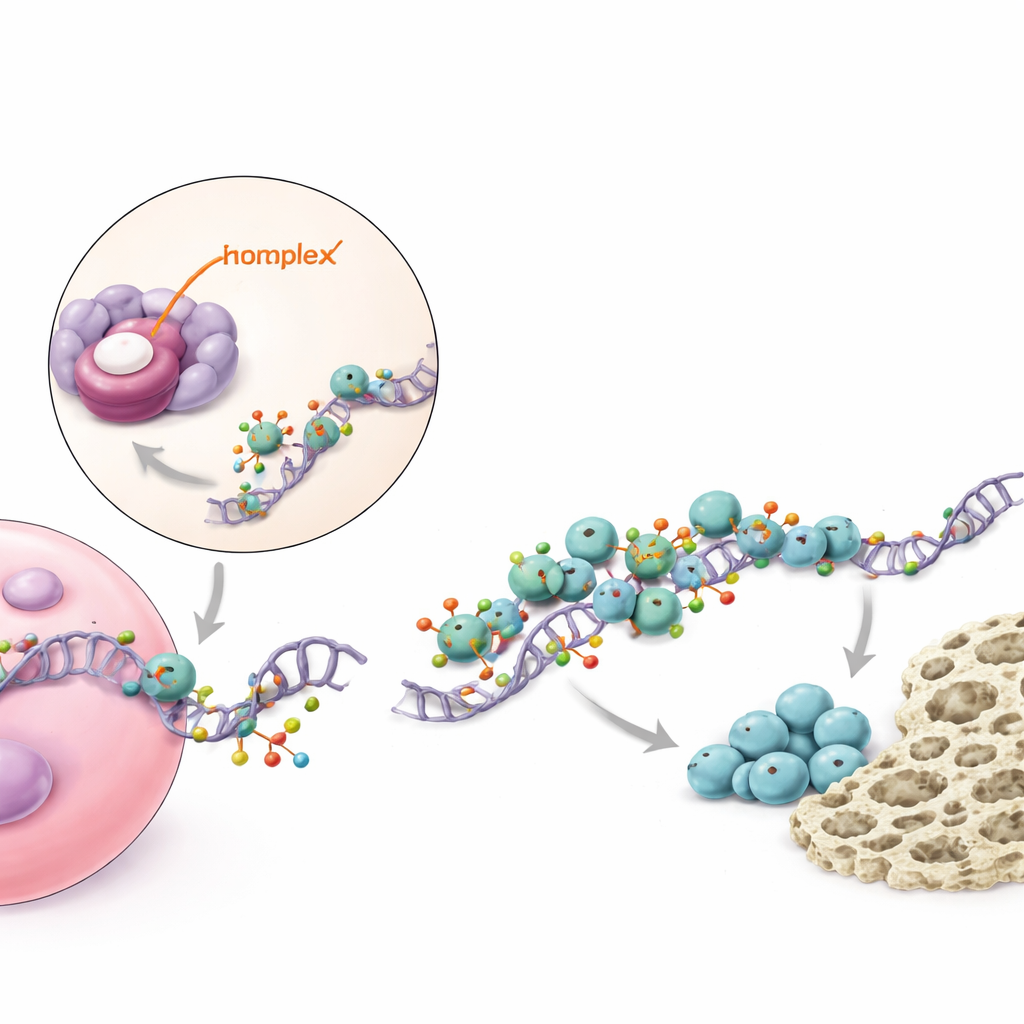
Um circuito molecular que potencializa um sinal ósseo chave
Investigando mais a fundo, o estudo mapeou como piR48444 exerce seus efeitos dentro das células. O pequeno RNA se liga e suprime uma proteína chamada METTL7A, que atua como uma enzima que modifica moléculas mensageiras que carregam a receita para o BMP2, um fator de crescimento bem conhecido que estimula fortemente a formação óssea. METTL7A adiciona pequenas marcas químicas às mensagens de BMP2, tornando‑as mais estáveis e mais fáceis de serem lidas pela maquinaria de produção de proteínas da célula. METTL7A também trabalha em conjunto com outra proteína, eIF4E, que ajuda a iniciar a síntese proteica. Quando piR48444 é abundante, METTL7A fica reprimida, menos mensagens de BMP2 são marcadas e traduzidas, e menos proteína BMP2 é produzida, de modo que as células‑tronco têm menor probabilidade de se tornarem osso. Quando piR48444 é bloqueada, METTL7A e BMP2 aumentam, impulsionando as células em direção à formação óssea.
O que isso significa para a reparação óssea futura
Em termos simples, os autores revelam uma cadeia de controle na qual um pequeno RNA (piR48444) atenua uma enzima auxiliar (METTL7A), que por sua vez limita um potente sinal de construção óssea (BMP2). Ao interromper essa cadeia no nível de piR48444, eles conseguem tornar várias células‑tronco melhores na formação de osso e reduzir a perda óssea em camundongos. Embora segurança, efeitos fora do alvo e desfechos de longo prazo ainda precisem de testes cuidadosos, o trabalho aponta piR48444 tanto como um possível marcador sanguíneo de risco de osteoporose quanto como um alvo promissor para fármacos destinados a aprimorar a regeneração óssea baseada em células‑tronco na clínica.
Citação: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Palavras-chave: regeneração óssea, células‑tronco mesenquimais, osteoporose, RNA não codificante, sinalização BMP2