Clear Sky Science · pt
Afixação local de cátions distorce e amacia o duplex de RNA
Por que essa pequena torção no RNA importa
Dentro de cada célula, DNA e RNA são constantemente dobrados, esticados e torcidos enquanto armazenam e usam informação genética. Esses movimentos não são meros detalhes mecânicos — eles controlam como os genes são lidos, como vírus se copiam e como futuras drogas e nanodispositivos baseados em RNA vão funcionar. Este estudo mostra que sais simples, formados por íons carregados positiva e negativamente, podem alterar dramaticamente o quão rígido ou flexível o RNA é, e que o RNA responde de forma muito diferente do DNA. Entender essa sutil dança de “amolecimento e enrijecimento” pode ajudar cientistas a projetar melhor medicamentos à base de RNA, vacinas e ferramentas moleculares.
Ambientes salgados e moléculas genéticas
DNA e RNA carregam uma forte carga elétrica negativa, por isso estão cercados por nuvens de íons de carga oposta na água. A maior parte do trabalho anterior concentrou-se em íons positivamente carregados, especialmente os multivalentes que têm duas ou três cargas positivas, como magnésio ou espermidina. Sabe-se que esses íons mantêm fitas de DNA juntas, as condensam ou mudam com que facilidade elas se dobram. O RNA, embora quimicamente semelhante ao DNA, comporta-se de modo diferente: geralmente é mais difícil de dobrar, mas mais fácil de esticar. O novo trabalho faz uma pergunta mais profunda: o que acontece quando tanto os íons positivos quanto seus parceiros negativos — chamados ânions — interagem com DNA e RNA em níveis de sal muito altos, bem superiores aos típicos nas células?
Puxando moléculas únicas para medir rigidez
Os pesquisadores usaram uma técnica chamada pinças magnéticas para esticar individualmente hélices duplas de DNA ou RNA, uma por vez. Cada molécula era ancorada a uma superfície de vidro em uma extremidade e a uma pequena esfera magnética na outra. Ao mover ímãs acima da amostra, podiam aplicar forças controladas e registrar quanto cada molécula se estendia e como ela torcia sob tensão. A partir dessas curvas força–extensão, extraíram quatro características mecânicas chave: quão difícil é dobrar a molécula, quão difícil é esticá-la, seu comprimento efetivo por base e como a torção altera seu comprimento. Repetiram essas medições em uma ampla faixa de concentrações de sais multivalentes para vários sais diferentes, incluindo espermidina e cloreto de cálcio.
O DNA novamente se torna mais rígido, mas o RNA de repente amolece
Para o DNA, o comportamento correspondeu em grande parte às expectativas. À medida que a concentração de íons multivalentes positivos aumentava, o DNA primeiro ficou mais fácil de dobrar — sua rigidez diminuiu — porque os íons neutralizaram sua carga negativa. Em níveis ainda mais altos, o excesso de íons positivos compensou demais, efetivamente invertendo a carga líquida do DNA. Essa “inversão de carga” tornou o DNA novamente mais difícil de dobrar, fazendo sua rigidez subir. Surpreendentemente, o RNA mostrou o padrão oposto e mais dramático. Em níveis baixos a moderados de sal, sua rigidez à flexão aumentou: o duplex de RNA ficou mais reto e mais rígido. Mas em concentrações muito altas, a rigidez à flexão do RNA caiu para menos da metade, e outras propriedades como sua extensibilidade e o comportamento torção–extensão inverteram-se de maneiras inesperadas.
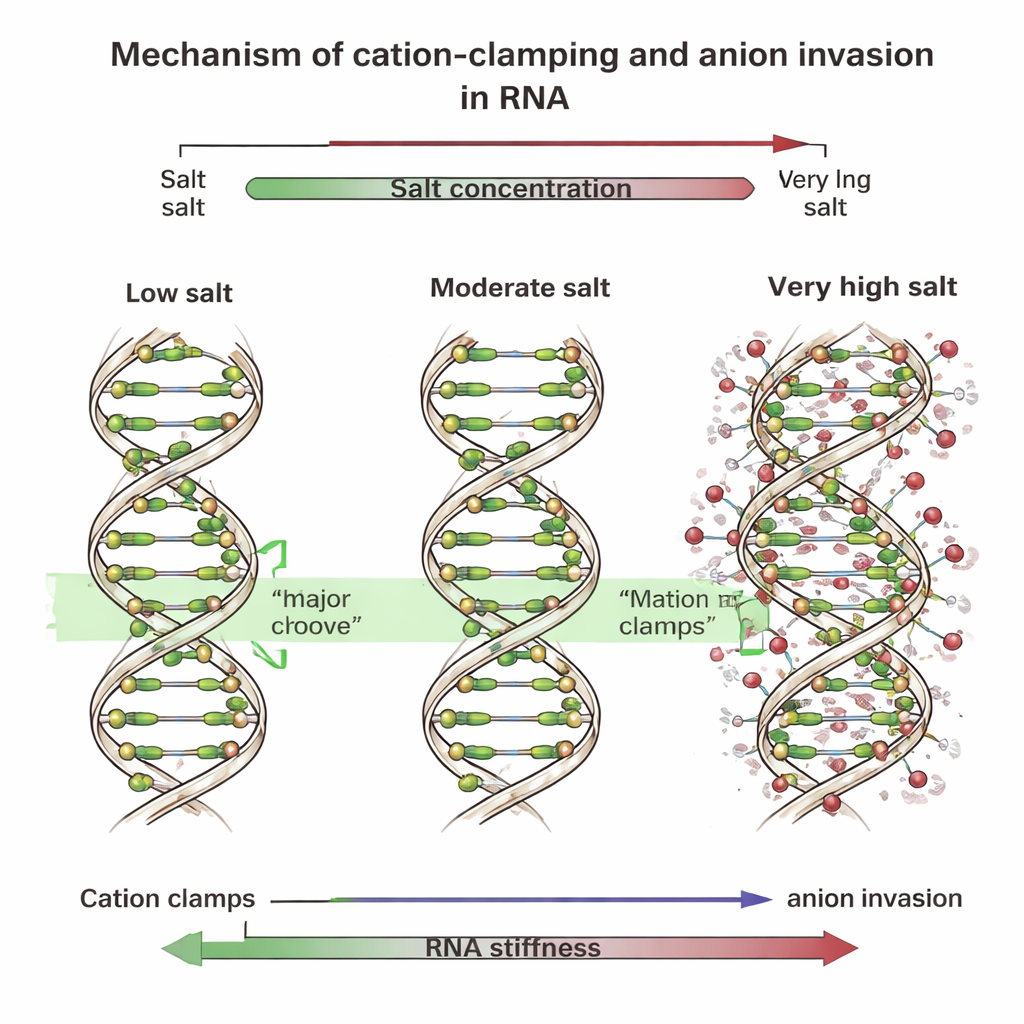
“Grampos”, sulcos e íons invasores
Para descobrir a causa, a equipe realizou simulações computacionais detalhadas que acompanharam cada átomo de fragmentos curtos de DNA e RNA em água salgada. Essas simulações revelaram que, em concentrações baixas e moderadas, íons multivalentes positivos se acomodam em uma ampla superfície do RNA chamada sulco maior. Ali eles formam “grampos de cátions” que fazem a ponte através do sulco, aproximando seus lados, endireitando a hélice e tornando-a mais rígida. O DNA, cujos sulcos têm formato diferente, liga esses íons principalmente ao longo de sua espinha dorsal externa. Em níveis muito altos de sal, contudo, muitos íons negativos — como cloreto — se aproximam da espinha dorsal do RNA e até invadem o sulco maior. Sua presença desorganiza os grampos ordenados, quebrando-os em “grampos locais” irregulares e em manchas que distorcem a hélice. Quando os pesquisadores imitaram esse efeito adicionando molas artificiais ou prendendo íons negativos extras perto do RNA nas simulações, a espinha do RNA se curvou mais e sua rigidez geral despencou, exatamente como observado nos experimentos.
O que isso significa para futuras tecnologias com RNA
Em termos simples, o estudo mostra que o RNA pode ser tornado ora mais reto e rígido, ora mais dobrado e flexível simplesmente alterando o tipo e a concentração dos sais ao redor. Em níveis modestos de íons multivalentes, cargas positivas fixam uniformemente a superfície do RNA e o travam; em níveis extremos, íons negativos invasores quebram esse suporte uniforme e criam regiões deformadas e mais macias. O DNA não mostra esse amolecimento abrupto porque se liga aos íons de modo diferente e passa por inversão líquida de carga em vez disso. Essas percepções destacam que não apenas os íons positivos, mas também seus parceiros negativos são cruciais para controlar a forma do RNA. Esse conhecimento ajudará pesquisadores a ajustar deliberadamente a mecânica do RNA no laboratório — por exemplo, para estabilizar medicamentos de RNA, controlar como o RNA se dobra em biossensores ou projetar nanostruturas baseadas em RNA mais confiáveis.
Citação: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Palavras-chave: Mecânica do RNA, íons multivalentes, fixação de cátions, DNA versus RNA, efeitos do sal