Clear Sky Science · pt
CISH, um ponto de verificação intracelular chave, em comparação e em combinação com pontos de verificação imunes contra o câncer existentes e emergentes
Soltando os Freios das Células que Combatem o Câncer
As imunoterapias contra o câncer mudaram o prognóstico de muitos pacientes, mas uma grande parcela de pessoas ainda obtém pouco ou nenhum benefício. Este estudo explora uma nova maneira de turbinar as próprias células T do corpo — os assassinos do sistema imune — desativando um “freio” interno chamado CISH. Ao contrário dos medicamentos atuais que atuam em chaves na superfície celular, essa estratégia mira um sistema de controle enterrado dentro da célula, com o objetivo de tornar células T engenheirizadas muito melhores em localizar e destruir tumores, mesmo quando os cânceres tentam se esconder.
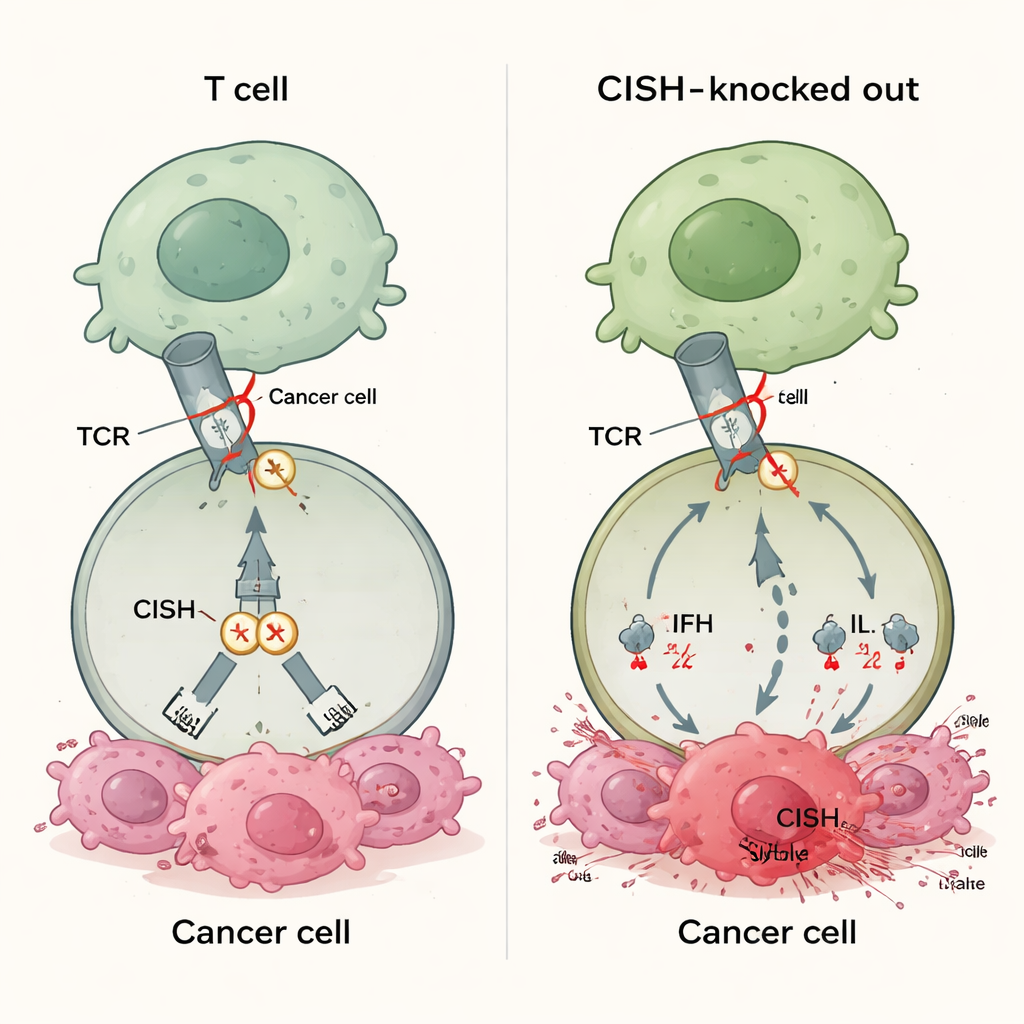
Um Novo Tipo de Freio Imune
A maioria dos medicamentos de imunoterapia aprovados bloqueia proteínas como PD-1 na superfície das células T. Esses fármacos funcionam apenas quando os tumores exibem moléculas parceiras correspondentes, como PD-L1, e muitos cânceres ou nunca expressam quantidade suficiente dessas parceiras ou as perdem ao longo do tempo. Isso ajuda a explicar por que 30–60% dos pacientes não respondem às terapias com pontos de verificação atuais. CISH pertence a uma classe diferente de freios que ficam dentro da célula T. Ele é ativado quando o receptor da célula T percebe um alvo e então atenua o sinal promovendo a degradação de uma proteína de sinalização chave. Como essa ação não depende de ligantes expressos pelo tumor, desligar o CISH poderia, em princípio, aumentar as respostas das células T em muitos tipos de câncer, independentemente do status de PD-L1 ou de outros biomarcadores.
Frente a Frente com Pontos de Verificação Existentes
Os pesquisadores usaram edição gênica CRISPR para remover o CISH e compararam as células T resultantes com células sem PD-1 ou sem outros freios intracelulares. Quando estimularam as células T de forma fraca — uma situação pensada para imitar tumores que exibem apenas pequenas quantidades de antígeno — as células com deleção de CISH produziram muito mais mensageiros imunes chave, incluindo interferon-gama, TNF-alfa e IL-2. Essas células também foram mais “polifuncionais”, o que significa que células T individuais podiam desempenhar várias tarefas ao mesmo tempo, uma marca de atividade antitumoral potente. Em contraste, simplesmente remover PD-1 não ajudou nessas condições de sinal fraco. Em vários testes, a perda de CISH aumentou mais fortemente a ativação, a capacidade de matar e a formação de células T com memória durável do que a eliminação de outros pontos de verificação internos candidatos, como RASA2, CBLB, SOCS1, REGNASE1, HPK1 ou PTPN1/2.
Trabalhando Junto com Outros Interruptores Internos
Como a sinalização das células T é controlada por muitas vias sobrepostas, a equipe investigou se combinar a deleção de CISH com a remoção de outros freios poderia produzir benefícios aditivos. Usando edição CRISPR multiplex, descobriram que deletar CISH junto com SOCS1, HPK1 ou RASA2 aumentou ainda mais a produção de citocinas úteis sob estimulação fraca. Em um modelo tumoral centrado em uma mutação KRAS comum, células T engenheirizadas com um receptor específico para KRAS foram melhores em matar células cancerosas quando CISH foi removido, e esse efeito ficou mais forte quando a perda de CISH foi combinada com a deleção de SOCS1 ou RASA2. Esses achados sugerem que CISH controla um nó não redundante na biologia das células T e pode cooperar com parceiros selecionados para aguçar a capacidade de matar específica ao tumor.
Tornando as Células CAR-T Mais Resistentes Contra Tumores Astutos
Os autores então avaliaram um cenário clinicamente relevante: células CAR-T que miram o marcador de células B CD19. Eles criaram células leucêmicas que expressavam diferentes níveis de CD19 para imitar tumores que perdem ou reduzem seus alvos para escapar da terapia. As CAR-T sem CISH foram notavelmente melhores em destruir células cancerosas, mesmo quando o CD19 era escasso, e secretaram mais sinais de ativação e recrutamento. Ao mesmo tempo, liberaram menores quantidades de moléculas conhecidas por enfraquecer células T ou promover o crescimento tumoral, como Galectina-1, Galectina-3, 4-1BB solúvel, IL-1α e a glicoproteína EMMPRIN/CD147. Em conjunto, essas mudanças apontam para uma célula CAR-T mais agressiva e menos facilmente suprimida, particularmente adequada a ambientes tumorais hostis e com baixo antígeno.
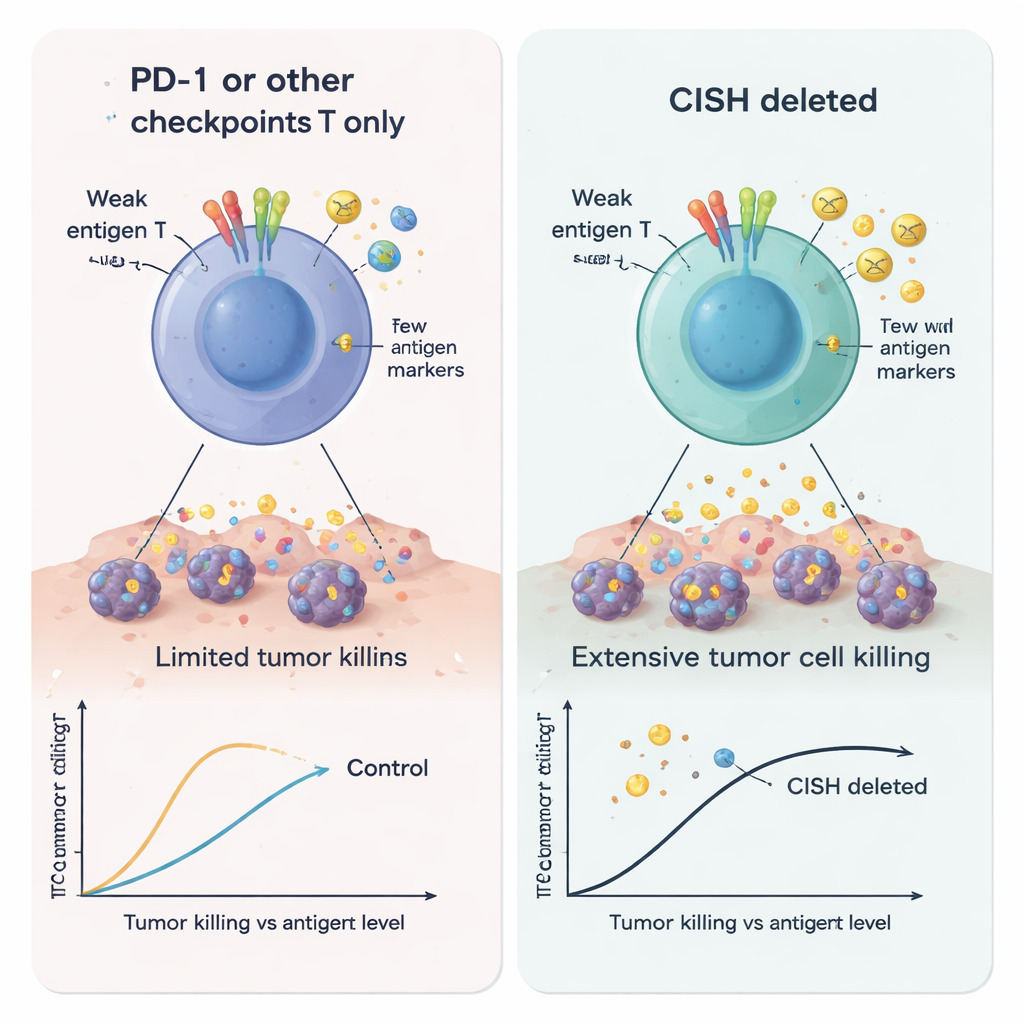
Do Banco de Laboratório aos Pacientes
Além de tubos de ensaio e placas de cultura, a ideia de mirar o CISH já chegou a pacientes. Um ensaio pioneiro em humanos usando linfócitos infiltrantes de tumor editados para remover CISH em uma pessoa com câncer colorretal avançado produziu uma resposta completa que durou mais de dois anos, apesar da resistência do câncer a múltiplos tratamentos prévios. Ao demonstrar que CISH é um ponto de verificação interno potente e passível de intervenção que aumenta a sensibilidade das células T mesmo a sinais tumorais fracos, este estudo ajuda a explicar esse resultado clínico notável e apoia esforços para desenvolver terapias futuras — sejam células editadas por genes ou comprimidos — que afrouxem esse freio interno de forma segura e ampliem o alcance da imunoterapia contra o câncer.
Citação: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Palavras-chave: imunoterapia do câncer, células T, terapia CAR-T, pontos de verificação imunes, edição gênica CRISPR