Clear Sky Science · pt
Uma mutação patogênica em α-SNAP prejudica a ligação lipídica à membrana ao ocultar um loop hidrofóbico crítico
Como uma pequena alteração em uma proteína pode atrapalhar o desenvolvimento do cérebro
Nossas células cerebrais transportam constantemente cargas em pequenas bolhas chamadas vesículas, e uma proteína auxiliar chamada alpha-SNAP é central para que essas entregas ocorram. Uma mutação rara em alpha-SNAP, conhecida por uma linhagem de camundongos chamada “hyh”, causa problemas graves na formação do cérebro e no equilíbrio de fluidos. Este estudo faz uma pergunta aparentemente simples, mas com grandes consequências: essa troca de um único aminoácido em alpha-SNAP impede que ela se prenda às membranas celulares, e isso poderia ser uma razão chave para o mau desenvolvimento cerebral?
Um estivador celular com muitas funções
Alpha-SNAP normalmente atua como uma espécie de estivador para vesículas, ajudando-as a se fundir com as membranas celulares para que cargas possam ser liberadas ou recicladas. Ela coopera com um conjunto de proteínas chamadas SNAREs e com uma máquina que usa energia chamada NSF para aproximar as membranas e depois resetar o sistema para a próxima rodada. Além desse papel clássico, alpha-SNAP também ajuda a controlar processos como autofagia, morte celular, entrada de cálcio e sensoriamento de energia. Todas essas funções dependem, de uma forma ou de outra, da capacidade de alpha-SNAP de tocar e se inserir parcialmente na superfície oleosa das membranas.
Um loop oculto e uma mutação problemática
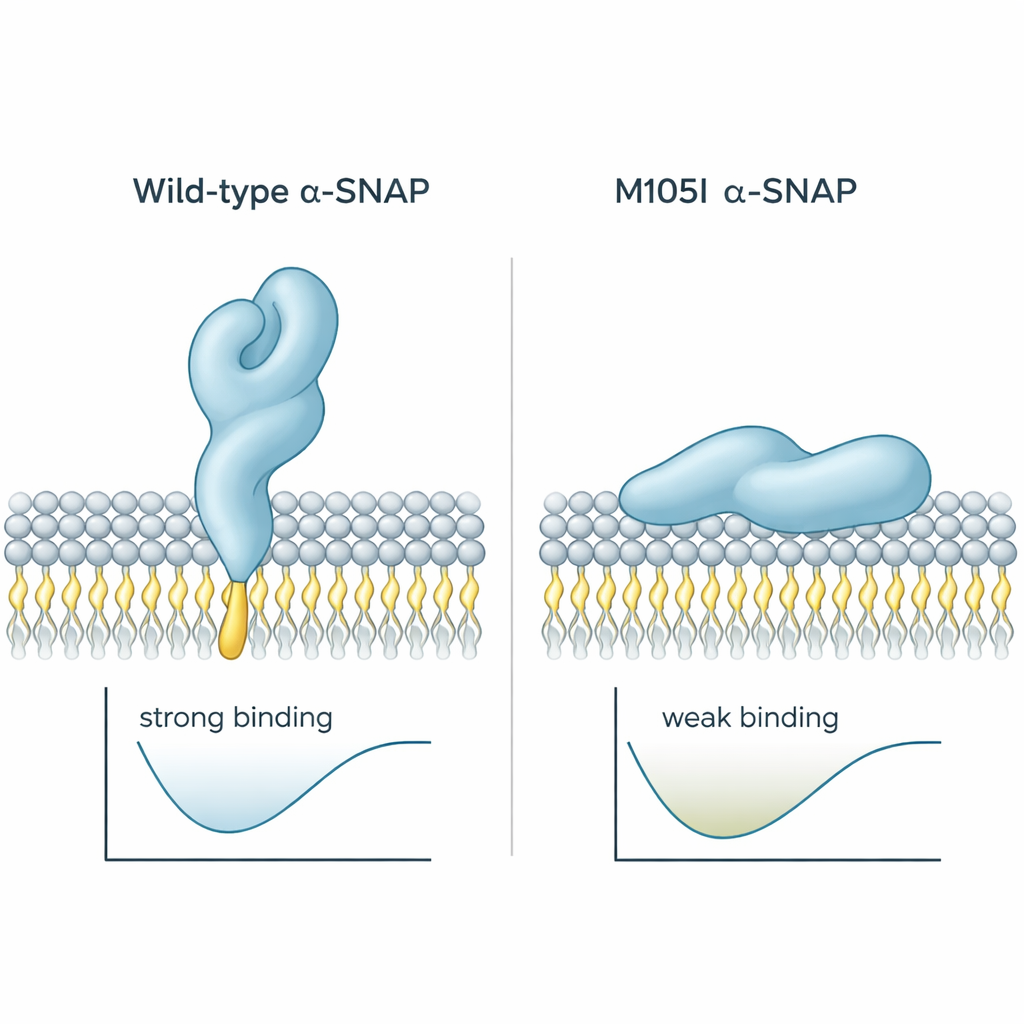
Trabalhos anteriores mostraram que alpha-SNAP usa um curto “loop” graxo perto de uma das extremidades da proteína para se ancorar às membranas. Na proteína saudável, esse loop sobressai e pode mergulhar na camada externa da membrana. No camundongo hyh, um único bloco construtor na posição 105 é trocado, criando a mutação M105I. Os autores usaram simulações computacionais para ver como essa mudança altera a forma da proteína. Eles descobriram que a proteína mutante se torna ligeiramente mais compacta e torce de um modo que encolhe o loop hidrofóbico para dentro, afastando-o da água e das membranas. Como resultado, a proteína mutante se aproxima das membranas com um ângulo mais raso e tende a pressioná-las com uma região menos aderente, reduzindo tanto o tempo de contato quanto a profundidade de inserção. Cálculos de energia de ligação corroboraram isso: a proteína selvagem acomodou-se em um estado de baixa energia e fortemente ligado, enquanto a mutante preferiu contatos mais fracos e rasos.
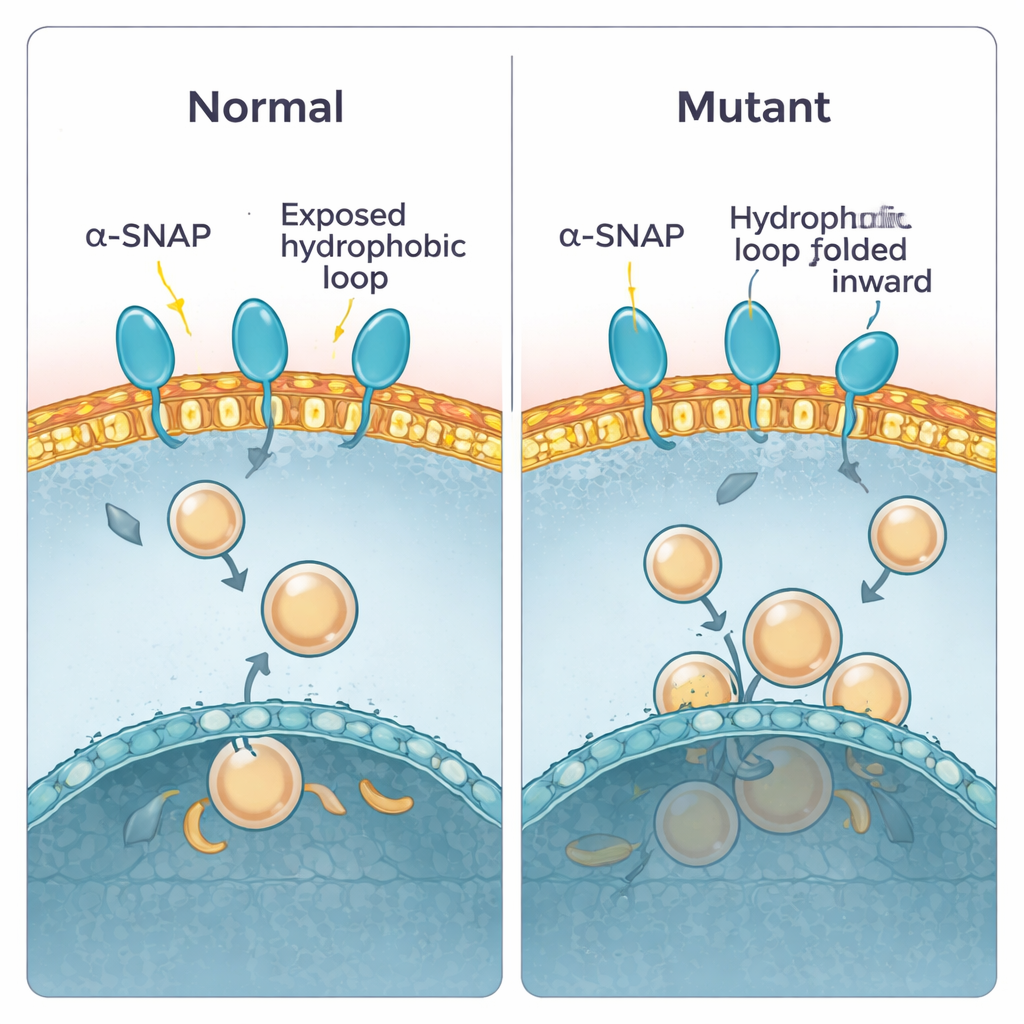
Colocando a previsão à prova no laboratório
Para verificar essas previsões, a equipe purificou tanto a alpha-SNAP normal quanto a mutante e testou como elas se comportavam em diferentes preparações experimentais. Primeiro, usaram um detergente que se separa em fases aquosa e oleosa, imitando a escolha entre água e membrana. A alpha-SNAP normal se repartiu de forma equilibrada, consistente com uma superfície parcialmente oleosa. A versão mutante mostrou menos disposição para entrar na fase oleosa, sugerindo que suas partes graxas estão de fato mais enterradas. Em seguida, deixaram as proteínas interagirem com “folhas” planas de membrana plasmática preparadas a partir de células e imagearam quantos pontos de ligação apareciam. Novamente, a alpha-SNAP normal pontilhava a membrana, enquanto a mutante se ligou muito menos. Por fim, flutuaram bolhas artificiais de membrana (lipossomos) feitas de lipídios cerebrais através de gradientes de açúcar. A alpha-SNAP selvagem subiu com as vesículas ricas em lipídios de membrana plasmática, enquanto a mutante ficou para trás, ligando-se mal, a menos que as vesículas fossem feitas de uma mistura de membrana mais interna.
Consequências no cérebro em desenvolvimento
Os pesquisadores então analisaram cérebros de embriões de camundongo em desenvolvimento, focando em um estágio em que novos neurônios estão sendo gerados. Ao separar o conteúdo celular em frações solúveis e ligadas à membrana, mostraram que os níveis totais de alpha-SNAP já estavam reduzidos nos cérebros hyh, mas, mais importante, a fração presa às membranas era desproporcionalmente baixa em comparação com camundongos normais. Quando separaram ainda mais diferentes tipos de membrana, constataram que a maior perda ocorria na membrana plasmática, a superfície externa da célula, enquanto membranas internas foram muito menos afetadas. A microscopia contou a mesma história: em tecido normal, alpha-SNAP delineava as células em um padrão de favo que correspondia a um marcador de superfície conhecido. Nos cérebros hyh, essa marcação de borda nítida desbotava para um brilho mais difuso e interno, indicando que a proteína mutante falha em permanecer ancorada na borda celular onde a fusão de vesículas e a sinalização são mais ativas.
Por que isso importa para a doença
Em conjunto, o trabalho mostra que a mutação M105I faz mais do que simplesmente reduzir a quantidade de alpha-SNAP; ela altera o modo como a proteína se dobra de modo que seu loop chave de captura da membrana fica escondido. Isso dificulta que alpha-SNAP agarre a membrana plasmática e assuma a orientação adequada para organizar a maquinaria de fusão. Em um cérebro em desenvolvimento, onde a entrega precisa de sinais e materiais de construção na superfície celular é essencial, essa falha estrutural sutil provavelmente contribui para a hidrocefalia, o córtex mal conectado e outros defeitos observados em camundongos hyh. Para não-especialistas, a mensagem é clara: até uma pequena mudança na forma de uma única proteína pode remodelar a maneira como as células se comunicam e, por sua vez, como um cérebro é construído.
Citação: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Palavras-chave: alpha-SNAP, ligação à membrana, mutação proteica, desenvolvimento cerebral, fusão de vesículas